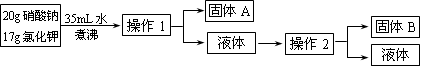
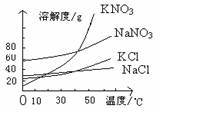
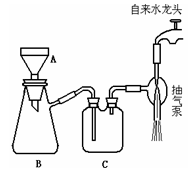
-
属于强电解质的是①NaOH ②NH3·H2O ③CaCO3 ④CH3COOH⑤NaHCO3⑥氢氧化铝⑦氯化铵⑧二氧化碳⑨乙醇⑩铜
A.①③⑥⑦ B.②④⑥⑦ C.①③⑤⑦ D.除⑧⑨⑩
难度: 简单查看答案及解析
-
下列实验操作或原理不正确的是
A.纸层析法中的展开剂之所以能够展开的主要原理是毛细现象
B.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.测定溶液pH的操作:将pH试纸置于表面皿上,用洁净玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较
难度: 简单查看答案及解析
-
以下关于纸层析法的叙述,错误的是
A.纸层析法适用于分离和检验化学性质十分相近的物质
B.用纸层析法可以检验氯化铁溶液中是否混有少量氯化铜
C.配制时试样溶液的浓度较大,点样时试样点斑较小
D.为了看到色斑,只有有色离子的检验才可以用纸层析法
难度: 简单查看答案及解析
-
下列叙述正确的是
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO)>c(NH)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1 mol·L-1的氨水中加入少量硫酸铵固体,则溶液中
增大
难度: 简单查看答案及解析
-
下表是常温下某些一元弱酸的电离常数:
弱酸
HCN
HF
CH3COOH
HNO2
电离常数
6.2×10-10
6.8×10-4
1.7×10-5
6.4×10-6
则0.1 mol·L-1的下列溶液中,pH最小的是
A.HCN B.HF C.CH3COOH D.HNO2
难度: 简单查看答案及解析
-
在25℃时,用蒸馏水稀释1 mol·L-1氨水至0.01 mol·L-1,随溶液的稀释,下列各项中始终保持增大趋势的是
难度: 简单查看答案及解析
-
下列各组离子在指定条件下,一定能大量共存的是
A.在
的溶液中:NH4+、Ca2+、Cl-、K+
B.能溶解Al(OH)3固体的溶液:Na+、K+、Cl-、HCO3-
C. pH=1的无色溶液: Fe3+、K+、SO42-、NO3-
D.FeCl3溶液中加入过量Cu粉充分反应后的溶液:Cl-、Cu2+、Fe2+、Fe3+
难度: 简单查看答案及解析
-
某溶液中仅含Na+、H+、OH-、CH3COO-四种离子,下列说法错误的是
A.溶液中四种粒子之间可能满足:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
B.若溶液中粒子间满足:c(CH3COO-)=c(Na+),则该溶液一定呈中性
C..若溶液中溶质仅为CH3COONa且浓度为0.1 mol·L-1,则粒子间一定满足:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.若溶液中的溶质为CH3COONa和CH3COOH,则溶液中粒子间一定满足:
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
难度: 简单查看答案及解析
-
实验室用标准盐酸测定NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是
A.酸式滴定管在装酸液前未用标准盐酸溶液润洗2~3次
B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.锥形瓶内溶液颜色由黄色变橙色,立即记下滴定管内液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
难度: 简单查看答案及解析
-
某学生用碱式滴定管量取0.1 mol·L-1的NaOH溶液,开始时仰视液面,读数为1.00 mL,取出部分溶液后,俯视液面,读数为11.00 mL,该同学在操作中实际取出的液体如图
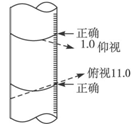
A.大于10.00 mL B.小于10.00 mL C.等于10.00 mL D.等于11.00 mL
难度: 简单查看答案及解析
-
将pH=5的H2SO4溶液稀释1 000倍后,溶液中SO浓度与H+浓度的比值约为
A.1∶10 B.1∶1 C.1∶2 D.1∶20
难度: 简单查看答案及解析
-
NH4Cl溶于重水(D2O)后,产生的一水合氨和水合氢离子均正确的是
A.NH2D·H2O和D3O+ B.NH3·D2O和HD2O+
C.NH3·HDO和D3O+ D.NH2D·HDO和H2DO+
难度: 简单查看答案及解析
-
已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1 mol·L-1的NaA和NaB混合溶液中,下列排序正确的是
A.c(OH-)>c(HA)>c(HB)>c(H+) B.c(OH-)>c(A-)>c(B-)>c(H+)
C.c(OH-)>c(B-)>c(A-)>c(H+) D.c(OH-)>c(HB)>c(HA)>c(H+)
难度: 简单查看答案及解析
-
AgCl和Ag2CrO4的溶度积分别为1.8×10-10 mol2·L-2和2.0×10-12 mol3·L-3,若用难溶盐在溶液中的浓度来表示其溶解度,则下面的叙述中正确的是
A.AgCl和Ag2CrO4的溶解度相等
B.AgCl的溶解度大于Ag2CrO4的溶解度
C.两者类型不同,不能由Ksp的大小直接判断溶解能力的大小
D.都是难溶盐,溶解度无意义
难度: 简单查看答案及解析
-
下列说法正确的是
A.在一定温度下AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数
B.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液
C.AgCl的Ksp=1.8×10-10 mol2·L-2,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10 mol2·L-2
D.向饱和AgCl水溶液中加入盐酸,Ksp值变大
难度: 简单查看答案及解析
-
海带中碘元素的分离实验中,在灼烧后的海带灰中加入蒸馏水,煮沸2~3 min,再过滤,得到滤液。煮沸的目的是
A.加快碘元素与水反应的速率 B.使溶液浓缩
C.使空气中的氧气更多地进入溶液 D.加速碘化物的溶解
难度: 简单查看答案及解析
-
除去食盐中混有的少量碘化钠杂质应采用的方法是
A.加入AgNO3溶液后加热蒸干 B.加入适量盐酸后加热蒸干
C.加水溶解后通入适量氯气再加热蒸干D.加水溶解后滴入适量溴水再加热蒸干
难度: 简单查看答案及解析
-
已知在100℃的温度下(本题涉及的溶液其温度均为100℃,水的离子积KW=1.0×10-12 mol2·L-2。下列说法中正确的是
A.0.05 mol·L-1的H2SO4溶液,pH=1
B.0.001 mol·L-1的NaOH溶液,pH=11
C.0.005 mol·L-1的H2SO4溶液与0.01 mol·L-1的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸性
D.完全中和pH=3的H2SO4溶液50 mL,需要pH=11的NaOH溶液50 mL
难度: 简单查看答案及解析