-
(2011年浙江义乌,35题)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,这引起了同学们的兴趣。难道生成的硫酸铜粉末受热后还能分解?那分解的产物是什么呢?
通过查阅资料,同学们了解到:
1、硫酸铜受热分解生成氧化铜和气体。气体是由SO2、SO3、O2中的一种或几种。受热时
温度不同,生成的气体成分也不同。
2、SO2、SO3都能被碱石灰吸收。
3、SO2、SO3都能被氢氧化钠溶液吸收。
【提出猜想】根据质量守恒定律猜测气体的成分:
I. 只含▲ 一种; II.含有SO2、O2二种; III.含有SO2、SO3、O2三种。
【设计实验】利用下图装置加热硫酸铜粉末直至完全分解
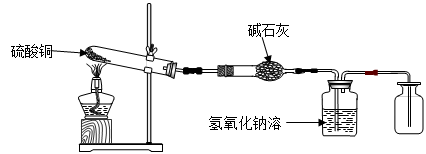
A B C D
【获取事实】
(1)用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有▲ 。
(2)已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
装置
A(试管+粉末)
B
C
反应前
42.0克
75.0克
140.0克
反应后
37.0克
79.5克
140.0克
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个 ?▲
A.3CuSO4△3CuO+SO3↑+2SO2↑+O2 ↑ B. 4CuSO4△4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4△5CuO+SO3↑+4SO2↑+2O2 ↑ D. 6CuSO4△6CuO+4SO3↑+2SO2↑+O2↑
九年级化学探究题中等难度题查看答案及解析
-
(2011年浙江杭州,38题)某学校科学兴趣小组想设计一个实验,来模拟研究CO2 :浓度增加是否增大地球“温室效应”。他们查阅了有关数据:
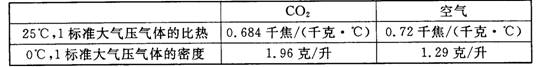
并设计了下面的实验和操作步骤:
Ⅰ、在两只同样的玻璃瓶里分别充满CO2和空气,并编号为甲、乙,塞紧带有同样温度计的橡皮塞。再把两只玻璃瓶放在阳光下照射(如右图),观察甲、乙瓶中的温度变化。

Ⅱ、.阳光持续照射,间隔一定时间测量两玻璃瓶温度值,并记录(见下表)
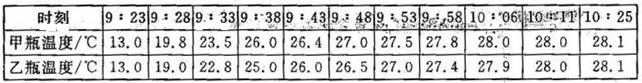
请回答下列问题:
(1)、写出实验室制取CO2的化学方程式________。
(2)、往瓶中充CO2时,验证瓶中已充满了CO2的方法是________。
(3)、该实验中,照射同样时间,根据上表的数据,比较甲、乙瓶温度变化的规律是________
________。
(4)、该实验中,在阳光照射下,影响甲、乙瓶温度不同的原因,除了CO2的温室效应以外,还有的可能原因是(写出一点即可)________
________
(5)有同学认为根据该模拟实验的目的,实验设计存在问题,你认为是(写出一点即可)________
________。
九年级化学探究题中等难度题查看答案及解析
-
(2011年浙江杭州,31题)下图甲是氢气和氧化铜反应的实验,下图乙是木炭和氧化铁反应的实验。
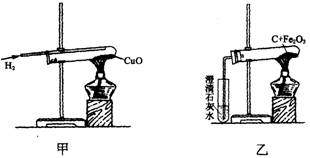
(1)、在上述两个实验中,氢气和木炭表现出相同的化学性质是________性。
(2)、实验步骤的先后次序非常重要,比如甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生爆炸;反应结束后必须先________后________,否则生成的红色的铜会变成黑色。
(3)、某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中 也未产生预期的气泡,这说明该反应并没有生成________
(4)、该同学查阅资料,得到关于铁的氧化物如下信息:

根据以上信息,试写出乙实验试管中反应的化学方程式________
经分析后,该同学试着提高反应温度后,实验出现了预期的现象。
________
九年级化学探究题中等难度题查看答案及解析
-
(2011年浙江杭州, 30题)为了减轻酸雨的危害,我国研发了“海水法烟气脱硫工艺”。其工艺流程大致是:
I、从高处喷淋下的海水(pH=8.1-8.3)洗脱从下而上燃煤烟气中的SO2, (SO2+H2O=H2SO3 H2SO3是弱酸),海水变为弱酸性;
Ⅱ、.将洗过烟气后的海水与氧气充分接触,发生下列反应:
4NaC1+O2十2H2SO3 ==2Na2SO4+4HC1
III.再将与氧气充分接触的海水跟大量天然海水混合等措施,使各项指标接近天然海水后再排放。
(1)、在坐标图中画出“海水法烟气脱硫工艺”全过程中海水的pH依次变化大致趋势。
(2)、工艺流程中天然海水接触烟气后变为弱酸性,这说明在此过程中海水中的 离子和H2SO3电离出的氢离子发生了反应。
(3)、若要测定海水中Na2SO4含量,实验操作步骤是:
取少量被测海水,测定________、加入足量的________溶液(写化学式)、再加入稀硝酸、过滤、洗涤、烘干、称量沉淀质量。
九年级化学探究题中等难度题查看答案及解析
-
(2011年浙江湖州,30题)某同学看到装有薯片的包装袋总是鼓鼓的,里面充有气体,他进行了如下探究:

(1)他提出的问题是________。
(2)其他同学一致认为该实验方案是不合理的,正确的实验方案是:将收集的气体________,观察现象。
九年级化学探究题中等难度题查看答案及解析
-
某化学学习小组的同学围绕“澄清石灰水与碳酸钠溶液的反应”展开了如下探究活动。(1)该反应的化学方程式为________________________________。
(2)反应后溶液中的溶质是什么?同学们一致认为有以下三种情况:
①氢氧化钠和氢氧化钙;②氢氧化钠和碳酸钠;③_______________。
(3)小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况_____(填序号)是不可能的。
为了进一步确定溶液的成分,同学们设计了如下实验方案:
实验步骤
现象
结论
情况①正确
在同学们的合作下,他们顺利完成了探究任务。
九年级化学探究题中等难度题查看答案及解析
-
通过一年的化学学习,相信你已掌握了实验室制取气体的有关知识。请结合图示回答下列问题。
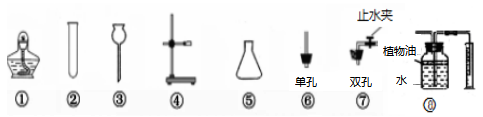
(1)仪器⑤的名称是_________________。
(2)从以上仪器中选择出可制取H2、CO2、O2的发生装置的组合__________________要求:可以随时添加液体药品),实验室制氧气的化学方程式为________________________。
(3)为了测定硫酸钠中碳酸钠的含量,某学习小组将混合物中加入稀硫酸,通过测定产物中的二氧化碳来计算碳酸钠的质量。装置⑧可以用来测量生成的CO2气体的体积(制取的CO2的体积不超过水的体积),植物油上方原有的空气对实验的结果_________(填“有”或“没有”)明显影响。
九年级化学探究题中等难度题查看答案及解析
-
有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究。
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末。打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃。当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
【探究与反思】
打火石是________(填“混合物”或“纯净物”),这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?________,这种蜡烛也可以熄灭,你采用的方法是________。
【实验探究】吹不灭的蜡烛芯内的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
实验
操作步骤
现象
结论
1
切开蜡烛,取出打火石,用砂纸打磨
打火石是银白色
2
该金属一定不是铁
3
取少量打磨后的打火石于试管中,滴加硫酸铜溶液。
有红色物质析出
该金属一定是镁
【分析思考】
(1)请写出“实验3”中可能涉及到的化学方程式。
(2)有同学认为通过“实验3”中现象不能证明烛芯内的金属一定是镁,
因为________ 。
(3)针对以上实验,请你设计一个合理的实验方案来进一步验证这种金属________。
九年级化学探究题中等难度题查看答案及解析
-
通过半年多时间的学习,同学们一定对下图装置很熟悉,请回答有关问题:
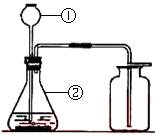
(1)写出标号仪器有名称:①________ ②________;
(2)我们知道有两种气体在实验室可以采用右图装置进行制取,请写出这两个制备反应的化学方程式;。
九年级化学探究题中等难度题查看答案及解析
-
(10分)初中化学课上,同学们利用下列实验探究碱的化学性质:

(1)A实验中反应的化学方程式为________________________________________。
(2)C实验中观察到的现象是____________________________________________。
(3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】 废液中含有什么物质?
【假设猜想】 通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有___________。
老师问:废液中还可能有什么物质?引发了同学们热烈讨论,下面是大家的发言:
学生甲
可能有Ca(OH)2、NaOH
学生丙
可能有Ca(OH)2、CaCl2
学生乙
可能有NaOH、Na2CO3
学生丁
可能有Na2CO3
学生戊
可能有NaOH
……
…………
【实验验证】 同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钡溶液,得到白色沉淀,红色褪去。
【结论】上述滤液中,还含有________,没有______________________。
九年级化学探究题中等难度题查看答案及解析