-
请按题目要求回答:
(1)在CuCl2和FeCl2的混合溶液中加入一定质量的Mg粉,充分反应后过滤,得到滤渣和滤液。向滤渣中滴加稀HCl,有气泡产生,则滤渣中一定含有的物质是_________________(填化学式)。
(2)某钢铁厂每天需消耗4900 t含Fe2O376%的赤铁矿石,该厂理论上可每天生产含Fe98%的生铁的质量是多少?(写出计算过程)____
九年级化学计算题中等难度题查看答案及解析
-
用500t含氧化铁质量分数为70%的赤铁矿,可以炼出含杂质4%的生铁多少吨?
九年级化学计算题中等难度题查看答案及解析
-
20℃时,NaCl的溶解度为36.0g,现有该温度下200g 5%的NaCl溶液,求下列变化后溶液中NaCl的质量分数。
(1)加10gNaCl完全溶【解析】
_______;(2)加20g水:_______;
(3)蒸发20g水:_______。(计算结果精确到0.1%)
九年级化学计算题中等难度题查看答案及解析
-
兴趣小组的同学在社会实践基地发现一袋商标模糊的硝酸铵化肥。同学们要帮助基地的工作人员测定化肥中硝酸铵的含量,请你参与他们的探究活动。
(查阅资料)①铵态氮肥易溶于水。②铵态氮肥与碱反应产生氨气。③氨气易溶于水,溶液呈碱性。
(实验过程)小丽同学准确称取9.0 g硝酸铵化肥样品,与过量的氢氧化钙粉末混合,充分反应后,产生的氨气用足量的稀硫酸全部吸收,测得2分钟内稀硫酸溶液质量的变化,记录如下表所示(样品中的杂质不含氮元素,也不与氢氧化钙反应)。
时间/s
0
20
40
60
80
100
120
溶液增加的质量/g
0
0.7
1.2
1.5
1.6
1.7
1.7
(数据处理)
计算此化肥中硝酸铵的质量分数_____(写出计算过程)。
(反思交流)
化肥对粮食增产有着重要的作用,如何科学合理使用或贮存铵态氮肥,请你给工作人员提一条合理化建议_____。
九年级化学计算题中等难度题查看答案及解析
-
某生产化肥碳酸氢铵(NH4HCO3)的企业,做了一个大型户外广告。如图所示,根据相关信息计算:(该化肥中的其他成分不含氮元素)
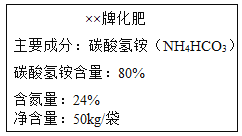
(1)碳酸氢铵(NH4HCO3)中氮元素的化合价为________________价。(已知碳为+4价)
(2)碳酸氢铵(NH4HCO3)的相对分子质量为_________________。
(3)碳酸氢铵(NH4HCO3)中氮、氢、氧、碳的原子个数比为_________________。
(4)碳酸氢铵(NH4HCO3)中氮、氢、氧、碳元素质量比为_________________。
(5)碳酸氢铵(NH4HCO3)中氮元素的质量分数为______。(结果精确到0.1%)
(6)计算该化肥含氮量,用数据说明其_______(是、否)为虚假广告。
九年级化学计算题中等难度题查看答案及解析
-
科学研究表明:绿原酸具有抗菌、抗病毒、增高白血球、保肝利胆、抗肿瘤、降血脂、清除自由基和兴奋中枢神经系统等作用,被誉为“第七营养素”, 它可以从忍冬科植物中提取,化学式为C16H18O9。请问:
(1)绿原酸由_____种元素组成。
(2)一个绿原酸分子由_____个原子构成。
(3)绿原酸中H、O元素的质量比是_____。
九年级化学计算题中等难度题查看答案及解析
-
某化学小组测量氢化钙(CaH2)样品中氢化钙的质量分数。取5g样品于锥形瓶中,加入100g水充分反应,称得锥形瓶内剩余物质的质量与反应时间的关系如图所示。假设杂质分布均匀且与水不发生反应,反应方程式为
,请回答:

(1)反应生成的氢气质量为_______________;
(2)样品中氢化钙的质量分数为________。(写出计算过程)
九年级化学计算题中等难度题查看答案及解析
-
为了测定实验室中KClO3样品的纯度,某学习小组取2.5g该样品与0.5gMnO2混合,加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体的质量,重复以上操作,依次称得加热t1、t2、t3、t4时间后剩余固体的质量,记录数据如下表所示。
加热时间
t1
t2
t3
t4
剩余固体质量/g
2.48
2.34
2.04
2.04
请仔细分析实验数据,回答下列问题:
(1)在_____________时间后,该样品中的KClO3已经完全反应。
(2)完全反应后产生O2的质量是_______________。
(3)该样品中KClO3的质量是______。
九年级化学计算题中等难度题查看答案及解析
-
实验室用34gH2O2溶液和1g的MnO2混合制取O2,生成O2的质量与反应时间的关系如下图所示。
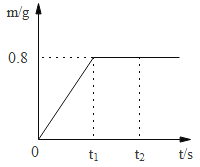
(1)在__________s时,H2O2恰好完全反应;
(2)原溶液中H2O2的质量为______克。
九年级化学计算题中等难度题查看答案及解析
-
为检测市场销售的小苏打(主要成分是碳酸氢钠)的含量,取 5.0g 样品加热到质量不再减少为止,收集到干燥的气体 0.88g。(碳酸氢钠受热分解的化学方程式为:2NaHCO3=Na2CO3+H2O+CO2↑,杂质不参加反应)。求该样品中碳酸氢钠的质量分数。_____
九年级化学计算题中等难度题查看答案及解析