-
室温下,下列事实不能说明NH3·H2O为弱电解质的是( )
A. 0.1 mol·L-1NH3·H2O的pH小于13
B. 0.1 mol·L-1NH4Cl溶液的
pH小于7
C. 相同条件下,浓度均为0.1 mol·L-1NaOH溶液和氨水,氨水的导电能力弱
D. 0.1 mol·L-1NH3·H2O能使无色酚酞溶液变红色
难度: 简单查看答案及解析
-
25 ℃时,在含CH3COOH和CH3COO-的溶液中,CH3COOH、CH3COO-二者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示。下列说法不正确的是( )

A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3C
OOH)
B. 在pH=7的溶液中,α(CH3COOH)=0,α(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,α(CH3COOH)与α(CH3COO-)之和保持不变
难度: 中等查看答案及解析
-
下列物质的水溶液因水解而呈酸性的是( )
A. NaOH B. (NH4)2SO4 C. Na2CO3 D. NaCl
难度: 简单查看答案及解析
-
为证明醋酸是弱电解质,下列方法不正确的是( )
A. 测定0.1 mol·L-1醋酸溶液的pH
B. 测定0.1 mol·L-1CH3CO
ONa溶液的酸碱性
C. 比
较浓度均为0.1 mol·L-1盐酸和醋酸溶液的导电能力
D. 比较相同物质的量浓度的NaOH溶液和醋酸溶液恰好反应完全时消耗两溶液的体积
难度: 简单查看答案及解析
-
常温下,用浓度为0.100 mol·L-1的NaOH溶液分别逐滴加入到20.00 mL 0.100 0 mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确的是( )

A. V(NaOH)=10.00 mL时,两份溶液中c(X-)>c(Y-)
B. V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
C. V(NaOH)=20.00 mL时,c(OH-)>c(H+)>c(Na+)>c(X-)
D. pH=7时,两份溶液中c(X-)=c(Na+)=c(Y-)
难度: 困难查看答案及解析
-
下列物质的水溶液呈碱性的是( )
A. CH3COOH B. FeCl3 C. Na2SiO3 D. NaCl
难度: 简单查看答案及解析
-
为证明NH3·H2O是弱电解质。在常温下,下列实验方法不正确的是( )
A. 比较浓度相同的氨水与NaOH溶液的导电能力,可证明NH3·H2O为弱电解质
B. 测定NH4Cl溶液的pH小于7,可证明NH3·H2O为弱电解质
C. 测定0.01 mol·L-1的氨水的pH小于12,可证明NH3·H2O为弱电解质
D. 测定0.01 mol·L-1的NH4HSO4溶液的pH小于7,可证明NH3·H2O为弱电解质
难度: 中等查看答案及解析
-
一定温度下,等体积、pH相等的盐
酸和醋酸溶液,下列说法正确的是( )
A. 两溶液中,所含溶质的分子数:盐酸等于醋酸
B. 与等体积等浓度NaHCO3混合,开始产生CO2速率相等,后来盐酸快
C. 等体积的盐酸和醋酸溶液分别与足量的Zn完全反应,盐酸产生的H2多
D. 用同浓度的NaOH溶液分别与两溶液恰好反应完全,根据消耗的NaOH溶液体积的多少可以判断醋酸是弱电解质
难度: 中等查看答案及解析
-
已知NaHSO4在水中的电离方程式为NaHSO4===Na++H++SO
,某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2,对于该溶液,下列叙述中不正确的是( )
A. 该温度高于25 ℃
B. 水电离出的c(H+)=1×10-10 mol·L-1
C. c(H+)=c(OH-)+c(SO
)
D. 该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好呈中性
难度: 简单查看答案及解析
-
室温下,有关下列四种溶液的叙述正确的
是(忽略溶液混合时体积变化)
①
②
③
④
pH
12
12
2
2
溶液
氨水
氢氧化钠溶液
醋酸
盐酸
A. 在①②中分别加入氯化铵晶体,两溶液的pH值均增大
B. 分别将等体积的①和②加水稀释100倍,所得溶液的pH:①>②
C. 把①④两溶液等体积混合后所得溶液显酸性
D. 将溶液②和溶液③等体积混合,混合后所得溶液pH=7
难度: 简单查看答案及解析
-
25 ℃时,向20.00 mL浓度均为0.100 0 mol·L-l的三种酸HX、HY、HZ中分别逐滴加入0.100 0 mol·L-l的NaOH溶液,所得溶液的pH随加入NaOH溶液的体积关系如图所示。
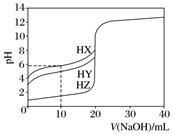
下列说法正确的是( )
A. V(NaOH)=0 mL时,三份溶液相比较c(X-)>c(Y-)>c(Z-)
B. 当三份溶液pH均等于7时,反应消耗的n(HX)=n(HY)=n(HZ)
C. 当V(NaOH)=10 mL时,反应后溶液中各离子浓度由大到小的顺序为c(X-)>c(Y-)>c(Z-)>c(Na+),且在HZ溶液中:c(Z-)>c(H+)>c(Na+)>c(OH-)
D. HY与HZ混合溶液中:c(H+)=c(Y-)+c(Z-)+
难度: 困难查看答案及解析
-
常温下,将体积为V1 的 0.100 0 mol·L-1 HCl溶液逐滴加入到体积为V2的0.100 0 mol·L-1Na2CO3 溶液中,溶液中H2CO3、HCO
、CO
所占的物质的量分数(α)随pH的变化曲线如图。下列说法不正确的是( )

A. 在pH=10.3时,溶液中:c(Na+)+c(H+)=c(HCO
)+2c(CO
)+c(OH-)+c(Cl-)
B. 在pH=8.3时,溶液中:0.100 0>c(HCO
)+c(CO
)+c(H2CO3)
C. 在pH=6.3时,溶液中,c(Na+)>c(Cl-)>c(HCO
)>c(H+)>c(OH-)
D. V1∶V2=1∶2时,c(OH-)>c(HCO
)>c(CO
)>c(H+)
难度: 中等查看答案及解析
-
下列物质的水溶液因水解而呈酸性的是( )
A. HCl B. NH4Cl C. CH3COONa D. NaHCO3
难度: 简单查看答案及解析
-
中和相同体积、相同pH值的H2SO4、HCl和CH3COOH三种稀溶液,所需相同浓度的NaOH溶液的体积为V1、V2和V3,则( )
A. V1>V2>V3 B. V3>V2>V1 C. V3>V1=V2 D. V1>V2=V3
难度: 中等查看答案及解析
-
某温度下,关于①0.01 mol·L-1 醋酸溶液,②pH=2的醋酸溶液,下列说法正确的是( )
A. c(CH3COOH):① > ②
B. c(CH3COO-):① > ②
C. c(CH3COOH)+c(CH3COO-):①=②
D. c(C
H3COO-) +c(OH-):① < ②
难度: 中等查看答案及解析
-
常温下,向25 mL 0.1 mol·L-1弱碱MOH溶液中逐滴滴加0.2 mol·L-1的HCl,溶液pH的变化曲线如图所示(溶液混合时体积的变化忽略不计)。下列说法正确的是( )
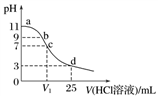
A. MOH电离方程式为MOH===M++OH-
B. 在b点,离子浓度大小为c(OH-)>c(H+)>c(M+)>c(Cl-)
C. 在c点,滴加的V(HCl)>12.5 mL
D. 在d点,c(Cl-)=2c(MOH)+2c(M+)=0.1 mol·L-1
难度: 困难查看答案及解析
-
下列溶液中离子浓度关系的表示正确的是( )
A. 在0.1 mol·L-1 KHC2O4溶液中:c(K+)+c(H+)=c(HC2O
)+c(OH-)+c(C2O
)
B. 0.1 mol·L-1的Na2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
C. 0.1 mol·L-1的NH4NO3溶液中:c(NO
)>c(H+)>c(NH
)>c(OH-)
D. 物质的量浓度相等的HCOOH和HCOONa溶液等体积混合后的溶液中:2c(Na+)=c(HCOO-)+c(HCOOH)
难度: 中等查看答案及解析
-
室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )
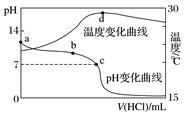
A. a点由水电离出的c(H+)=1.0×10-14 mol·L-1
B. b点:c(NH
)+c(NH3·H2O)=c(Cl-)
C. c点:c(Cl-)=c(NH
)
D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
难度: 简单查看答案及解析