-
下列仪器中,没有“0”刻度的是:
A.量筒 B.温度计 C.酸式滴定管 D.托盘天平游码刻度尺
难度: 简单查看答案及解析
-
下列反应必须用稀硫酸,而不能用浓硫酸的是:
A.用纤维素制硝化纤维 B.跟苯、浓硝酸作用制硝基苯
C.溶解金属铜 D.锌与酸制氢气
难度: 简单查看答案及解析
-
下列操作属于萃取的是:
A.向溴的煤油溶液里加入苯后振荡 B.向溴水里加入酒精后振荡
C.向硫的二硫化碳溶液里加水后振荡 D.向碘水里加入四氯化碳后振荡
难度: 简单查看答案及解析
-
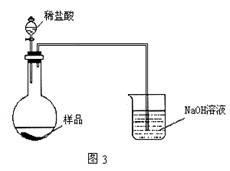
实验室制取气体时,吸收尾气的方案,正确的是:
①向KMnO4晶体中加入浓盐酸,产生的气体进行漂白实验后的尾气用NaOH溶液吸收;②向Na2SO3晶体中滴入浓H2SO4,尾气用氨水吸收;③向FeS固体中滴入稀盐酸,最后的尾气用CuSO4溶液吸收;④浓H2SO4与食盐晶体共热,将多余的气体用水吸收;
A.①④ B.②③ C.①③④ D.①②③④
难度: 简单查看答案及解析
-
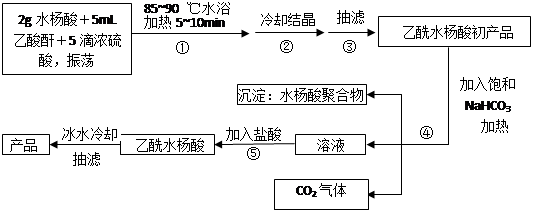
实验室进行下列实验:①苯与浓HNO3在浓H2SO2作用下制硝基苯;②酚醛树脂的制备;③葡萄糖溶液的银镜反应;④乙酸与乙醇在浓硫酸作用下制乙酸乙酯。其中需用水浴加热的有:
A.①②③④ B.①②③ C.②③④ D.①③④
难度: 简单查看答案及解析
-
下列关于层析实验的说法正确的是:
A.点样后应在滤纸上形成一个直径较大的样斑,便于实验时观察
B.展开剂可以既是流动相又是固定相
C.为使层析实验有较好的分离效果,试样溶液浓度应较小
D.纸层析法简称纸层析,是色谱分析法的一种
难度: 简单查看答案及解析
-
关于下列实验,说法正确的是:
A.将一块铝片投入足量NaOH溶液中,充分反应后铝片消失,将溶液蒸干便可得到纯净NaAlO2
B.将二块相同铝片投入到等物质的量浓度的CuSO4和CuCl2溶液中,反应速率几乎相同
C.将铝粉投入浓NaOH溶液中,1mol铝可还原3mol水
D.将一小块钠投入盛有乙醇的烧杯中,由于钠的密度大于乙醇,所以钠一直在液面下反应
难度: 简单查看答案及解析
-
在实验室进行下列实验, 括号内的实验用品都能用到的是
A. 硫酸铜晶体里结晶水含量的测定(坩埚、温度计、硫酸铜晶体)
B. 蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液)
C. 钠的焰色反应(铂丝、氯化钠溶液、稀盐酸)
D. 肥皂的制取(蒸发皿、玻璃棒、甘油)
难度: 简单查看答案及解析
-
某无色溶液中滴入酚酞试液显红色,该溶液中可以大量共存的离子组是
A.Mg2+、Al3+、HCO3-、SO32- B.K+、Ca2+、MnO4-、Cl-
C.Ba2+、Na+、AlO2-、NO3- D.NH4+、Fe3+、SO42-、SCN-
难度: 简单查看答案及解析
-
下列说法正确的是:
A.化合态的氟没有毒,含氟牙膏中的氟含量越多越好
B.火柴头中含有的氯元素为氯化钾
C.可用高锰酸钾来检测新装修居室内甲醛的浓度
D.火柴燃烧生成的气体不能使品红溶液褪色
难度: 简单查看答案及解析
-
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是:
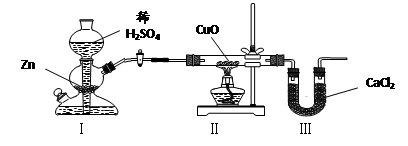
A.Ⅰ、Ⅱ装置之间缺少干燥装置 B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝 D.CuO没有全部被还原
难度: 简单查看答案及解析
-
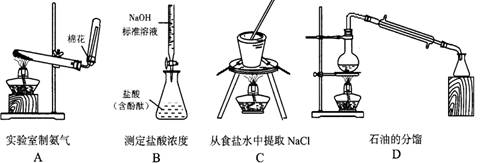
用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是:
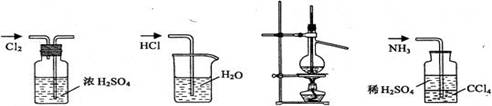
A.干燥Cl2 B.吸收HCl C.石油的蒸馏 D.吸收NH3
难度: 简单查看答案及解析
-
下列物质分离过程中涉及共价键断裂的是:
A.用渗析法除去淀粉胶体中的少量NaCl B.用CCl4萃取碘水中的碘
C.用饱和食盐水洗去Cl2中的少量HCl D.用升华法除去NaCl中混有的少量碘
难度: 简单查看答案及解析
-
下列结论均出自《实验化学》中的实验,其中错误的是:
A.往新配制的可溶性淀粉溶液中滴加碘水,溶液显蓝色,用CCl4不能从中萃取出碘。
B.硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出。
C.制备硫酸亚铁铵晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液表面出现晶膜为止,不能将溶液全部蒸干。
D.重结晶时,溶液冷却速度越慢得到的晶体颗粒越小。
难度: 简单查看答案及解析
-
实验室里不宜长期放置,应在使用时才配制的试剂是:
①酚酞试液 ②银氨溶液 ③Na2CO3溶液 ④Cu(OH)2悬浊液
⑤酸性FeCl3溶液 ⑥FeSO4溶液 ⑦NaCl溶液 ⑧氯水
A.②⑤⑥⑧ B.①③④⑤ C.①②⑤⑦ D.②④⑥⑧
难度: 简单查看答案及解析
-
用苯酚做下列实验,能成功的是
A.与浓硫酸和浓硝酸混合液发生硝化反应
B.与乙醇发生酯化反应
C.在80℃的水中形成乳浊液
D.与福尔马林在沸水浴中便可发生缩聚反应制酚醛树脂
难度: 简单查看答案及解析
-
下列实验装置设计正确,且能达到目的的是:
难度: 简单查看答案及解析
-
向NaBr、NaI、Na2SO3混合液中,通入—定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是:
A.NaCl NaBr B.NaCl NaBr Na2SO4 C.NaCl D. Na2SO4
难度: 简单查看答案及解析
-
能证明苯酚具有弱酸性的方法是:
A.苯酚溶液加热变澄清 B.苯酚浊液中加NaOH后,溶液变澄清。
C.苯酚可与FeCl3反应 D.在苯酚溶液中加入浓溴水产生白色沉淀
难度: 简单查看答案及解析
-
下列物质显示酸性,且能发生酯化反应和消去反应的是:
A.
B.CH3CH2=CHCOOH
C. CH3CH2
COOH D. CH3CH2
COOH
难度: 简单查看答案及解析
-
某无色混合气体可能含有Cl2、O2、HCl、NH3、NO、NO2中的两种或多种,现将此混合气体经过浓硫酸后体积减小,将剩余气体排入空气中,很快变成红棕色。对于原混合气体成分的判断中,正确的是:
A.肯定有O2 B.肯定没有Cl2、NH3、NO2
C.肯定有NH3、NO、HCl D.肯定只有NH3和NO
难度: 简单查看答案及解析
-
化学教科书中有大量的数据,下列为某同学对数据的利用情况,其中不正确的是:
A.用溶解度数据判断长时间煮沸Mg(HCO3)2溶液得到的产物是Mg(OH)2而不是MgCO3
B.用沸点数据推测一些液体混合物用分馏的方法分离开来的可能性
C.用反应热数据的大小判断不同反应的反应速率的快慢
D.用原子(或离子)半径数据推测某些原子(或离子)氧化性或还原性的强弱
难度: 简单查看答案及解析
-
下列反应的离子反应方程式书写正确的是:
A.向碘化钾溶液中加入用硫酸酸化的过氧化氢溶液: 2I-+H2O2=I2+2OH-
B.向碳酸氢铵溶液中加入过量的稀氢氧化钠溶液:NH4++ HCO3-+2OH-= NH3·H2O + CO32-+H2O
C.向Ba(OH)2溶液中加入过量NH4HSO4:Ba2++H++NH4++2OH-+SO 42-=BaSO4↓+H2O+NH3·H2O
D.Fe2O3溶于过量的氢碘酸中:Fe2O3 +6H+ = 2Fe3+ + 3H2O
难度: 简单查看答案及解析
-
将铝粉和某铁的氧化物FeO·2Fe2O3粉末配制成铝热剂,分成两等分。一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为15.68L,另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为:
A. 11.20L B.15.68L C.22.40L D.31.36L
难度: 简单查看答案及解析