-
次氯酸的分子式是
A.HClO4 B.HClO3 C.HClO D.HCl
难度: 简单查看答案及解析
-
下列化学式所表示的物质属于酸性氧化物的是
A.CO B.SiO2 C.Na2O D.H2O2
难度: 中等查看答案及解析
-
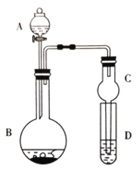
配制100mL0.1mol·L−1的Na2CO3溶液,下列仪器不需要用到的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列物质中不能与稀硫酸反应的是
A.Al B.CH4 C.FeO D.NaHSO3
难度: 中等查看答案及解析
-
2015年中国药学家屠呦呦获得诺贝尔医学奖,以表彰她在青蒿素研究方面做出的突出贡献。提取青蒿素通常可以用乙醚浸取,这与下列哪种方法的原理相同
A.蒸馏法 B.过滤法 C.结晶法 D.萃取法
难度: 中等查看答案及解析
-
反应2Na2O2+2CO2=2Na2CO3+O2中,氧化产物是
A.Na2O2 B.CO2 C.Na2CO3 D.O2
难度: 中等查看答案及解析
-
下列物质溶于水后,仅以分子形式存在的是
A.HCHO B.CH3COOH C.CH3COONa D.MgSO4
难度: 中等查看答案及解析
-
下列表示正确的是
A.硫离子的结构示意图:
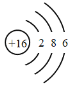 B.乙酸的结构式:
B.乙酸的结构式:C.H2O的球棍模型:
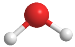 D.CCl4的电子式:
D.CCl4的电子式:难度: 中等查看答案及解析
-
下列说法不正确的是
A.O2和O3互为同位素 B.
和
为同一物质
C.CH4和C3H8互为同系物 D.CH3CH2OH和CH3OCH3互为同分异构体
难度: 中等查看答案及解析
-
下列有关物质性质或用途的说法不正确的是
A.常温下浓硫酸可贮存在铁罐中
B.ClO2具有氧化性,可用于自来水的杀菌消毒
C.燃着的镁条放入盛满二氧化碳的集气瓶中可继续燃烧
D.铁比铜金属性强,所以可用FeCl3腐蚀Cu刻制印刷电路板
难度: 中等查看答案及解析
-
如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R是其中的五种元素。下列说法不正确的是

A.离子半径:Y>X
B.33号砷元素与Q同族
C.最高价氧化物的水化物的酸性:R>W
D.单质与水(或酸)反应的剧烈程度:Y>Z
难度: 中等查看答案及解析
-
下列方程式不正确的是
A.工业制造漂白粉的化学方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
B.制备硝基苯的化学方程式:
+HO-NO2

+H2O
C.将少量碳酸氢铵溶液滴入NaOH溶液反应的离子方程式:NH4++HCO3-+2OH-=NH3↑+CO32−+2H2O
D.CuCl2的水解方程式:Cu2++2H2O
Cu(OH)2↓+2H+
难度: 中等查看答案及解析
-
下列说法不正确的是
A.含有少量氯化钠的硝酸钾粉末,可采用冷却热饱和溶液的结晶法进行提纯
B.实验室中少量金属钠常保存在煤油中,实验时多余的钠不能放回原试剂瓶中
C.铁丝能代替铂丝做焰色反应实验
D.苯不能用带橡胶塞的试剂瓶贮存
难度: 中等查看答案及解析
-
下列说法正确的是
A.石油的分馏和煤的液化都是发生了物理变化
B.相同质量的乙炔、苯分别在足量氧气中燃烧,苯比乙炔消耗的氧气质量多
C.乙醇在灼热铜丝存在下与氧气反应时发生氧化反应
D.乙烯、乙炔、苯都能与Br2发生反应,反应原理相同,都发生加成反应
难度: 中等查看答案及解析
-
下列说法正确的是
A.花生油的主要成分是高级脂肪酸甘油酯,属于高分子化合物
B.汽油和食用油都可以在碱性条件下水解
C.脱脂棉、滤纸的主要成分均为纤维素,完全水解能得到葡萄糖
D.钠与乙醇反应时钠浮在液面上,反应比钠与水反应更剧烈
难度: 中等查看答案及解析
-
元素铬(Cr)的几种化合物存在下列转化关系,下列判断不正确的是
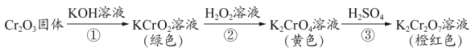
A.反应①表明Cr2O3有酸性氧化物的性质
B.反应②利用了H2O2的氧化性
C.反应②的离子方程式为2CrO2ˉ+3H2O2+2OHˉ=2CrO42ˉ+4H2O
D.反应①②③中铬元素的化合价均发生了变化
难度: 中等查看答案及解析
-
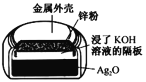
锌—空气电池(原理如图)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时,下列说法正确的是
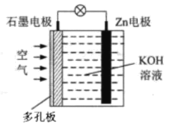
A.Zn电极是该电池的正极
B.Zn电极的电极反应:Zn+H2O-2e‾=ZnO+2H+
C.OH‾向石墨电极移动
D.标准状况下,当消耗11.2LO2时,电路中流过2mol电子
难度: 中等查看答案及解析
-
下列说法不正确的是
A.常温下,pH<7的溶液一定是酸溶液
B.常温下,浓度均为0.1mol·L-1的盐酸和醋酸溶液,盐酸的导电能力强
C.中和相同体积、相同浓度的氨水和NaOH溶液,所需HCl的物质的量相同
D.向NaOH溶液中滴加醋酸至c(CH3COO‾)=c(Na+),则溶液呈中性
难度: 中等查看答案及解析
-
下列说法正确的是
A.金刚石和足球烯是同素异形体,熔化时都只克服共价键
B.H2O汽化成水蒸气、分解为H2和O2,都需要破坏共价键
C.CCl4和CO2两种分子中,每个原子的最外电子层都具有8电子稳定结构
D.NaHSO4晶体溶于水时,离子键被破坏,共价键不受影响
难度: 中等查看答案及解析
-
已知断裂1molH2(g)中的H-H键需要吸收436kJ能量,断裂1molI2(g)中的I-I键需要吸收151kJ能量,生成HI(g)中的1molH-I键能放出299kJ能量。下列说法正确的是
A.1molH2(g)和1molI2(g)的总能量为587kJ
B.H2(g)+I2(s)
2HI(g)ΔH=-11kJ·molˉ1
C.HI(g)
H2(g)+
I2(g)ΔH=+5.5kJ·molˉ1
D.H-H键比I-I键更容易断裂
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,2.24L的乙醇中含有氢原子的数目为0.6NA
B.1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
C.1L0.1mol·Lˉ1Na2CO3溶液中含有的CO32ˉ数目等于0.1NA
D.25℃时,1LpH=13Ba(OH)2溶液中含有OH-的数目为0.2NA
难度: 中等查看答案及解析
-
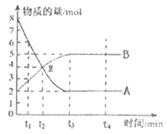
某研究欲利用甲烷消除NO2污染,CH4(g)+2NO2(g)
N2(g)+CO2(g)+2H2O(g)。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见表。
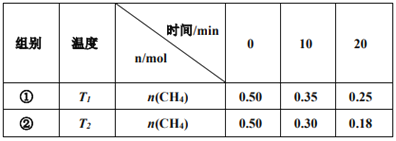
下列说法正确的是
A.①组中,0~20min内,用NO2表示的反应速率为0.0125mol·Lˉ1·minˉ1
B.由实验数据可知实验控制的温度T1<T2
C.容器内混合气体的密度不变,说明反应已达到平衡状态
D.若增大压强,则正反应速率加快,逆反应速率减慢
难度: 中等查看答案及解析
-
根据下列实验操作和现象所得出的结论正确的是
选项
实验操作和现象
结论
A
向NaCl粉末中加入适量酒精,充分振荡形成无色透明液体。用激光笔照射,出现一条光亮通路
形成的分散系是胶体
B
水蒸气通过灼热的焦炭后,将混合气体通过灼热的氧化铜,所得气体能使无水硫酸铜变蓝色
高温下,C与水蒸气反应生成H2
C
取4mL淀粉溶液,加入5mL稀硫酸,加热5min后,再加入少量新制的Cu(OH)2,加热至沸腾,没有出现砖红色沉淀。
淀粉未水解
D
向某无色溶液中加入盐酸溶液,产生无色无味气体
溶液中一定有CO32ˉ
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
某海水浓缩液中含有大量的Clˉ、Brˉ、Iˉ,取1L该浓缩液,向其中通入一定量的Cl2,溶液中三种离子的物质的量与通入Cl2的体积(标准状况)的关系如下表。下列有关说法中不正确的是
Cl2的体积(标准状况)
2.8L
5.6L
11.2L
n(Clˉ)
1.25mol
1.5mol
2mol
n(Brˉ)
1.5mol
1.4mol
0.9mol
n(Iˉ)
amol
0
0
A.当通入Cl2的体积为2.8L时,只有Iˉ与Cl2发生反应
B.当通入Cl2的体积为2.8L~5.6L时,只有Brˉ与Cl2发生反应
C.a=0.15
D.原溶液中c(Clˉ)∶c(Brˉ)∶c(Iˉ)=10∶15∶4
难度: 中等查看答案及解析
-
某固体混合物中可能含有:SiO2、Na2O、CaO、CuO、Fe2O3。现将该固体进行如下实验(所加试剂均过量):
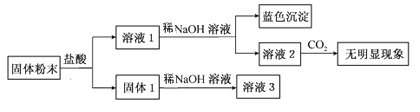
下列说法正确的是( )
A.该混合物一定含有CuO、SiO2,可能含有Na2O
B.该混合物可能含有Fe2O3
C.该混合物一定不含CaO和Na2O
D.无法确定是否含有CaO和Fe2O3
难度: 中等查看答案及解析