-
下列化学试剂常作家庭消毒用品,下列说法正确的是
A.乙醇室内消毒适宜雾喷,能够扩大消毒空间 B.“84”消毒液与乙醇混合使用能提高消毒效率
C.室内熏蒸过氧乙酸、双氧水可加快消毒速率 D.75%的乙醇溶液消毒效果好于95%的乙醇溶液
难度: 简单查看答案及解析
-
白矾
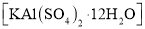 又称明矾、钾铝矾、钾明矾,《本草图经》有“敷脓疮收水”“净水”之功效的记载。下列说法正确的是
又称明矾、钾铝矾、钾明矾,《本草图经》有“敷脓疮收水”“净水”之功效的记载。下列说法正确的是A.
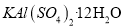 属于混合物
属于混合物B.白矾能够“净水”是因为白矾具有杀菌消毒之功效
C.通过焰色反应可以检验出白矾中含有钾元素
D.一定量白矾溶液中滴加
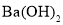 溶液至过量,沉淀质量先增大后减小最后保持不变
溶液至过量,沉淀质量先增大后减小最后保持不变难度: 中等查看答案及解析
-
乙烯在一定条件下可以发生反应:
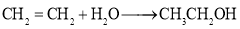 ,下列说法正确的是
,下列说法正确的是A.中子数为8的氧原子
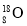 B.羟基的电子式:
B.羟基的电子式:
C.乙烯分子中所有原子一定共平面 D.乙烯的球棍模型

难度: 简单查看答案及解析
-
设
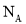 为阿伏加德罗常数的值,下列说法一定正确的是
为阿伏加德罗常数的值,下列说法一定正确的是A.
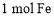 在
在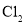 中燃烧,转移电子数为
中燃烧,转移电子数为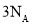
B.标准状况下,
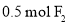 与
与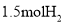 充分反应后,得到22.4L气体
充分反应后,得到22.4L气体C.
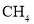 、
、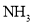 两种气体所含电子数和质子数均为
两种气体所含电子数和质子数均为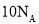
D.
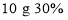 的福尔马林溶液中含有的氧原子个数为
的福尔马林溶液中含有的氧原子个数为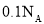
难度: 中等查看答案及解析
-
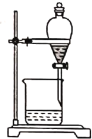
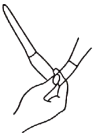
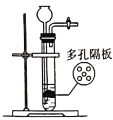
下列图示的实验操作,能够达到实验目的的是
A
B
C
D
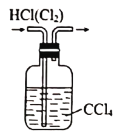
除去
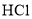 中混有的气体杂质
中混有的气体杂质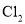
苯萃取溴水中的溴,放出溴的苯溶液
排除装有
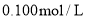 盐酸的滴定管中的气泡
盐酸的滴定管中的气泡二氧化锰催化双氧水分解制备
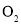 ,可随时控制反应进行
,可随时控制反应进行A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列离子方程式的书写正确的是
A.
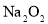 用作供氧剂,遇水反应:
用作供氧剂,遇水反应: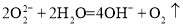
B.
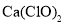 溶液吸收有毒的
溶液吸收有毒的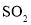 气体:
气体: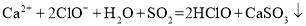
C.工业上常用
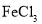 溶液刻蚀铜电路板:
溶液刻蚀铜电路板: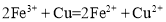
D.纯碱溶液中滴加少量的盐酸:
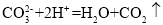
难度: 中等查看答案及解析
-
某碘盐(含
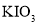 )溶解于水,滴加KOH溶液使之显碱性,若通入氯气可以生成
)溶解于水,滴加KOH溶液使之显碱性,若通入氯气可以生成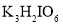 ,关于该反应的说法错误的是
,关于该反应的说法错误的是A.碘盐中碘元素被氧化 B.
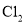 的氧化性强于
的氧化性强于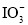
C.氧化剂与还原剂的物质的量之比为1:2 D.转移
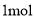 电子时,有
电子时,有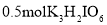 生成
生成难度: 中等查看答案及解析
-
下列实验操作、现象及解释或结论均正确的是
选项
操作
现象
解释或结论
A
稀硫酸滴加到纯碱中,产生的气体通入
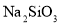 溶液中
溶液中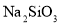 溶液中出现白色沉淀
溶液中出现白色沉淀非金属性:
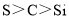
B
某钠盐晶体完全溶解于稀盐酸,所得澄清溶液中滴加
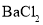 试剂
试剂澄清溶液中出现白色沉淀
该盐为
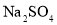
C
溴的苯溶液滴加到铁粉中,产生的气体通入硝酸酸化的
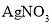 溶液中
溶液中产生浅黄色沉淀
溴与苯发生取代反应生成HBr
D
蔗糖中滴加稀硫酸,加热一段时间后,滴加银氨溶液,再加热
未出现银镜现象
蔗糖没有发生水解生成葡萄糖
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
W、X、Y、Z四种短周期元素的原子序数依次增大,W可以与第二周期的四种不同元素结合形成四种不同的10电子的分子,X、Y可形成阴、阳离子个数之比为1:2的两种化合物,其中一种具有强氧化性,Z与X同主族,化合物A、B均由W、X、Y、Z四种元素组成。下列说法错误的是
A.原子半径大小顺序为
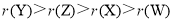
B.W和X、Z均能形成18电子的分子
C.X、Y之间形成的化合物只含离子键
D.A与B之间可以发生反应
难度: 中等查看答案及解析
-
氯喹对新冠肺炎有较好的疗效,制药厂通常将其转化为磷酸氯喹,其结构及其转化如图所示。下列说法错误的是
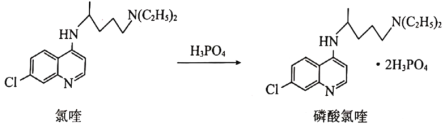
A.氯喹转化为磷酸氯喹可增加其溶解性 B.氯喹分子中苯环上二溴代物多于一溴代物
C.氯喹能够发生还原、加成及取代反应 D.氯喹可使酸性高锰酸钾溶液褪色
难度: 中等查看答案及解析
-
以闪锌矿(主要成分为
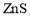 ,含
,含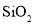 和少量
和少量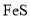 、
、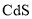 、
、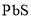 等杂质)为原料制备金属锌的生产流程如图所示。下列说法错误的是
等杂质)为原料制备金属锌的生产流程如图所示。下列说法错误的是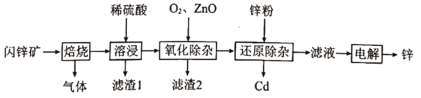
A.焙烧产生的气体可用作某些食品的杀菌保鲜剂
B.“滤渣1”置于烧碱溶液中可得澄清溶液
C.可以用
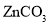 代替生产中加入的ZnO
代替生产中加入的ZnOD.获取锌后的电解液可以循环利用
难度: 中等查看答案及解析
-
氮气是一种重要的化工原料,工业上常用氮气合成氨、制硝酸。合成氨、制取硝酸的转化过程如图所示。下列说法正确的是
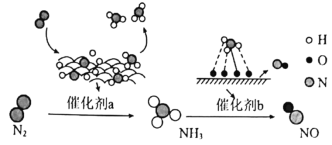
A.图示中N元素在转化过程中均被氧化
B.催化剂a可加快合成氨的反应速率并提高平衡转化率
C.不使用催化剂,上述转化不能发生
D.催化剂a与催化剂b表面均有极性键形成
难度: 中等查看答案及解析
-
已知可充电的钒锂电池的放电反应为
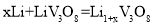 ,利用如图装置完成氢氧化铁胶体的电泳实验。下列说法正确的是
,利用如图装置完成氢氧化铁胶体的电泳实验。下列说法正确的是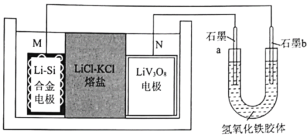
A.电子的移动方向为
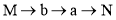
B.一段时间后电极b附近颜色变深
C.钒锂电池中
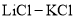 熔盐可以使用
熔盐可以使用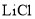 溶液代替
溶液代替D.电池的正极反应为
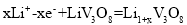
难度: 中等查看答案及解析
-
国际权威期刊《Science》刊发了德国化学家研究的以CO2为原料制备有机物的科研成果。已知
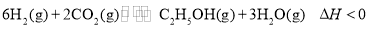 ,该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是
,该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是A.
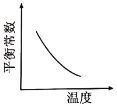 B.
B.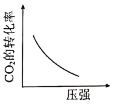
C.
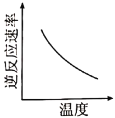 D.
D.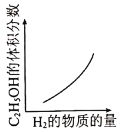
难度: 中等查看答案及解析
-
下列图像所表示的化学反应过程与对应的化学反应原理相符合的是
A
B
C
D
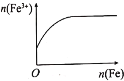
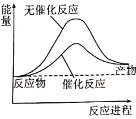
将铁粉加入到10mL、0.1mol/L的HNO3溶液中
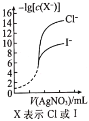
已知AgCl的Ksp大于AgI,0.01mol/L AgNO3溶液滴入到等浓度的Cl-、I-的混合液中
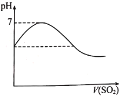
已知H2SO3的Ka1大于H2S的Ka2,SO2气体通入到饱和的H2S溶液中
SO2与O2在密闭容器中反应:2SO2(g)+O2(g)⇌2SO3(g) ∆H<0
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
已知
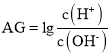 ,室温下,用
,室温下,用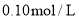 的盐酸滴定
的盐酸滴定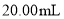 相同浓度的某一元碱
相同浓度的某一元碱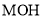 ,溶液的
,溶液的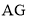 与所加盐酸的体积关系如图所示。下列有关说法错误的是
与所加盐酸的体积关系如图所示。下列有关说法错误的是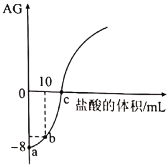
A.不同温度下,若
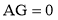 ,则溶液一定显中性
,则溶液一定显中性B.
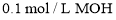 的电离度大约为1%
的电离度大约为1%C.可用甲基橙作指示剂
D.b点溶液中存在:
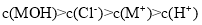
难度: 中等查看答案及解析
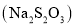 易被氧化,可存在于碱性溶液中,化工上常用作脱氯剂。下面是某兴趣小组在实验室进行的脱氯实验,回答下列问题:
易被氧化,可存在于碱性溶液中,化工上常用作脱氯剂。下面是某兴趣小组在实验室进行的脱氯实验,回答下列问题: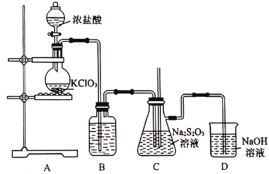
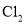 的化学反应方程式为_______________。
的化学反应方程式为_______________。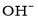 、
、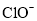 、
、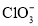 ,推测一定还含有的阴离子是________,若D中
,推测一定还含有的阴离子是________,若D中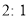 ,则反应消耗的
,则反应消耗的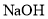 的物质的量之比为_____________。
的物质的量之比为_____________。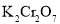 的一种化工流程如下:
的一种化工流程如下: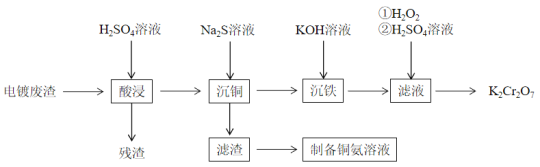
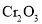 、
、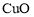 、FeO及
、FeO及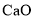 。
。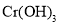 属于两性氢氧化物,碱性条件下,
属于两性氢氧化物,碱性条件下,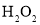 可将溶液中Cr(Ⅲ)氧化为
可将溶液中Cr(Ⅲ)氧化为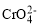 ;酸性条件下,
;酸性条件下,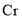 (Ⅵ)还原为
(Ⅵ)还原为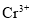 。
。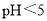 时,主要以
时,主要以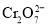 的形式存在;在
的形式存在;在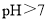 时,主要以
时,主要以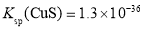 ,
,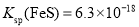 。
。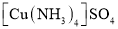 溶液,该反应的化学方程式为_________________;该步骤温度不宜过高,原因是_______________(写出2点)。
溶液,该反应的化学方程式为_________________;该步骤温度不宜过高,原因是_______________(写出2点)。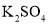 、
、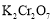 的溶解度曲线变化如图所示,则从滤液中获得粗
的溶解度曲线变化如图所示,则从滤液中获得粗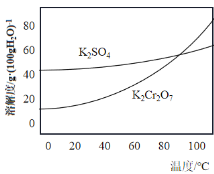
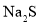 溶液,当Cu2+完全沉淀时,有无
溶液,当Cu2+完全沉淀时,有无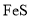 沉淀生成?列式计算说明。(已知:此时溶液中
沉淀生成?列式计算说明。(已知:此时溶液中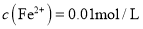 ,离子浓度小于
,离子浓度小于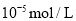 时认为完全沉淀)______________。
时认为完全沉淀)______________。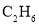 制取具有工业使用价值的
制取具有工业使用价值的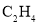 气体。回答下列问题:
气体。回答下列问题: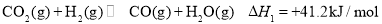
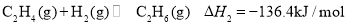
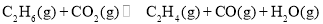
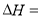 _____
_____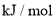 。
。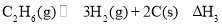 。
。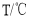
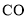
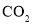 中生成
中生成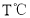 、
、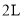 的某刚性容器中充入
的某刚性容器中充入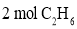 、
、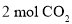 混合气体,压强为p,若仅发生如下反应:
混合气体,压强为p,若仅发生如下反应: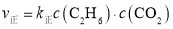 ,逆反应速率为
,逆反应速率为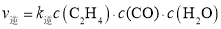 ,其中
,其中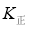 、
、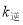 为速率常数,则
为速率常数,则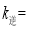 ______(以
______(以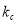 和
和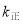 表示),
表示),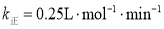 ,则平衡时
,则平衡时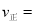 ________。
________。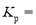 ______。
______。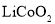 、
、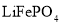 是锂离电池常用的电极材料。回答下列相关问题:
是锂离电池常用的电极材料。回答下列相关问题: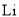 、
、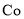 、O三种元素的电负性大小顺序为________;第二周期元素中,第一电离能介于
、O三种元素的电负性大小顺序为________;第二周期元素中,第一电离能介于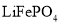 结构中,
结构中,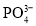 的空间构型为________,写出一个与之属于等电子体的离子________。
的空间构型为________,写出一个与之属于等电子体的离子________。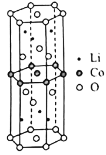
 型晶型,晶体中O原子的配位数为_______;晶体中O原子占据金属原子形成的_______(填“四而体空隙”或“八而体空隙”)。
型晶型,晶体中O原子的配位数为_______;晶体中O原子占据金属原子形成的_______(填“四而体空隙”或“八而体空隙”)。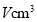 ,设
,设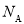 表示阿伏加德罗常数的值,则
表示阿伏加德罗常数的值,则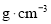 。
。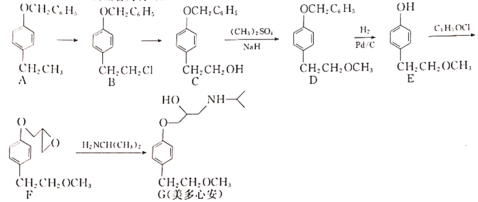
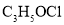 的结构简式为________。
的结构简式为________。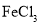 溶液发生显色反应,能发生水解反应;②
溶液发生显色反应,能发生水解反应;②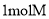 能够与
能够与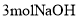 反应;③苯环上仅有两个侧链。
反应;③苯环上仅有两个侧链。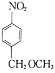 的线路图(写出必要的试剂及反应条件)。_________
的线路图(写出必要的试剂及反应条件)。_________