-
某外控型食品保鲜剂以淀粉、二氧化硅(SiO2)为载体,吸附酒精制作而成。保鲜原理是酒精缓慢挥发,在食品周围形成一定浓度的气体保护层。下列说法错误的是
A.酒精挥发时分子体积变大 B.起保鲜作用的物质是酒精
C.该保鲜剂不能与明火接触 D.SiO2中的Si的化合价为+4
难度: 中等查看答案及解析
-
在公路上,经常能见到运输汽油、柴油的油罐车,其车身上往往有以下哪种危险品标志

难度: 简单查看答案及解析
-
下列操作正确的是
A. pH试纸直接蘸取NaOH溶液测定其pH
B. 存放化学品的仓库失火后,尽快用水灭火
C. 蒸馏时,加热一段时间后,再投入沸石
D. 切割剩下的白磷放回原试剂瓶水封保存
难度: 简单查看答案及解析
-
下列实验操作正确的是
A. 分液时,先将上层液体从上口倒出
B. 萃取时,振荡后,须打开活塞放气
C. 蒸馏时,先点燃酒精灯,后通冷凝水
D. 蒸发时,将溶剂蒸干一段时间后,熄灭酒精灯
难度: 简单查看答案及解析
-
下列情境中,对分离原理说法错误的是
A.沙里淘金,利用了沙子和金子的密度不同
B.海水晒盐,利用了水和NaCl的沸点不同
C.酒糟酿酒,利用了粮食和酒精分子的颗粒大小不同
D.植物油能萃取蔬菜汁中的植物精华——维生素,利用了维生素在水和油中溶解度不同
难度: 简单查看答案及解析
-
9月15日22时04分09秒,长征二号FT2火箭托举着天宫二号空间实验室腾空而起,成功送上太空。该火箭所用的推进燃料偏二甲肼(化学式为C2H8N2),下列说法中正确的是
A.lmolC2H8N2中含有lmolN2
B.偏二甲肼的摩尔质量为60g
C.偏二甲肼是比液氢更环保的燃料
D.偏二甲肼燃烧时能放出大量的热和气体
难度: 简单查看答案及解析
-
绿色植物是空气天然的“净化器”,研究发现,10000m2柳杉每月可以吸收160kgSO2,则100 m2柳杉每月吸收的SO2的物质的量为
A.2.5mol B.5mol C.25mol D.250mol
难度: 简单查看答案及解析
-
右图是BaC12溶液在稀释过程中,c(Ba2+)随溶液体积的变化曲线图,则M点时,溶液中c(Cl-)为

A. 0.25mol/L B. 0.5mol/L C.1 mol/L D.2mol/L
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的数值,下列叙述正确的是
A.17gOH-中含有的电子数为10NA
B.标准状况下,lmol CCl4的体积约为22.4L
C.1mol/LNa2CO3溶液中含有的Na+离子数为2NA
D.常温常压下,1NA个CO2分子占有的体积为22.4L
难度: 简单查看答案及解析
-
下列实验操作能达到实验目的的是
选项
实验目的
实验操作
A
除去CO中少量的CO2
通过足量灼热CuO
B
除去CuCO3溶液中的少量 CuO
加入足量稀H2SO4后,过滤
C
鉴别澄清石灰水和NaOH溶液
加入稀HCl
D
鉴别硬水和软水
加入肥皂水
难度: 中等查看答案及解析
-
下列除去杂质的试剂、方法的选择均正确的是

难度: 简单查看答案及解析
-
科学家己发现一种新型气态氢分子H3,在同温、同压下,等体积的H3和H2具有相同的
A.原子数 B.分子数 C.密度 D.质子数
难度: 简单查看答案及解析
-
对于某些离子的检验及结论正确的是
A.加入紫色石蕊试液,溶液变蓝,证明溶液中含有较多的H+
B.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-
C.加入稀硫酸后,生成能使澄清石灰水变浑浊的气体,可确定有大量的CO32-
D.加入盐酸酸化时无现象,再滴入BaCl2溶液,产生白色沉淀,可确定有SO42-
难度: 困难查看答案及解析
-
常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是
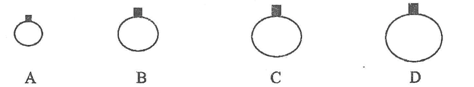
难度: 简单查看答案及解析
-
奥运会篮球比赛用球男女有别。男子篮球比赛用7#球,内部空间体积大约是7.35L,比赛时内部压强约为170kPa。己知,在25℃,100kPa时,气体摩尔体积约为24.5L/mol。假设比赛场馆温度为25℃,下列说法中正确的是
A.比赛时,篮球内一般充填氮气
B.比赛时,篮球内约有空气0.3mol
C.比赛时,篮球内约有空气14.8g
D.当25℃,170kPa时,Vm>24.5L/mol
难度: 简单查看答案及解析
-
近年,我国科学家首次拍摄到水分子团簇图像,模型如下图.下列说法正确的是

A.H、O两种元素只能组成水 B.团簇中的水分子不再运动
C.水蒸气冷凝成水,分子间隔减小 D.可燃冰和冰都是由水分子构成的
难度: 中等查看答案及解析
-
标准状况下,aL气体X2和bL气体Y2恰好完全反应生成cL气体Z,若2a=6b=3c,则Z的化学式为
A.X3Y B.XY3 C.XY2 D.X2Y
难度: 中等查看答案及解析
-
如何减少温室气体CO2的含量是科学家一直在探究的课题,最近中国科学技术大学的专家找到一种新型催化剂,可将CO2转化为液体燃料甲酸(CH2O2),下列说法中,不正确的是
A.地球上CO2含量上升的主要原因是植物的呼吸作用
B.CO2能吸收地面辐射,对地球有保温作用
C.CO2转化为甲酸的过程属于化学变化
D.这种新型催化剂在反应前后质量不变
难度: 中等查看答案及解析
-
己知:60℃ 时,KNO3的溶解度为110g。在此温度下,向盛有l00mL水的烧杯中投入101g KNO3后充分搅拌,此烧杯中将会得到
A.悬浊液 B.饱和溶液
C.质量分数约为50%的溶液 D.物质的量浓度为10mol/L的溶液
难度: 简单查看答案及解析
-
将15mL 2mol/LNa2CO3溶液逐滴加入到40mL 1.5mol/LMCln盐溶液中,恰好将溶液中的Mn+完全沉淀为碳酸盐,则MCln中n值是()
A.4 B.3 C.2 D.l
难度: 中等查看答案及解析