-
某兴趣小组为了探究一瓶久置的氢氧化钠溶液的变质情况,取出100g该溶液样品进行实验,依次加入质量分数4.9%的稀硫酸,测得的实验数据如下表所示:
实验编号
①
②
③
④
⑤
稀硫酸的质量(g)
20.0
40.0
60.0
80.0
100.0
溶液的总质量(g)
120.0
140.0
159.78
179.56
199.56
请回答下列问题:
(1)实验①﹑②没有产生气体的原因是 。
(2)100g溶液样品中碳酸钠的质量 。
(3)计算100g溶液样品中已经变质的氢氧化钠的质量(写出计算过程)
(3)分析实验数据,在图中,画出加入4.9%的稀硫酸质量0—80.0g过程中,产生气体质量对应的变化图,并标注必要的数值。
九年级化学计算题中等难度题查看答案及解析
-
测定合金中铜的质量分数。为测定某铜、锌合金中铜的质量分数,兴趣小组同学称取20g合金于烧杯中,将80g稀盐酸分四次加入,充分反应,测得实验数据如下表所示:
第一次
第二次
第三次
第四次
加入稀盐酸的质量(g)
20
20
20
20
烧杯中剩余物的质量(g)
39.92
59.84
79.80
99.80
(1)该铜、锌合金中铜的质量分数为_____________? (写出计算过程)
(2)第三次加入稀盐酸后烧杯内溶液中的溶质为________________(写化学式)。
九年级化学计算题困难题查看答案及解析
-
我省某地石灰石资源丰富。某化学兴趣小组称取8.0g石灰石样品,把100g稀盐酸分5次加入样品中(假设杂质不反应也不溶解),得实验数据如下表所示:请计算:
稀盐酸的用量
剩余固体的质量
第一次加入20g
6.0g
第二次加入20g
4.0g
第三次加入20g
2.0g
第四次加入20g
1.2g
第五次加入20g
1.2g
(1)8.0g石灰石样品中碳酸钙的质量是________g。
(2)求所用稀盐酸的溶质质量分数。(写出计算过程,结果精确到0.1%)______
九年级化学计算题中等难度题查看答案及解析
-
某化学兴趣小组的同学,为了判断某铁合金是生铁还是钢。取该铁合金8.6克(已知合金中只含铁、碳元素)于烧杯中,将80克稀酸分四次加入,充分反应,测得实验数据如下表所示。
一
二
三
四
加入稀硫酸的质量/g
20
20
20
20
烧杯中剩余物的质量/g
28.5
48.4
68.3
88.3
(1)铁合金完全反应生成氢气的总质量为_____克;
(2)请通过计算判断。该铁合金属于生铁还是钢?_____
九年级化学计算题中等难度题查看答案及解析
-
某硫酸厂产生的废水含有硫酸,需经处理至中性。兴趣小组的同学取100g酸性废水样品于烧杯中,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如下图所示。(假设废水中其他成分不与氢氧化钾反应)
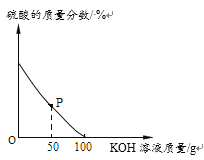
(1)P点对应溶液中含有的溶质有___________(填化学式)。
(2)计算废水中硫酸的质量分数__________。(精确到0.1%)
(3)请在如图中画出生成盐的曲线__________。
(4)工业上处理上述废水,应选用_____________更合理(填“KOH”或“CaO”)。(已知市场价格:KOH为9800元/t,CaO为70元/25kg。)
九年级化学计算题困难题查看答案及解析
-
为测定某黄铜(假设合金中仅含铜、锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉未于烧杯中,将80g稀盐酸分四次加入,充分反应后测得实验数据如下表:
第一次
第二次
第三次
第四次
加入稀盐酸的质量(g)
20
20
20
20
烧杯中剩余物的质量(g)
39.9
59.8
79.7
99.7
生成气体的质量(g)
0.1
X
0.3
0.3
(1)上述表格中X的值为_______g。
(2)该黄铜中铜的质量分数为______?(写出计算过程,计算结果保留两位小数)
(3)根据表中的数据,画出产生氢气的质量随加入稀盐酸的质量的变化关系;____________
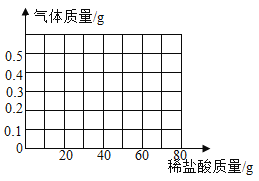
(4)同学们观察到反应一段时间后产生气体的速率减慢,原因可能是________。
九年级化学计算题中等难度题查看答案及解析
-
某化学兴趣小组的同学称取8.0g大理石样品,把80g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),测得实验数据如下表:
稀盐酸的用量
剩余固体的质量
第一次加入20g
6.0g
第二次加入20g
4.0g
第三次加入20g
2.0g
第四次加入20g
2.0g
(1)第 次加入稀盐酸时,大理石样品恰好完全反应。
(2)所加稀盐酸的溶质质量分数
九年级化学计算题中等难度题查看答案及解析
-
黄铜在日常生活中应用广泛,如许多电子元件、家用龙头等,为了测定某黄铜(合金中仅含铜、锌)中铜的含量。某兴趣小组称取25g黄铜粉末于烧杯中,将100g稀硫酸分四次加入,充分反应后,测得实验数据如下表:
次数
第1次
第2次
第3次
第4次
加入稀硫酸的质量(g)
25
25
25
25
烧杯中剩余物的质量(g)
49.88
74.76.
99.70
124.70
(1)第1次反应生成的氢气的质量 。
(2)该黄铜粉末的中铜的质量分数是多少?
(3)第3次实验后所得溶液中的溶质是(写化学式)?
九年级化学计算题简单题查看答案及解析
-
为测定某石灰石矿中碳酸钙的含量,兴趣小组同学称取12.5g石灰石矿样品粉末于烧杯中,将80 g稀盐酸分四次加入,充分反应,测得实验数据如下表所示(杂质不溶于水,也不参与反应,生成的气体全部逸出):
第一次
第二次
第三次
第四次
加入稀盐酸的质量(g)
20
20
20
20
烧杯中剩余物的质量(g)
30.5
48.5
68.1
88.1
(1)样品完全反应生成二氧化碳的总质量为多少g。
(2)计算该石灰石矿中碳酸钙的质量分数。
九年级化学计算题中等难度题查看答案及解析
-
兴趣小组同学取某种钢样(假设只含铁单质及碳单质)进行试验.分别向四份不同质量的钢样粉末中加入100g稀硫酸溶液,充分反应后,测得的实验数据如表所示:
(1)第三次实验是否恰好完全反应(填“是”或“否”)______.序号
质量实验1 实验2 实验3 实验4 钢样粉末质量(g) 2.84 4.25 6.23 7.51 生成H2的质量(g) 0.10 0.15 0.20 0.20
(2)计算100硫酸溶液中溶质的质量______g.
(3)求在实验3中溶液的溶质质量分数?(要写过程)九年级化学解答题中等难度题查看答案及解析