-
(1)为延长食品保质期,常在食品中添加苯甲酸(C6H5COOH)作为防腐剂。回答下列问题:①苯甲酸是由 种元素组成;②苯甲酸中碳元素与氢元素的质量比为 (最简整数比)。
(2)小明称取黄铜(铜锌合金)样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,测得实验数据如图所示。
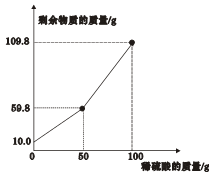
求:
①该铜锌合金中,铜和锌的质量比是 (最简整数比)。
②所用稀硫酸溶液中溶质的质量分数是多少?
九年级化学简答题极难题查看答案及解析
-
图中的A--H是初中化学常见的化合物,其中B是氧化物,白色固体F易溶于水并放出大量的热,G、H是配置农药波尔多液的原料。“—”表示相互能反应,“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
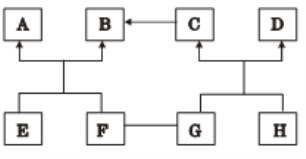
(1)F的化学式是_________________,
H的另一种常见用途是_______________。
(2)G和H反应的化学方程式_____________,
该反应的基本类型是_________________。
(3)若A、B、E、F是不同类别的化合物,则E和F反应的化学方程式____。
九年级化学简答题极难题查看答案及解析
-
Na2CO3中往往会含有少量的NaCl,现在一烧杯中盛有20.4g的固体混合物,向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
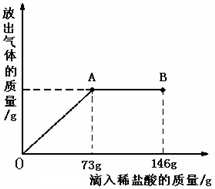
(1)当滴加稀盐酸至图中B点时,烧杯中溶的pH 7(填>、=、<)。
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)
九年级化学简答题极难题查看答案及解析
-
圆明园十二生肖兽首中的兔首和鼠首(如图)均为青铜器(铜、锡合金),某些铜器表面呈绿色,这是因为铜器长期暴露在空气中生了铜锈(俗称铜绿)。为了弄清铜绿的组成和铜生成铜绿的条件,某化学兴趣小组进行了如下探究:探究铜生锈的条件。

【查阅资料】铜绿的化学式是Cu2(OH)2CO3,它受热会分解生成三种氧化物。铜绿分解的化学方程式为______________________________________________________。
【猜想与假设】依据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及____________________共同作用而形成的。
【设计与实验】借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如图所示(所用铜片洁净、光亮):实验较长时间后,发现________试管中铜片最先生锈(填试管字母编号)。
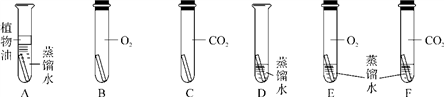
【评价与改进】小风认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是_________________________。
【拓展与应用】小明发现从不同地点收集到的两个铜器(一个材质是纯铜,一个材质是青铜)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小明的分析是否全面?并说明理由:____________________________________________________。
九年级化学简答题极难题查看答案及解析
-
一种名为“污渍爆炸盐”的洗涤产品能高效去除衣物上的顽固污渍,某化学兴趣小组对此产生了兴趣,开展了如下探究。
查阅资料:“污渍爆炸盐”的主要成分是过碳酸钠(化学式为Na2CO4),它是一种白色粉末,易溶于水且能与水反应生成甲和乙两种化合物,其中化合物乙有强氧化性,具有较好的去污效果。碳酸钠常温或加热不分解。
(1)小明同学对化合物乙的强氧化性产生兴趣,为了探究它的成分,做了如下实验设计,请你和他一起探究,完成下面问题。
序号
实验步骤
实验现象
实验结论与解释
1
取少量“污渍爆炸盐”于试管中,加入适量的水
固体溶解
该固体易溶于水且能与水反应
2
向1中所得的液体中加入适量的二氧化锰
产生大量气泡
3
将带火星的小木条放在试管中,观察现象
木条复燃
试管中产生的气体是________(填化学式,下同),过碳酸钠和水反应生成的化合物乙是________
(2)写出步骤2产生气体的化学方程式:____________________________。
(3)小明同学认为生成的化合物甲可能是碳酸钙(CaCO3),小亮同学认为可能是碳酸钠(Na2CO3)。你支持________同学的观点,你的理由是_____________________。
小磊同学将“污渍爆炸盐”放入冷水中,发现产生少量气泡;而放入热水中,产生较多气泡。由此,你认为影响化合物乙分解快慢的因素是____________。测定分解快慢的方法有很多,请你再写出一种测定的实验方法(用简洁的文字表述):________________。
(5)影响化合物乙分解快慢的因素还有哪些?请你提出一个猜想,并设计实验方案验证你的猜想。
猜想:____________________________________________。
实验方案:__________________________________________。
九年级化学简答题极难题查看答案及解析
-
(1)实验室现有溶质质量分数为98%、密度是1.84g·mL-1的浓硫酸20 mL,需要多少毫升水(水的密度是1g·mL-1)才能配制成19.6%的稀硫酸? ________________
(2)将10g锌铜合金投入154.7g稀硫酸中,恰好完全反应,生成氢气0.2g。求:
①求该锌铜合金中锌的质量。________________
②反应后所得溶液的溶质质量分数。________________
九年级化学简答题极难题查看答案及解析
-
A~H是初中化学常见的不同物质,它们的相互转化关系如下图所示。其中A是一种绿色固体,B是一种黑色固体,H能和人体中血红蛋白结合,H和D的组成元素相同。请回答下列问题:
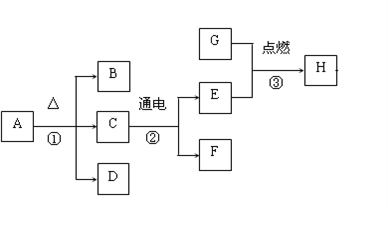
(1)反应①的基本反应类型为_______反应。
(2)B的化学式为_______。
(3)反应②的化学方程式为_______________________________。
(4)H和D的组成元素相同,但化学性质不同,原因是_____________________。
(5)H的用途有__________(写一点即可)。
九年级化学简答题极难题查看答案及解析
-
已知某固体混合物A中可能含有CuSO4、FeCl3、NaNO3、 BaCl2、CaCO3五种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所有发生的反应都恰好完全反应)。
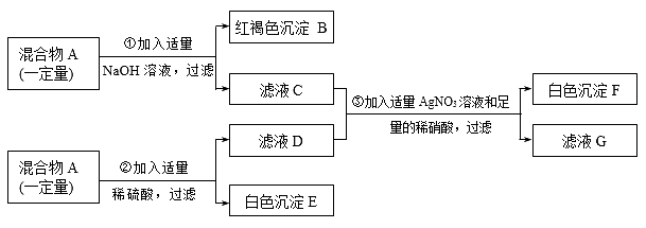
根据上述实验过程和发生的现象做出相应推理,填写以下空白:
(1)红褐色沉淀B的化学式是_______________。
(2)在固体混合物A里,上述五种物质中肯定存在的物质是_________________。
(3)写出步骤③中生成白色沉淀F的1个化学方程式________________。
(4)在滤液G中,含有的金属阳离子共有________种。
(5)在混合物A里,上述五种物质中肯定不存在的物质是(写化学式)__________,得出此结论的理由是_______________。
九年级化学简答题极难题查看答案及解析
-
A、B、C、D、E是初中化学中常见的物质。它们之间的转化关系如图所示(“→”表示物质之间的转化关系,“——”表示两端的物质能发生化学反应,有些转化关系的反应条件和其它反应物等已略去)。其中,A、B、C、D在一定条件下都能生成E;A和B都是黑色固体,且A为氧化物,B为单质,两者也能反应生成E;C是常见的补钙剂中的主要成分;D与E的组成元素种类相同。据此完成下列各题。
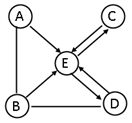
(1)写出E的化学式____________。
(2)写出A和B发生反应的化学方程式________________________。
(3)写出D→E反应的化学方程式 ______________________________。
(4)写出物质D的一种用途:______________________________。
九年级化学简答题极难题查看答案及解析
-
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如下图所示。试回答下列问题:
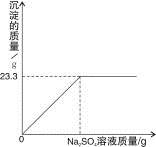
(1)完全反应后生成BaSO4沉淀 g。
(2)恰好完全反应时消耗Na2SO4溶液的质量是 g。
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?(精确到0.1%)
九年级化学简答题极难题查看答案及解析