-
下列说法不正确的是( )
A.牛油、植物油、汽油在碱性条件下的水解反应可以制造肥皂
B.氨基酸、蛋白质都既能和盐酸反应,也能和氢氧化钠溶液反应
C.向鸡蛋清溶液中加入饱和硫酸钠溶液产生沉淀属于物理变化
D.用酶催化淀粉水解的水解液中加入银氨溶液,水浴加热,无光亮银镜生成,说明无葡萄糖存在
难度: 中等查看答案及解析
-
下列属于碱的是( )
A.SO2 B.CH3CH2OH C.Ca(OH)2 D.KCl
难度: 简单查看答案及解析
-
下列仪器的用法正确的是( )
A.
①可以长期盛放溶液
B.
用②进行分液操作
C.
用酒精灯直接对③进行加热
D.
用④进行冷凝回流
难度: 简单查看答案及解析
-
下列属于置换反应的是( )
A.2C+SiO2
2CO+Si
B.2HClO
2HCl+O2↑
C.3CO+Fe2O3
3CO2+2Fe
D.2Na+Cl2=2NaCl
难度: 简单查看答案及解析
-
下列气体能使湿润的蓝色石蕊试纸最终变红的是 ( )
A.NH3 B.SO2 C.Cl2 D.CO
难度: 简单查看答案及解析
-
下列变化过程中,加入氧化剂才能实现的是( )
A.Cl2→Cl- B.Fe2+→Fe3+ C.Na2O2→O2 D.SO2→SO32-
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.液氯可以储存在钢瓶中
B.工业制镁时,直接向海水中加Ca(OH)2溶液以制取Mg(OH)2
C.用硫酸清洗锅炉后的水垢
D.在水泥回转窖中用石灰石、纯碱、黏土为原料制造水泥
难度: 简单查看答案及解析
-
下列表示正确的是( )
A.中子数为8的氧原子符号:
O
B.甲基的电子式:
C.乙醚的结构简式:CH3OCH3
D.CO2的比例模型:
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.沼气的主要成分是甲烷,它是不可再生能源
B.石油分馏得到的石油气常用来制造塑料或作为燃料
C.用煤气化得到的水煤气合成液态烃和含氧有机物的过程也属于煤的液化
D.垃圾分类处理后,对热值较高的可燃垃圾可进行焚烧发电
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.银氨溶液不能留存,久置后容易爆炸
B.白磷暴露在空气中易自燃,可保存在水中
C.易燃的有机溶剂使用时必须远离明火和热源
D.钠着火不能用水扑灭,可以用泡沫灭火器来灭火
难度: 中等查看答案及解析
-
下列实验能达到目的是( )
A.用饱和碳酸氢钠溶液鉴别SO2和CO2
B.用灼热的铜网除去CO中少量的O2
C.用溴水鉴别苯和CCl4
D.用蒸发结晶的方法从碘水中提取碘单质
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.H2与D2是氢元素的两种核素,互为同位素
B.甲酸(HCOOH)和乙酸互为同系物,化学性质不完全相似
C.C4H10的两种同分异构体都有三种二氯代物
D.石墨烯(单层石墨)和石墨烷(可看成石墨烯与H2加成的产物)都是碳元素的同素异形体,都具有良好的导电性能
难度: 中等查看答案及解析
-
元素X、Y、Z和Q在周期表中的位置如图所示,其中元素Q位于第四周期,X的最高正价和最低负价之和为0,下列说法不正确的是( )
X
Y
Z
Q
A.原子半径(r):r(Y)>r(Z)>r(X)
B.分别含Y元素和Z元素的两种弱酸可以反应生成两种强酸
C.推测Q的单质可以和氢气、氧气、活泼金属等反应
D.Z的简单阴离子失电子能力比Y的强
难度: 中等查看答案及解析
-
下列离子方程式不正确的是( )
A.3amolCO2与含2amolBa(OH)2的溶液反应:3CO2+4OH-+Ba2+=BaCO3↓+2HCO3﹣+H2O
B.NH4Fe(SO4)2溶液中加入几滴NaOH溶液:Fe3++3OH-=Fe(OH)3↓
C.亚硫酸溶液被氧气氧化:2SO32-+O2=2SO42-
D.酸性高锰酸钾溶液中滴加双氧水产生气泡:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑
难度: 中等查看答案及解析
-
向恒温恒容密闭容器中充入1molX和2molY,发生反应4X(g)+2Y(g)⇌3Z(g),下列选项表明反应一定已达平衡状态的是( )
A.气体密度不再变化
B.Y的体积分数不再变化
C.3v(X)=4v(Z)
D.容器内气体的浓度c(X):c(Y):c(Z)=4:2:3
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.新戊烷的系统命名法名称为2﹣二甲基丙烷
B.可以用氢气除去乙烷中的乙烯
C.己烷中加溴水振荡,光照一段时间后液体呈无色,说明己烷和溴发生了取代反应
D.苯中加溴的四氯化碳溶液振荡后,溶液分层,上层呈橙红色
难度: 中等查看答案及解析
-
如图是一种染料敏化太阳能电池的示意图,电池的一个电极由有机光敏染料(R)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,下列关于该电池叙述不正确的是( )

A.染料敏化TiO2电极为电池负极,发生氧化反应
B.正极电极反应式是:I3-+2e-=3I-
C.电池总反应是:2R++3I-=I3-+2R
D.电池工作时将太阳能转化为电能
难度: 中等查看答案及解析
-
下列说法正确的是
A.
时,将
的碳酸钠溶液加水稀释100倍,所得溶液的
B.pH相同的盐酸和醋酸溶液分别与足量镁粉反应,醋酸产生
体积更大
C.
时,
的HA弱酸溶液与
的NaOH溶液等体积混合,所得溶液pH一定小于7
D.
溶液中加入一定量
晶体,溶液中
增大,可以证明
为弱酸
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.某化合物在熔融状态下能导电,则该物质属于离子化合物
B.金属钠与水反应过程中,既有共价键的断裂,也有共价键的形成
C.硅单质与硫单质熔化时所克服微粒间作用力相同
D.CO2和NCl3中,每个原子的最外层都具有8电子稳定结构
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.pH=1的硫酸溶液1L,溶液中含SO42-的数目等于0.1NA
B.真空密闭容器中充入0.1molH2和0.1molI2充分反应后,容器内分子总数为0.2NA
C.10mL0.1mol⋅L-1的FeCl3与20mL0.1mol⋅L-1KI溶液反应,转移电子数为0.001NA
D.60gSiO2晶体中Si-O键数目为2NA
难度: 中等查看答案及解析
-
甲烷与氯气光照条件下取代反应的部分反应历程和能量变化如下:
第一步:
第二步:

第三步:
中
其中
表示氯原子,
表示甲基
,下列说法不正确的是( )
A.由题可知,甲烷和氯气在室温暗处较难反应
B.

C.形成
中
键放出的能量比拆开
中化学键吸收的能量多
D.若是甲烷与
发生取代反应,则第二步反应
难度: 中等查看答案及解析
-
已知:A(g)+3B(g)⇌2C(g)。起始反应物为A和B,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中C的物质的量分数如下表:下列说法不正确的是( )
温度
物质的量分数
压强
400℃
450℃
500℃
600℃
20MPa
0.387
0.274
0.189
0.088
30MPa
0.478
0.359
0.260
0.129
40MPa
0.549
0.429
0.322
0.169
A.压强不变,降低温度,A的平衡转化率增大
B.在不同温度下、压强下,平衡时C的物质的量分数可能相同
C.达到平衡时,将C移出体系,正、逆反应速率均将减小
D.为提高平衡时C的物质的量分数和缩短达到平衡的时间,可选择加入合适的催化剂
难度: 中等查看答案及解析
-
25℃时,向20.00mL0.100mol•L-1的氨水和醋酸铵溶液中分别滴加0.100mol•L-1的盐酸溶液,溶液pH随加入盐酸体积的变化如图所示。下列说法不正确的是( )
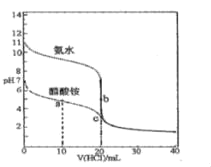
A.25℃时,Kb(NH3•H2O)=Ka(CH3COOH)≈10-5
B.b点溶液中水的电离程度比c点溶液中的大
C.在c点的溶液中:c(Cl﹣)>c(CH3COOH)>c(NH4+)>c(OH﹣)
D.在a点的溶液中:c(NH4+)+2c(H+)═2c(CH3COO-)+c(NH3•H2O)+2c(OH-)
难度: 中等查看答案及解析
-
举世闻名的侯氏制碱法的工艺流程如下图所示,下列说法正确的是( )

A.往母液中加入食盐的主要目的是使
更多的析出
B.从母液中经过循环Ⅰ进入沉淀池的主要是
、
和氨水
C.沉淀池中反应的化学方程式:

D.设计循环Ⅱ的目的是使原料氯化钠的利用率大大提升
难度: 中等查看答案及解析
-
将①中物质逐步加入②中混匀(②中离子均大量存在),预测的现象与实际相符的是( )
选项
①
②溶液
预测②中的现象
A
稀盐酸
Na+、SiO32-、OH-、SO42-
立即产生白色沉淀
B
氯水
K+、I-、Br-、SO32-
溶液立即呈黄色
C
过氧化钠
Ca2+、Fe2+、Na+、Cl-
先产生白色沉淀,最终变红褐色
D
小苏打溶液
Al3+、Mg2+、Ba2+、Cl-
同时产生气体和沉淀
A.A B.B C.C D.D
难度: 中等查看答案及解析


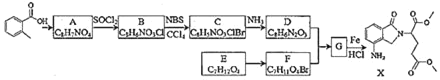
 ;②
;②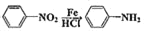 ;③
;③