-
已知X、Y、Z、W是短周期元素。X元素原子的2p能级处于半充满状态;Y元素原子最外电子层(L电子层)上s电子数和p电子数相等;Z元素的+2价阳离子的核外电子排布与氖原子相同;W元素原子的M电子层有1个未成对的p电子。下列说法一定正确的是( )
A.含有X元素的化合物一定是共价化合物
B.Y元素的电负性大于X元素的电负性
C.X元素的单质与Z元素的单质在一定条件下能发生化合反应
D.W元素的单质能与NaOH溶液反应放出氢气
化学单选题中等难度题查看答案及解析
-
已知A、B、C、D、E都是周期表中的前四周期的元素, 它们的核电荷数A<B<C<D<E。其中B、D、E原子最外层电子层的P能级(轨道)上的电子处于半充满状态。通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右图所示。原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一类半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料。
试回答下列问题:
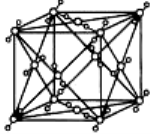
(1)基态Ga原子的核外电子排布式为: 。
(2)A、B、C的第一电离能由大到小的顺序: (用元素符号表示)。
(3)B元素的单质分子中有 个π键,与其互为等电子体的物质的化学式可能为 (任写一种)。
(4)上述A的氧化物分子中心原子采取 杂化,其晶胞中微粒间的作用力为 。
(5) EH3分子的空间构型为 ,其沸点与BH3相比 (填“高”或“低”),原因是
(6)向CuSO4溶液中逐滴加入BH3的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解得到深蓝色的透明溶液。请写出沉淀溶解的离子方程式 .
高三化学填空题中等难度题查看答案及解析
-
现有原子序数递增的X、Y、Z、W四种常见元素。其中X元素基态原子核外电子占据了三个能级,且每个能级上的电子数相等;Y原子的p轨道处于半充满状态,Z的单质是空气的主要成分之一;W在周期表中位于ds区,且与Z可形成化学式为W2Z或WZ的二元化合物。请回答下列问题:
⑴W元素原子核外电子运动状态有_____种,该元素基态离子W+的电子排布式为___________。
⑵元素X、Y和Z的第一电离能由大到小顺序为__________(填元素符号)。
⑶Y2Z与XZ2具有相同的结构特征,其理由是__________。
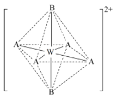
⑷X、Y和Z均可形成多种氢化物,写出一种X的氢化物分子结构中σ键和π键数目之比3∶2的结构式______;A、B分别是Y、Z的最简单氢化合物,A的空间构型为_______,其中Y原子的杂化轨道类型为______;W2+与A、B分子结合成配合离子[WA4B2]2+结构如下图,该配合离子加热时首先失去的组分是_____(填“A”或“B”)。
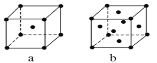
⑸元素W的单质晶体在不同温度下可有两种堆积方式,晶胞分别如图a和b所示,假定不同温度下元素W原子半径不变,且相邻最近原子间距为原子半径之和,则其体心立方堆积与面心立方堆积的两种晶体密度之比为_________。
高三化学综合题中等难度题查看答案及解析
-
M是原子序数小于30的一种金属,常用于航空、宇航、电器及仪表等工业部门,M原子的最外层有空轨道,且有两个能级处于半充满状态。
(1)M原子的外围电子排布式为 ,在周期表中属于 区元素。
(2)M的堆积方式属于钾型,其晶胞堆积方式为 ,其空间利用率为 。
(3)MCl3·6H2O有三种不同颜色的异构体
A、[M(H2O)6]Cl3 B、[M(H2O)5Cl]Cl2·H2O C、[M(H2O)4Cl2]Cl·2H2O。
为测定蒸发MCl3溶液析出的暗绿色晶体是哪种异构体,取0.010 mol MCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g。该异构体为_______________ (填A或B或C)。
(4)难溶碳酸盐受热易分解,试比较MgCO3和CaCO3的稳定性,并说明理由 .
(5)已知A12 Cl6 分子中每个原子都满足8电子稳定结构,写出其结构式 (用箭头表示配位键)。
(6)金刚石晶胞(如图
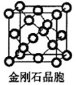 )含有 个碳原子。若碳原子半径为r pm ,金刚石晶胞的边长为a pm ,则r= a,列式并计算金刚石晶胞的空间利用率 。
)含有 个碳原子。若碳原子半径为r pm ,金刚石晶胞的边长为a pm ,则r= a,列式并计算金刚石晶胞的空间利用率 。高三化学填空题困难题查看答案及解析
-
已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B原子最外电子层的p能级处于半满状态,C原子最外层的p能级电子数是s能级电子数的2倍,C、F处于同一主族,E最外层电子数比最内层多1。回答下列问题:
(1)E元素基态原子的电子排布式为___。
(2)用电子排布图表示F元素原子的价电子排布:____。
(3)F、G元素对应的最高价含氧酸中酸性较强的是___(填化学式)。
(4)离子半径:D+___(填“<”“>”或“=”,下同)B3-,第一电离能:B___C,电负性:C__F。
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为___。试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式:__。
(6)写出E的单质与D的最高价氧化物对应的水化物反应的化学方程式:____。
高二化学推断题中等难度题查看答案及解析
-
已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B原子最外电子层的p能级处于半满状态,C原子最外层的p能级电子数是s能级电子数的2倍,C、F处于同一主族,E最外层电子数比最内层多1。回答下列问题:
(1)E元素基态原子的电子排布式为___。
(2)用电子排布图表示F元素原子的价电子排布:____。
(3)F、G元素对应的最高价含氧酸中酸性较强的是___(填化学式)。
(4)离子半径:D+___(填“<”“>”或“=”,下同)B3-,第一电离能:B___C,电负性:C__F。
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为___。试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式:__。
(6)写出E的单质与D的最高价氧化物对应的水化物反应的化学方程式:____。
高二化学推断题中等难度题查看答案及解析
-
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同;基态b原子的核外电子占据3个能级,且最高能级轨道为半充满状态;c的最外层电子数是内层电子数的3倍;d的原子序数是c的两倍;基态e原子3d轨道上有4个单电子。
回答下列问题:
(1)b、c、d电负性最大的是___(填元素符号)。
(2)b单质分子中σ键与π键的个数比为___。
(3)a与c可形成两种二元化合物分子,两种物质可以任意比互溶。其中一种不稳定,可分解产生c的单质,该化合物分子中的c原子的杂化方式为___;这两种物质的互溶物中,存在的化学键有___(填序号)。
①极性共价键 ②非极性共价键 ③离子键 ④金属键 ⑤氢键 ⑥范德华力
(4)这些元素形成的含氧酸中,分子内中心原子的价层电子对数为4的酸是___(填化学式,下同);酸根呈正三角形结构的酸是___,试从两者结构特点判断该酸分子与酸根离子的稳定性:酸分子___酸根离子(填“>”或“<”)。
(5)元素e在周期表中的位置是___区;e的一种常见氯化物中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在,结构式为
,请补写e的元素符号并用“→”表示出其中的配位键___。
高三化学推断题简单题查看答案及解析
-
(14分)W、X、Y、Z是元素周期表中前四周期的元素,它们的原子序数依次增加。请结合下表中的信息,回答下列问题
W
基态原子核外有三个能级,p能级电子处在半充满状态
X
是所有元素中电负性最大的元素
Y
气态氢化物及其最高价氧化物对应的水化物均为强酸
Z
原子序数为22,被称为“未来金属”
(1)Z位于元素周期表第_______族;该元素的基态原子价电子排布式为_____________。
(2)W与其同周期相邻的元素的第一电离能由大到小的顺序为________(填元素符号);X、Y两种元素与氢元素形成的共价键键能较大的是___________(请用元素符号表示)。
(3)X的气态氢化物的沸点在同族元素形成的气态氢化物中最_______(填“高”或“低”);已知WX3是微电子工业中优良的等离子刻蚀气体,沸点:129℃,其固态时的晶体类型为________,WX3在潮湿的空气中能与水蒸气发生氧化还原反应,反应生成的无色气体遇到空气变为红棕色,写出该反应的化学方程________。
(4)工业上制取Z的方法是:
第一步,在高温时,将金红石(ZO2)、炭粉混合并通人Y2制得ZY4和一种可燃性气体,已知(下列除Z、Y外其他都为实际元素符号)
①ZO2(s)+2Y(g)=ZY4(1)+O2(g) △H=-410.0kJ·mol-1
②CO(g)=C(s)+1/2O2(g) △H=+110.5 kJ·mol-1
则书写上述反应的热化学方程式是_________________________________________。
第二步,在氩气做保护气的环境中,用过量的金属镁在加热条件下与ZY4反应制得金属Z。
高三化学填空题困难题查看答案及解析
-
M是原子序数<30的一种金属,常用于航空、宇航、电器及仪表等工业部门,M原子的最外层有空轨道,且有两个能级处于电子半充满状态。

(1)M原子的外围电子排布式为_______________,在周期表中属于___________区元素。
(2)M的堆积方式属于钾型,其晶胞示意图为____(填序号)。其空间利用率为____。
(3) MCl3•6H2O有三种不同颜色的异构体
A、[M(H2O)6]Cl3,B、[M(H2O)5Cl]Cl2•H2O和C、[M(H2O)4Cl2]Cl•2H2O
为测定蒸发MCl3溶液析出的暗绿色晶体是哪种异构体,取0.10molMCl3·6H2O 配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g。该异构体为___________(填A或B或C)。
(4)常温下为暗红色液体,熔点-96. 5℃,沸点117℃,能与丙酮
等互溶。
①固态MO2Cl2属于___________晶体;
②中碳原子和丙酮(CH3COCH3)羰基中的碳原子分别采取的杂化方式为______杂化和_____杂化。
(5)+3价M的配合物
中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。
高二化学填空题中等难度题查看答案及解析
-
A、B、C、D、E、F为原子序数依次增大的六种元素,位于元素周期表的前四周期。B元素原子含有3个能级,且每个能级所含的电子数相同;D的原子核外有8种运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子3d轨道上有4个未成对电子。请回答下列问题:
(1)写出D基态原子的价电子排布图__________,F基态原子的外围电子排布式________。
(2)下列说法不正确的是____________(填序号)。
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点:SiO2>CO2
B.第一电离能由小到大的顺序:B
C.N2与CO为等电子体,结构相似
D.稳定性:H2O>H2S,水分子更稳定的原因是水分子间存在氢键
(3)F元素位于周期表中_____区,其离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点。向F的硫酸盐溶液中通入过量的C与A形成的气体X可生成[F(X)4]2+,该离子的结构式为_____________(用元素符号表示)。
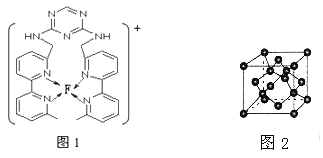
(4)某化合物与F(I)(I表示化合价为+1)结合形成图1所示的离子,该离子中碳原子的杂化方式为_________。
(5)B单质的一种同素异形体的晶胞如图2所示,则一个晶胞中所含B原子的个数为______。
(6)试从分子的立体构型和原子的电负性、中心原子上的孤电子对等角度解释与D的简单氢化物结构十分相似的OF2的极性很小的原因是____________。
(7)D与F形成离子个数比为1:1的化合物,晶胞与NaCl类似,设D离子的半径为apm。F离子的半径bpm,则该晶胞的空间利用率为______________。
高三化学综合题困难题查看答案及解析