-
Ca(OH)2变质得到Ca(OH)2和CaCO3的混合物。李琳同学设计了如下图的实验装置来测定CaCO3的含量,她用气密性良好的装置装上药品并通一会儿氮气后关闭止水夹,再打开分液漏斗活塞。提示:碱石灰(可以吸收CO2和H2O)浓硫酸均足量,稀盐酸不考虑其挥发性。
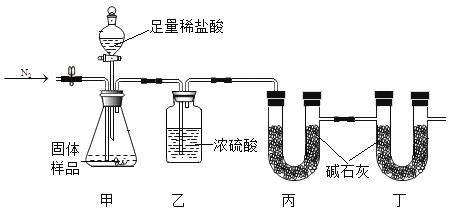
(1)通入N2的原因之一是N2的化学性质_____(填活泼或者不活泼)。
(2)甲装置中发生中和反应的化学方程式为_____。
(3)浓硫酸的作用是_____。
(4)测定CaCO3的含量需要测定两个物理量,其中一个物理量为样品的质量。
①另一个物理量为_____(填序号)。
A 滴下的稀盐酸质量 B 反应前后乙装置增加的质量
C 反应前后丙装置增加的质量 D 反应前后丁装置增加的质量
②若去掉丁装置,测得CaCO3含量_____(填“偏高”、“偏低”或“不变")。
③甲装置中反应结束后打开止水夹再通入一会儿N2的目的是_____。
-
Ca(OH)2变质得到Ca(OH)2和CaCO3的混合物。同学设计了如下图的实验装置来测定CaCO3的含量。提示:①碱石灰(主要成分:NaOH、CaO)、浓硫酸均足量,稀盐酸不考虑其挥发性。
②装置气密性良好,实验前弹簧夹K1、K2、K3处于关闭状态。
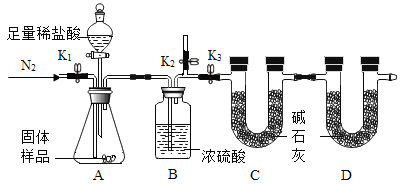
(1)A中反应前后都要通入氮气,选择氮气的理由是______。
(2)若没有B装置,测得CaCO3含量会______(填“偏高”、“偏低”或“不变”)。
(3)测定CaCO3的含量需要测定的数据是:样品的质量和______。
(4)利用上述装置测定碳酸钙的含量,写出不包含测量数据的实验操作______。
-
为了探究实验室中久置的生石灰样品变质情况,同学们进行如下图所示的实验。下列分析和结论不正确的是
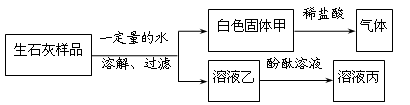
A.溶液丙呈红色
B.该样品中一定含有碳酸钙
C.固体甲可能为Ca(OH)2和CaCO3的混合物
D.该样品已完全变质
-
某校化学研究性学习课题组的同学们为了测定某氢氧化钙样品中Ca(OH)2的含量(含杂质CaCO3),共做了3次实验,使一定质量的该样品分别与同一种盐酸反应,所得相关实验数据记录如下表,请回答以下问题:
| 第1次 | 第2次 | 第3次 |
| 所取样品的质量/g | 17.4 | 17.4 | 17.4 |
| 所取稀盐酸的质量/g | 80 | 100 | 120 |
| 生成CO2的质量/g | 2.64 | 4.4 | 4.4 |
(1)在第_____次实验中,反应容器内有白色固体剩余。该实验中所发生反应的化学方程式为: 、 。
(2)求原样品中Ca(OH)2的质量分数?(计算结果精确到0.1%)
-
某校化学研究性学习课题组的同学们为了测定某氢氧化钙样品中Ca (OH)2含量(含有的杂质为CaCO3),共做了3次实验,使一定质量的该样品分别与同一种盐酸反应,所得相关实验数据记录如下表:
| 第1次 | 第2次 | 第3次 |
| 所取样品的质量 | 20g | 20g | 20g |
| 所取稀盐酸的质量 | 80g | 100g | 120g |
| 生成CO2的质量 | 3.58g | 4.4g | 4.4g |
(1)在第________________________________________________________________________________________ 次实验中,反应容器内有白色固体剩余。
(2)求原样品中Ca(OH)2的质量分数?
-
某校化学研究性学习课题组的同学们为了测定某氢氧化钙样品中Ca (OH)2含量(含有的杂质为CaCO3),共做了3次实验,使一定质量的该试样分别与同一种盐酸反应,所得相关实验数据记录如下表:
| 第1次 | 第2次 | 第3次 |
| 所取样品的质量 | 17.4g | 17.4g | 17.4g |
| 所取稀盐酸的质量 | 80g | 100g | 120g |
| 生成CO2的质量 | 2.64g | 4.4g | 4.4g |
(1)在第______次实验中,反应容器内有白色固体剩余.
(2)求原试样中Ca (OH)2的质量分数?
-
某校化学研究性学习课题组的同学们为了测定某氢氧化钙样品中Ca (OH)2含量(含有的杂质为CaCO3),共做了3次实验,使一定质量的该试样分别与同一种盐酸反应,所得相关实验数据记录如下表:
| 第1次 | 第2次 | 第3次 |
| 所取样品的质量 | 17.4g | 17.4g | 17.4g |
| 所取稀盐酸的质量 | 80g | 100g | 120g |
| 生成CO2的质量 | 2.64g | 4.4g | 4.4g |
(1)在第______次实验中,反应容器内有白色固体剩余.
(2)求原试样中Ca (OH)2的质量分数?
-
某校化学研究性学习小组的同学们为了测定某氢氧化钙试样品中的Ca(OH)2含量(含有的杂质为CaCO3),共做了三次实验,使一定质量的该试样分别与同一种盐酸反应,所得有关实验数据记录如下表:
| | 第1次 | 第2次 | 第3次 |
| 所取式样的质量(g) | 17.4 | 17.4 | 17.4 |
| 所取稀盐酸的质量(g) | 80 | 100 | 125 |
| 生成CO2的质量(g) | 2.64 | 4.4 | 4.4 |
(1)在第次实验中,反应容器内有白色固体剩余;
(2)求原试样中Ca(OH)2的质量分数(计算结果精确至0.1%)
(3)经测知,第2次实验反应完全后,所得溶液中溶质只有一种,通过计算求出实验所取稀盐酸中溶质的质量分数为多少?(计算结果精确至0.1%)
(4)已知20℃时,Ca(OH)2饱和溶液溶质的质量分数为0.17%,求20℃时Ca(OH)2的溶解度.
-
长期使用的保温瓶胆内壁有一层水垢,主要成分是CaCO3和Mg(OH)2. 厉山中学马立同学设计了如下实验测定水垢中CaCO3的含量:取1 00g水垢,加入过量的稀盐酸,同时测定5分钟内生成气体的质量,结果如下表:
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 15 | 25 | 30 | 33 | 33 |
试问:
(1)4分钟后,反应停止.此时,固体水垢______ (填“消失“或“部分消失”);
(2)请你简要说明,计算100g水垢中含CaCO3质量的解题思路.
-
某科学兴趣小组的同学在学习了空气中氧气含量的测定的基础上,改进了教材中的实验,设计出了如图所示的实验装置。实验步骤如下:
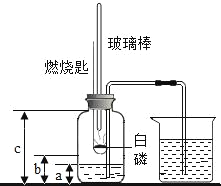
①连接仪器,检查装置气密性,发现装置气密性良好。
②在集气瓶里装进适量a体积的水,燃烧匙里放一小块白磷,在酒精灯上把玻璃棒下端加热,按图示把集气瓶中的空气密封起来,把集气瓶内的长导管伸到瓶底,长导管的另一端放入盛有足量水的烧杯中。
③把预先加热过的玻璃棒按下与白磷接触,观察到白磷立即着火燃烧产生大量白烟,同时放热。
④待白磷燃烧熄灭后,稍加振荡,白烟消失。
⑤待集气瓶完全冷却到室温,量出集气瓶中水的体积为b,整个集气瓶的体积为c。
⑥根据a、b、c三个数据,计算出空气中氧气的体积分数。
根据以上信息,回答下列问题:
(1)在白磷开始燃烧到最后熄灭的过程中,集气瓶内水面的变化情况是_____。
(2)若实验成功,请写出a、b、c三个数据应满足的一个等式关系_____。
(3)小组成员小宇无意间发现步骤⑤集气瓶内的水中滴加几滴石蕊试液,会变红。这一现象使组内成员积极地开展讨论,小玉认为是由于二氧化碳溶于水,使溶液显酸性,但小张马上反对:空气中二氧化碳的含量很少,而实验中又没有产生二氧化碳,短时间内不可能使溶液显酸性。请根据正确的观点,对变红现象提出大胆的猜想:_____。
(4)上述实验中,若集气瓶内的导管没有被液面封住,则导致测量的结果将_____(选填“偏大”、“偏小”或“不变”)。



