-
某同学发现家里的铜质水龙头表面出现了一层绿色的锈渍,经查阅资料,了解到这层锈渍的化学成分是碱式碳酸铜[Cu2(OH)2CO3],并对Cu2(OH)2CO3受热完全分解后的产物进行探究。
(查阅资料)(1)碱式碳酸铜受热分解生成水蒸气、二氧化碳和一种黑色固体。
(2)白色无水硫酸铜遇水变成蓝色。
(提出猜想)该同学根据碱式碳酸铜的化学式对黑色固体产物作出以下猜想:
①可能是碳;
②可能是氧化铜;
③可能是碳和氧化铜的混合物。
他猜想的依据是_____,且碳和氧化铜都是黑色的。
(实验探究)实验Ⅰ:按下图进行实验,证明分解产物中有H2O和CO2(图中夹持装置省略)。
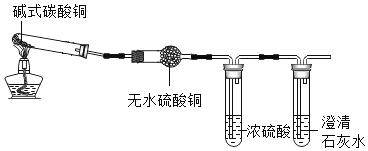
实验Ⅱ:为验证猜想,他做了如下实验:向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,待完全反应后静置,观察现象。
(实验分析及结论)
实验Ⅰ中:证明产物中有水生成的依据是_____;澄清石灰水变浑浊,产物中有_____生成。
实验Ⅱ中:因为黑色粉末溶逐渐消失且_____,所以猜想②正确,故碱式碳酸铜受热分解的化学方程式为_____。
通过上述实验及结论分析可知,铜质水龙头生锈过程中与水、二氧化碳、_____有关。
(实验反思)为了防止铜质水龙头生锈,通常可采取的有效措施是_____。
(拓展应用)依据碱式碳酸铜受热分解的产物及所学酸碱盐的知识,该同学认为可以用稀盐酸除去铜质水龙头表面的锈渍,反应的化学方程式为_____。
-
某同学发现家里的铜质水龙头表面出现了一层绿色的锈渍,经查阅资料,了解到这层锈渍的化学成分是碱式碳酸铜[Cu2(OH)2CO3],并对Cu2(OH)2CO3受热完全分解后的产物进行探究。
(查阅资料)(1)碱式碳酸铜受热分解生成水蒸气、二氧化碳和一种黑色固体。
(2)白色无水硫酸铜遇水变成蓝色。
(提出猜想)该同学根据碱式碳酸铜的化学式对黑色固体产物作出以下猜想:
①可能是碳 ②可能是氧化铜 ③可能是碳和氧化铜的混合物。
他猜想的依据是___________,且碳和氧化铜都是黑色的。
(实验探究)实验Ⅰ:按下图进行实验,证明分解产物中有H2O和CO2(图中夹持装置省略)
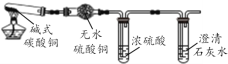
实验Ⅱ:为验证猜想,他做了如下实验:向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,待完全反应后静置,观察现象。
(实验分析及结论)
实验Ⅰ中:证明产物中有水生成的依据是_____________;澄清石灰水变浑浊,产物中有_____生成。
实验Ⅱ中:因为_____________且溶液变成蓝色,所以猜想②正确,故碱式碳酸铜受热分解的化学方程式为___________。
通过上述实验及结论分析可知,铜质水龙头生锈过程中与水、二氧化碳、______________有关。
(实验反思)为了防止铜质水龙头生锈,通常可采取的有效措施是________________。
(拓展应用)依据碱式碳酸铜受热分解的产物及所学酸碱盐的知识,该同学认为可以用稀盐酸除去铜质水龙头表面的锈渍,反应的化学方程式为______________。
-
某同学发现家里用的铜质水龙头表面出现了一层绿色的锈渍。经查阅资料,锈渍的化学成分是碱式碳酸铜 〔Cu2(OH)2CO3〕。根据质量守恒定律,铜生锈肯定与空气中的__________有关,还可能与另一种气体有关,但需进行实验探究才能最终确定。
-
小明发现铜质水龙头表面出现了一层绿色物质,小鹏和同学们特别好奇,决定对该绿色物质进行探究。
[查阅资料]铜长期暴露在潮湿的空气中会生锈,表面有绿色物质生成,俗称铜绿,主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3。
探究一:铜在什么条件下会生锈
[提出猜想]同学们对空气中参与铜生锈的物质提出以下猜想:
猜想①:O2
猜想②:H2O
猜想③:N2
[交流讨论]经过讨论后,同学们一致认为猜想______________不合理,请解释理由_____________。
[拓展提升]除上述猜想外,你认为参与铜生锈的物质可能还有_____________。
探究二:铜绿的化学性质
[实验1]小芳同学取一定量干燥的铜绿放在试管中隔绝空气加热,如图所示。一段时间后,观察到绿色粉末逐渐变成黑色,试管口有无色液滴生成,且烧杯中的澄清石灰水变浑浊;请你用化学方程式解释澄清石灰水变浑浊的原因_______________。
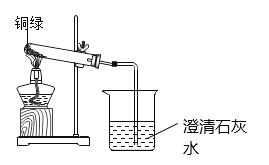
[实验2]小华同学另取一定量的铜绿于试管中,加入适量的稀盐酸,可观察到的现象是________________。
[得出结论]根据小芳、小华同学的实验,同学们总结出铜绿的化学性质为:①铜绿受热易分解;②铜绿能与稀盐酸反应。
[反思交流]同学们从安全角度考虑,认为小芳同学在结束实验1时,应该进行的操作是_______________。
[拓展应用]①小明发现不同地点收集的两个铜器(一个是纯铜做的,一个是表铜做的),纯铜器的铜绿比青铜器的少,他据此分析铜比纯铜易锈蚀,小明的分析是否全面?请你说明理由_______________。
②日常生活中为防止铜制品、铁制品的生锈,应保持其表面洁净和干燥;在金属表面涂保护层;镀一层不易生锈的金属;改变金属的组成和结构。
-
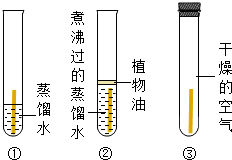
(2011•青岛)甲、乙两位同学发现铜质眼镜架上出现一些绿色的锈渍.经查阅资料得知,铜锈的化学成分是碱式碳酸铜[Cu2(OH)2CO3].他们依照钢铁生锈的研究方法设计如下实验(如右图所示):①将光亮铜片部分浸入蒸馏水中;②将光亮铜片究全浸入煮沸过的蒸馏水中;③将光亮铜片放在干燥的空气中.请回答:
(1)推测一段时间后会出现铜锈的是______ (填写序号)试管内的铜片.
(2)根据上述实验.甲同学认为:铜的锈蚀是铜与水、氧气共同作用的结果.你是否同意他的观点?______ (填写“是”或“否”)
(3)乙同学认为要弄清导致铜锈蚀的因索,还应该再补充一些实验.在补充的实验中,如果要改变的因素______.则保持不变的因素是______(选取“水”、“氧气”、“二氧化碳”等填写)

-
甲、乙两位同学发现铜质眼镜架上出现一些绿色的锈渍.经查阅资料得知,铜锈的化学成分是碱式碳酸铜[Cu2(OH)2CO3].他们依照钢铁生锈的研究方法设计如下实验(如图1所示):①将光亮铜片部分浸入蒸馏水中;②将光亮铜片完全浸入煮沸过的蒸馏水中;③将光亮铜片放在干燥的空气中.请回答:
(1)推测一段时间后会出现铜锈的是:________(填序号)试管内铜片.
(2)根据上述实验,甲同学认为:铜的锈蚀是铜与水、氧气共同作用的结果.乙同学不同意甲同学的观点,欲弄清导致铜锈蚀的因素,他根据铜锈的成分设计了图2实验,请帮他在横线上分别写出B、C、D三只试管中应加入的物质的化学式:

(3)请你帮两位同学想一个防止铜质眼镜框生锈的原理:________.
-
甲、乙两位同学发现铜质眼镜架上出现一些绿色的锈渍.经查阅资料得知,铜锈的化学成分是碱式碳酸铜[Cu2(OH)2CO3].他们依照钢铁生锈的研究方法设计如下实验(如右图所示):①将光亮铜片部分浸入蒸馏水中;②将光亮铜片究全浸入煮沸过的蒸馏水中;③将光亮铜片放在干燥的空气中.请回答:
(1)推测一段时间后会出现铜锈的是______ (填写序号)试管内的铜片
(2)根据上述实验.甲同学认为:铜的锈蚀是铜与水、氧气共同作用的结果.你是否同意他的观点?______ (填写“是”或“否”)
(3)乙同学认为要弄清导致铜锈蚀的因索,还应该再补充一些实验.在补充的实验中,如果要改变的因素______.则保持不变的因素是______(选取“水”、“氧气”、“二氧化碳”等填写)
(4)通过此探究实验,我得到的启示是______.
-
甲、乙两位同学发现铜质眼镜架上出现一些绿色的锈渍.经查阅资料得知,铜锈的化学成分是碱式碳酸铜[Cu2(OH)2CO3].他们依照钢铁生锈的研究方法设计如下实验(如右图所示):①将光亮铜片部分浸入蒸馏水中;②将光亮铜片究全浸入煮沸过的蒸馏水中;③将光亮铜片放在干燥的空气中.请回答:
(1)推测一段时间后会出现铜锈的是______ (填写序号)试管内的铜片.
(2)根据上述实验.甲同学认为:铜的锈蚀是铜与水、氧气共同作用的结果.你是否同意他的观点?______ (填写“是”或“否”)
(3)乙同学认为要弄清导致铜锈蚀的因索,还应该再补充一些实验.在补充的实验中,如果要改变的因素______.则保持不变的因素是______(选取“水”、“氧气”、“二氧化碳”等填写)
-
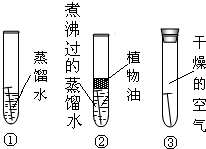
甲、乙两位同学发现铜质眼镜架上出现一些绿色的锈渍.经查阅资料得知,铜锈的化学成分是碱式碳酸铜[Cu2(OH)2CO3].他们依照钢铁生锈的研究方法设计如下实验(如右图所示):①将光亮铜片部分浸入蒸馏水中;②将光亮铜片究全浸入煮沸过的蒸馏水中;③将光亮铜片放在干燥的空气中.请回答:
(1)推测一段时间后会出现铜锈的是______ (填写序号)试管内的铜片.
(2)根据上述实验.甲同学认为:铜的锈蚀是铜与水、氧气共同作用的结果.你是否同意他的观点?______ (填写“是”或“否”)
(3)乙同学认为要弄清导致铜锈蚀的因索,还应该再补充一些实验.在补充的实验中,如果要改变的因素______.则保持不变的因素是______(选取“水”、“氧气”、“二氧化碳”等填写)
-
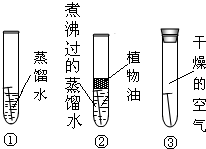
甲、乙两位同学发现铜质眼镜架上出现一些绿色的锈渍。经查阅资料得知,铜锈的化学成分是碱式碳酸铜[Cu2(OH)2CO3]。他们依照钢铁生锈的研究方法设计如下实验(如右图所示):①将光亮铜片部分浸入蒸馏水中;②将光亮铜片究全浸入煮沸过的蒸馏水中;③将光亮铜片放在干燥的空气中。请回答:
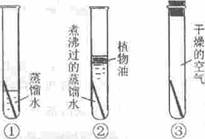
(1)推测一段时间后会出现铜锈的是________ (填写序号)试管内的铜片。
(2)根据上述实验.甲同学认为:铜的锈蚀是铜与水、氧气共同作用的结果。你是否同意他的观点?________ (填写“是”或“否”)
(3)乙同学认为要弄清导致铜锈蚀的因素,还应该再补充一些实验。在补充的实验中,如果要改变的因素________.则保持不变的因素是________(选取“水”、“氧气”、“二氧化碳”等填写)








