-
现化学实验小组要提纯含有CaCl2、 Na2SO4、MgCl2及泥沙等杂质的粗盐,将粗盐溶于适量水中,再按以下流程进行处理:①加过量的NaOH溶液;②加过量的BaCl2溶液;③加过量的Na2CO3溶液;④过滤;⑤加适量的盐酸;⑥蒸发、结晶,得到精盐。
(1)请写出③加过量的Na2CO3溶液后发生的化学方程式。_____(写出一个即可)
(2)⑥中蒸发时玻璃棒的作用是什么_____?
(3)通过操作④所得溶液中的溶质有哪些?_____(用化学式表示)
九年级化学流程题中等难度题查看答案及解析
-
某同学要提纯含有CaCl2、MgSO4及泥沙等杂质的粗盐,将粗盐溶于适量水中,再按以下流程进行处理:
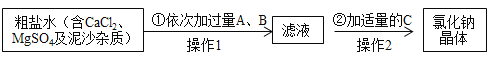
(1)写出加入试剂A时反应的化学方程式____。
(2)若未进行操作1而直接加入试剂C,对提纯结果有影响,为什么?____
(3)操作1后所得滤液中除了氯化钠还含有哪些溶质,请设计实验验证。_____(写出简单操作、现象和结论)
九年级化学推断题中等难度题查看答案及解析
-
(6分)某化学兴趣小组查阅资料得知,粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了将粗盐提纯,设计了以下操作流程:
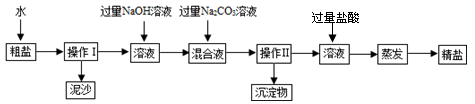
请你根据以上信息回答下述问题:
(1)操作Ⅰ的名称为_______________。
(2)加入过量氢氧化钠溶液,发生化学反应的方程式为 。
(3)加入过量碳酸钠溶液的实验目的是 。
经过操作Ⅱ所得溶液中含有的阴离子是 。
过滤
(4)某同学所得精盐比其他同学明显要多,原因可能是__________。AB
_______ ____
A.滤纸破损,滤液浑浊就蒸发
B.蒸发时未用玻璃棒,有一些液体溅出
C.提纯后所得精盐尚未完全干燥
D.溶解时水的量太少,使食盐未完全溶解
九年级化学填空题困难题查看答案及解析
-
某粗盐样品中除含有泥沙等不溶性固体杂质外,还含有少量MgCl2、CaCl2、Na2SO4三种可溶性杂质,我校初三化学兴趣小组的同学在实验室完成的对粗盐提纯的实验,流程如图所示:
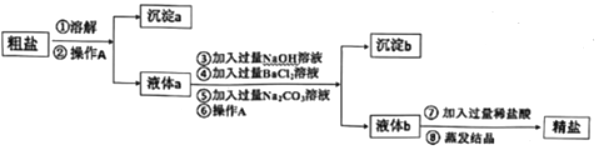
(1)操作A的名称是_____;
(2)步骤⑧蒸发结晶时,玻璃棒的作用是_____;
(3)若将步骤④和步骤⑤交换,所得的精盐中可能混有的杂质为_____(填化学式)。
九年级化学流程题困难题查看答案及解析
-
从海水中得到的粗盐中往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。实验室粗盐提纯的部分流程如图,有关该流程说法错误的是()
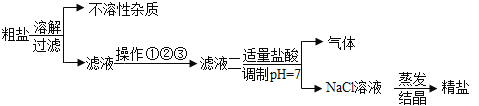
A.不溶性杂质主要是泥沙
B.过滤时要用玻璃棒引流
C.蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
D.操作①②③依次加入的试剂可以为Na2CO3溶液、NaOH溶液、BaCl2溶液。
九年级化学单选题中等难度题查看答案及解析
-
从海水中得到的粗盐中往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。实验室粗盐提纯的部分流程如图,有关该流程说法错误的是()
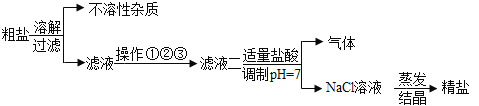
A.不溶性杂质主要是泥沙
B.过滤时要用玻璃棒引流
C.蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
D.操作①②③依次加入的试剂可以为Na2CO3溶液、NaOH溶液、BaCl2溶液。
九年级化学单选题中等难度题查看答案及解析
-
潍坊海水资源丰富,从海水得到的粗盐往往含有可溶性杂质(MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活。实验室模拟工业粗盐提纯的流程如图,请回答:
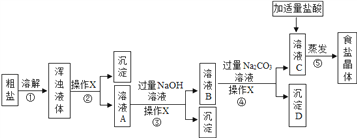
(1)操作X的名称是_____,该操作中用到的玻璃仪器有烧杯、玻璃棒和______。
(2)加适量盐酸的目的是____________________________________________。
(3)生成沉淀D的化学方程式为_____________________________ 。
(4)下图为氯化钠、碳酸钠在水中的溶解度曲线。 请回答下列问题。
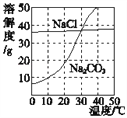
①30℃时,将等质量的两种物质的饱和溶液同时降温至10℃,晶体析出后所得氯化钠溶液的溶质质量分数___(填“>”“<”或“=”)碳酸钠溶液的溶质质量分数。
②在20℃时,各取NaCl、Na2CO3固体30g,分别加入100g水,充分溶解后达到饱和状态的物质是_____。
九年级化学流程题困难题查看答案及解析
-
潍坊海水资源丰富,从海水得到的粗盐往往含有可溶性杂质(MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活。实验室模拟工业粗盐提纯的流程如图,请回答:
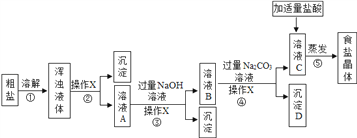
(1)操作X的名称是_____,该操作中用到的玻璃仪器有烧杯、玻璃棒和______。
(2)加适量盐酸的目的是____________________________________________。
(3)生成沉淀D的化学方程式为_____________________________ 。
(4)下图为氯化钠、碳酸钠在水中的溶解度曲线。 请回答下列问题。
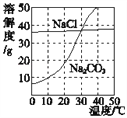
①30℃时,将等质量的两种物质的饱和溶液同时降温至10℃,晶体析出后所得氯化钠溶液的溶质质量分数___(填“>”“<”或“=”)碳酸钠溶液的溶质质量分数。
②在20℃时,各取NaCl、Na2CO3固体30g,分别加入100g水,充分溶解后达到饱和状态的物质是_____。
九年级化学流程题困难题查看答案及解析
-
现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4,MgCl2,CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下:
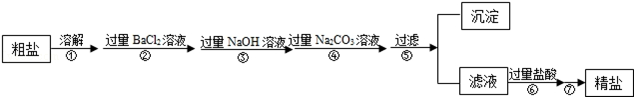
请根据提纯步骤回答下列问题.
(1)步骤⑦的操作名称为________.
(2)请写出实验步骤②中所涉及的化学方程式________.
(3)步骤⑥中加入过量盐酸的目的是________.
(4)步骤②和步骤④________(填“可以”或“不可以”)颠倒,理由是________.
(5)检验步骤④中Na2CO3溶液已过量的方法是________.
(6)加碘食盐相关信息如图所示.
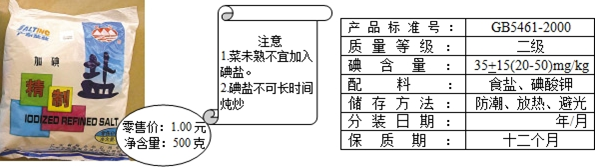
食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),化学方程式如下:
KIO3+5KI+6HCl=6KCI+3I2+3H2O
①向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘化钾,则加入食盐后的实验现象________.
②小强同学欲测定加碘盐中碘元素的质量分数,实验步骤如下:取10g食盐样品于试管中加水溶解,加入过量KI的和淀粉混合溶液,再滴入稀盐酸将溶液酸化使其充分反应后,调节溶液呈中性,再向试管中滴加硫代硫酸钠溶液(Na2S2O3),发生化学反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI
当加入质量分数为0.237%Na2S2O3溶液2g时,I2恰好反应完全,通过计算判断该食盐样品是否合格(已知Na2S2O3的相对分子质量为158.请写出计算过程).
九年级化学计算题中等难度题查看答案及解析
-
现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4,MgCl2,CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下:
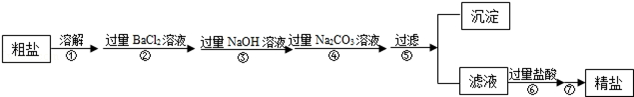
请根据提纯步骤回答下列问题.
(1)步骤⑦的操作名称为________.
(2)请写出实验步骤②中所涉及的化学方程式________.
(3)步骤⑥中加入过量盐酸的目的是________.
(4)步骤②和步骤④________(填“可以”或“不可以”)颠倒,理由是________.
(5)检验步骤④中Na2CO3溶液已过量的方法是________.
(6)加碘食盐相关信息如图所示.
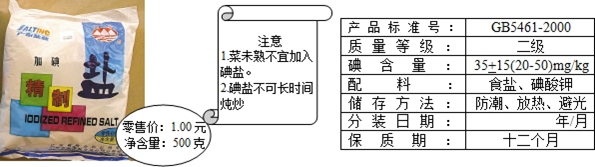
食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),化学方程式如下:
KIO3+5KI+6HCl=6KCI+3I2+3H2O
①向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘化钾,则加入食盐后的实验现象________.
②小强同学欲测定加碘盐中碘元素的质量分数,实验步骤如下:取10g食盐样品于试管中加水溶解,加入过量KI的和淀粉混合溶液,再滴入稀盐酸将溶液酸化使其充分反应后,调节溶液呈中性,再向试管中滴加硫代硫酸钠溶液(Na2S2O3),发生化学反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI
当加入质量分数为0.237%Na2S2O3溶液2g时,I2恰好反应完全,通过计算判断该食盐样品是否合格(已知Na2S2O3的相对分子质量为158.请写出计算过程).
九年级化学计算题中等难度题查看答案及解析