-
金属材料广泛应用于生产生活中,回答下列问题。

(1)如图所示探究铁生锈的条件(每支试管中均放有完全相同的洁净铁钉):
①一段时间后,观察到A、B试管中的铁钉无锈蚀,C试管中铁钉出现锈迹,D试管中的铁钉锈蚀最严重。观察试管________(填字母)发生的现象,可得出铁生锈的条.件是铁与氧气和水共同作用的结果。
②试管D实验的目的是进一步探究铁在_________存在的环境中是否更容易锈蚀。
③铁锈的主要成分是氧化铁,可用稀盐酸除去,其反应原理是________(用化学方程式表示),根据铁钉锈蚀的,原因,提出一条防止铁制品锈蚀的建议________。
(2)合金具有许多特殊性能,合金的硬度一般比各成分金属的硬度________。
(3)将一定质量的铁粉放人硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是________,应后溶液质量________(填“增大”、“减小”或“不变”)。
-
金属材料在国民生产和日常生活中得到普遍广泛的应用
(1)用如图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁片);

①甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,认为必须全面观察试管_______(选填试管编号)发生的现象,并经过科学严谨的推理,才能得出上述结论。B中植物油的作用是_______。
②试管D和E实验的目的是进一步探究铁在_______的环境中是否更容易锈蚀。
(2)黄铜(铜锌合金)用作弹壳的制造。现有一批使用过的,锈迹斑斑的弹壳,处理这批弹壳可以制得硫酸锌和铜,其主要流程如图甲所示:
(收集资料)弹壳上的锈主要为Cu2(OH)2CO3,能与稀硫酸反应得到硫酸铜溶液;弹壳中其他杂质不溶于水,也不参加反应。

甲 乙
①写出弹壳上的锈与稀硫酸反应的化学方程式_______。
②固体D为_______。从微观的角度来看,A与E的反应微观实质是_______。
(3)为了比较甲、乙两种金属的活动性强弱和相对原子质量大小,小昊设计了一套实验装置(如图乙),他取两种金属各m克,分别加入足量的稀硫酸进行反应,在相同条件下测定不同时间内收集到的气体体积,实验记录如表:
| 反应时间(秒) | 20 | 40 | 60 | 80 | 100 | 120 | 140 |
| 收集到的气体体积(毫升) | 甲金属 | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
| 乙金属 | 30 | 75 | 120 | 150 | 150 | 150 | 150 |
①由实验结果可知:金属活动性较强的是_______。实验中,除了要控制两种金属的质量相等,还需要控制的变量有_______。
②为了使得到的实验数据准确,小昊开始收集气体的时间点应该是_______(填字母)
A.导管口一有气泡冒出时 B.冒出气泡连续且均匀时C.检验产生的气体纯净时
③根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,还需知道的数据是_______。
-
金属材料在生产、生活中应用广泛。
(1)由于金属铜具有良好的________,常用于制作导线。
(2)现有如下实验装置(每支试管中均放有完全相同的洁净铁钉):
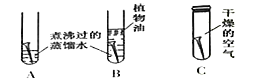
①一段时间后甲同学观察到:_________试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与_________共同作用的结果。
②为防止金属锈蚀,可以采取的措施有______________________(填一种)。
③铁制品中不能盛放稀盐酸的原因,该反应的化学方程式是_________。
-
金属材料在生产、生活中应用广泛。
(1)由于金属铜具有良好的________,常用于制作导线。
(2)现有如下实验装置(每支试管中均放有完全相同的洁净铁钉):
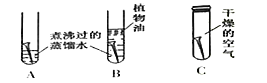
①一段时间后甲同学观察到:_________试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与_________共同作用的结果。
②为防止金属锈蚀,可以采取的措施有______________________(填一种)。
③铁制品中不能盛放稀盐酸的原因,该反应的化学方程式是_________。
-
某化学兴趣小组对金属的性质做了如下探究,请你填写空格:
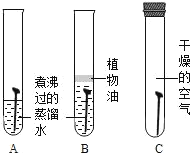
(1)用如图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁片):
①C试管的铁钉未生锈的原因是_____.如向B试管持续几天通入氧气,则产生的现象是_____;
②为防止菜刀生锈,通常的做法是_____;
③为防止轮船外壳生锈,经常在船体外悬挂一块_____.
(2)某同学向分别盛有等质量的铁粉和锌粒的试管中,倒入等质量、等浓度的稀硫酸,以“金属表面产生气泡的快慢”为标准来判断两种金属的活动性强弱.有的同学认为这种方案不够合理,理由是_____.
-
某化学兴趣小组对金属的性质做了如下探究,请你填写空格:
(1)用如图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁钉):

①甲同学认为:试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,认为必须全面观察试管_________(填试管编号)发生的现象,并经过科学严谨的推理,才能得出上述结论。
②试管D和E实验的目的是进一步探究铁在_______的环境中是否更容易锈蚀。
③为防止金属锈蚀,除了采用覆盖保护膜等措施以外,还可以制成合金。这是因为合金与纯金属相比,其组成和内部结构发生变化,从而引起____________的变化。
(2)某同学向分别盛有等质量的铁粉和锌粒的试管中,倒入等质量、等溶质质量分数的稀硫酸,以“金属表面产生气泡的快慢”为标准来判断两种金属的活动性强弱。有的同学认为这种方案不够合理,理由是_________________________________________________________________________。
(3)将一定质量的铁粉放入硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是________,且反应后溶液质量比反应前________(填“增大”“减小”或“不变”)。
-
金属在生产和生活中应用广泛。请回答下列问题。
(1)铁制品广泛应用于生产、生活中。下列不属于铁合金的是________________ (选填字母)。
A 铁锈 B 生铁 C 不锈钢
(2)铁钉生锈可以用稀硫酸除去铁锈,写出化学方程式________________________________。
(3)某化工厂的废液中含有硝酸银、硝酸亚铁和硝酸锌。某同学取适量的上述废液样品,将一定质量的镁粉加入样品中,充分反应后过滤,得到滤液和滤渣。请填空:
①若得到的滤液为浅绿色,则滤液中的溶质一定含有______(填写化学式,下同),可能含有________________________________。
②若得到的滤液为无色,则滤渣中至少含有__________种金属。
-
某化学兴趣小组对金属的性质做了如下探究,请你帮他们完成下面的内容。
(1)探究铁生锈的原因(如下图)(每支试管中均放有完全相同的洁净铁钉):
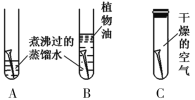
①一段时间后甲同学观察到:______ 试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与______________共同作用的结果。
②为防止金属锈蚀,可以采取的措施有____________(填一种)。
③在焊接铁制品前,常用稀盐酸清除其表面的锈,该反应的化学方程式是______________________。
(2)某同学分别向盛有形状、大小相同的铁片和锌片的试管中,倒入等质量、溶质质量分数相同的稀硫酸,以 “_________________________________”为依据来判断两种金属的活动性强弱。
(3)将一定质量的铁粉放入硫酸铜、硫酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是______,所得滤液中一定含有的溶质是____________________(填化学式)。
-
金属材料在生产、生活中有越来越广泛的用途。请你根据所学知识回答下列问题。
(1)若探据铁钉锈蚀的必要条件,如图所示的实验中没有必要做的实验是_____。
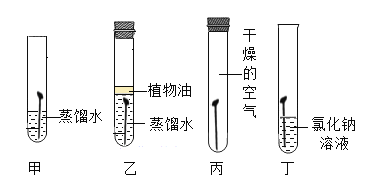
(2)一段时间后,甲、丁中铁钉生锈,且丁铁钉锈蚀最快、最严重,乙、丙无明显现象。
①铁锈属于_____(填“混合物”或“纯净物”)。
②铁生锈的必要条件是____。
③甲、乙中的蒸馏水要预先煮沸,其目的是_____。
④由实验得知氯化钠能加速铁的锈蚀,由此_____(填“能”或“不能”)判断氯化钠可作铁锈蚀的催化剂。
⑤(拓展应用)资料:铜制品生锈可生成铜绿,铜绿的化学式为 Cu2(OH)2CO3。小明作出合理猜想:铜生锈的条件是铜与氧气、水、二氧化碳同时接触。他作出此猜想的依据是:空气的组成以及______。
-
金属具有广泛的应用。请回答:
(1)工业大生产中,炼铁的设备名称是_____。
(2)防止金属锈蚀是保护金属资源的有效途径之一。洁净的铁钉在下列情况下容易生锈的是_____(填字母)。
A 在干燥的空气中 B 在潮湿的空气中 C 浸没在植物油中
(3)铝具有很好的抗腐蚀性能,原因是_____。使用铝制品时要尽量避免与酸性物质接触,铝与稀硫酸反应的化学方程式为_____。
(4)波尔多液是农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。不能用铁质容器配制波尔多液的原因是_____(用化学方程式表示)。
(5)向铁粉和氧化铜粉末的混合物中加入一定量的稀盐酸,充分反应后过滤,得滤渣和滤液。向滤液中加铁片,铁片没有变化。则滤液中含有的溶质是_____(填化学式下同),滤渣中一定含有的物质是_____。








