-
金属在生活、生产中应用广泛。请回答下列问题:
(1)合金比纯金属的利用更广泛,主要原因是_____ (答一点)。
(2)钢铁材料可以通过铁矿石冶炼生产。请写出工业用赤铁矿炼铁的化学方程式_____。
(3)世界上每年因锈蚀而损失的金属数量巨大。金属资源的保护和回收利用成为科学研究中的重大课题。用含较多铁锈的废铁屑制作动物饲料中的添加剂硫酸亚铁晶体的工艺流程如图所示[已知 ]:
]:
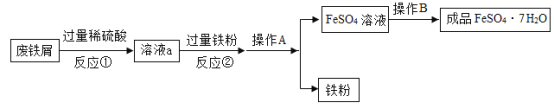
a.操作A的名称是_____。
b.溶液a中的溶质为_____。
c.反应②加入过量铁粉的目的是_____。
-
人类文明进步与金属材料的发展关系十分密切,金属在生活生产中有着非常广泛的应用.请回答下列问题:

(一)铁的广泛应用
(1)钢铁属于 ________(填“纯净物”或“混合物”);
(2)如图为生活中常见“暖贴”的部分标签.暖贴可以贴于身体的某个部位,自行发热,用于取暖或热敷.使用时空气进入暖贴,空气中的氧气、水蒸气与暖贴中的_____发生反应而使暖贴放热.使用后,发现暖贴内有的物质变为红色,该红色固体主要成分的化学式为______.
(二)铁化学性质的探究
将m克Zn和Fe的混合物中加入一定质量的CuCl2溶液,充分反应后过滤,将滤渣洗涤、干燥后称量.质量仍为mg,对所得滤液和滤渣有如下四种判断,以下判断正确的是______.
A.滤液可能是无色
B.滤渣中的物质可能有3种
C.滤液中一定有ZnCl2和FeCl2
D.滤渣中加稀盐酸一定有气泡产生
(三)炼铁过程的探究
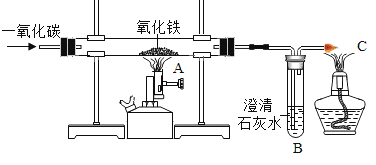
(1)在化学实验室里,可以利用如图装置制得铁:
①在装置B的反应中,实验开始前应先_______(选填“通CO”或“加热”);
②C处酒精灯的作用是__________;
③工业上,高炉炼铁的原料是赤铁矿、焦炭、空气和____;
(2)某铁矿粉,主要成分为铁的氧化物(FeXOy),一学生利用上图实验作进一步分析,过程及数据如下。(注:铁矿粉中杂质不参与下列过程中的反应)
ⅰ.取29g该铁矿粉在CO气流中充分加热,将反应后的气体用烧碱溶液充分吸收,烧碱溶液增重17.6g
ⅱ.将上述加热后的固体取出后,再向固体逐滴加入稀硫酸,测得产生气体与滴入稀硫酸的质量关系如下图:
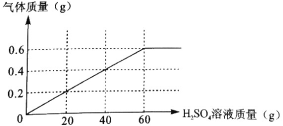
计算该铁的氧化物化学式中,x、y的最简整数比x︰y=______。
-
人类文明进步与金属材料的发展关系十分密切,金属在生活生产中有着非常广泛的应用.请回答下列问题:

(1)铁的广泛应用
①钢铁属于____________ (填“纯净物”或“混合物”);
②如上图为生活中常见“暖贴”的部分标签.暖贴可以贴于身体的某个部位,自行发热,用于取暖或热敷.使用时空气进入暖贴,空气中的氧气、水蒸气与暖贴中的____________ 发生反应而使暖贴放热.使用后,发现暖贴内有的物质变为红色,该红色固体主要成分的化学式为______________。
(2)铁的化学性质探究
将m g Zn和Fe的混合物中加入一定质量的CuCl2溶液,充分反应后过滤,将滤渣洗涤、干燥后称量.质量仍为m g,对所得滤液和滤渣有如下四种判断,以下判断正确的是(____)
A.滤液可能是无色
B.滤渣中的物质可能有3种
C.滤液中一定有ZnCl2和FeCl2
D.滤渣中加稀盐酸一定有气泡产生
(3)炼铁过程的探究
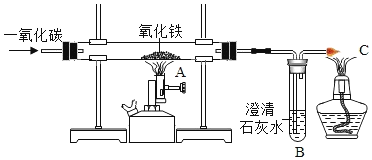
在化学实验室里,可以利用如图装置制得铁:
①写出其反应方程式_____________________________;
②在装置A的反应中,实验开始前应先______________ (选填“通CO”或“加热”);
③C处酒精灯的作用是__________________ 。
-
(5分)金属材料在生活、生产中应用十分广泛。

(1)图A是金属的一个应用实例,利用了金属
的 。
(2)图B是两块金属片相互刻划后,在纯铜片上有明
显的划痕,该实验探究的目的是:比较合金和纯金属
的 。
(3)为比较铁和铜的活动性,小军用稀盐酸进行实验、小华使用硫酸铜溶液进行实验。问:
①小军判断铁比铜活泼的依据是 。
②写出小华能说明铁比铜活泼的化学反应方程式 。
-
金属材料在生活、生产中应用十分广泛.

(1)图 A 是金属的一个应用实例,利用了金属的_______.
(2)图 B 是两块金属片相互刻划后,在纯铜片上有明显的划痕,该实验探究的目的是:比较合金和纯金属的_____.
-
金属在生活、生产中有着非常广泛的应用,请回答下列问题。
(1)铁在潮湿的空气中很容易生锈,请写出一种防止钢铁制品锈蚀的方法_____;
(2)请写出工业用赤铁矿石炼铁的化学方程式:_____。生铁和钢的性能不同,原因是_____;
(3)向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,操作流程如图所示。
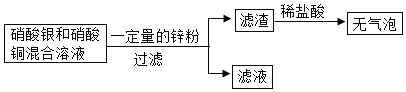
①滤渣中一定含有的物质是_____(填化学式,下同);
②若滤液呈蓝色,滤液中一定含有的溶质是_____,此时不能确定是否发生的反应化学方程式是_____。
-
运用知识节约资源 金属在人类的生产和生活中有广泛的应用。请回答下列问题:
(1)钨丝可用于制造灯泡中的灯丝是利用了该金属____________的性质。 保险丝(铅锑合金)比组成它的纯金属的熔点_____________(选填“低”或“高”)。
(2)如图所示装置是探究铁生锈的实验,实验所用铁片形状、大小相同。请你填写空格:

①一段时间后,试管 A 中铁片生锈,试管 B 和 C 中铁片保持光亮,试管 D 和 E 中铁片生锈都比试管A多。全面观察试管 ABC 发生的现象,推理得出结论:钢铁锈蚀主要是铁与空气中的_____________共同作用的结果。
②对比试管 A、E 所得实验结论是:___________。
③生活中海边比河边的铁制品更容易生锈,从而猜测氯化钠能加快铁的锈蚀。为验证猜想,应做的实验是_______(选填试管编号)。
(3)我国每年报废的手机超过 1 亿部。废旧手机的电路板中含有铜、铁、铝、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。化学小组为回收其中的铜,设计并进行了如下实验。已知: Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。
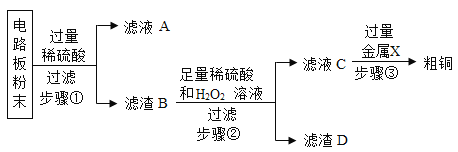
①写出一个步骤①中发生反应的化学方程_____________。
②滤液 A 中的阳离子有_____________(填写离子符号)。
③滤液 C 中一定含有的溶质是_____________。
-
金属在生活生产中有着非常广泛的应用,请回答下列问题:
(1)根据下图的应用实例,写出金属具有的物理性质_________________。(答出一点即可)

(2)生铁和钢的性能不同,原因是____________不同。
(3)铁制品易生锈,为了防止自行车链条生锈常采取的措施是_____________。地球上的金属资源有限,除了防止金属锈蚀以外,我们还可以通过来保护金属资源____________________。(答出一点即可)
-
(6分)金属在生产生活中应用广泛.
(1)下列厨房用品所使用的主要材料,利用金属导热性的是 (填字母序号).

(2)汽车表面喷漆,可以延缓钢铁的锈蚀,其防锈原理是隔绝 .
(3)根据图示中的变化,下列结论正确的是 (填字母序号).
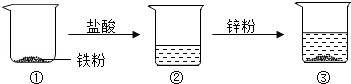
A.烧杯②中溶液含有盐酸 B.烧杯③中一定没有盐酸
C.烧杯③中溶液为氯化锌溶液 D.烧杯③中的固体可能是铁.
-
金属在人类生活和生产中应用越来越广泛。
(1)铝在多个领域替代易生锈的钢铁,其主要原因是_______________
(2)钢铁的冶炼是人类文明的-一个重要标志,下图是实验室模拟炼铁的装置图,回答下列问题。
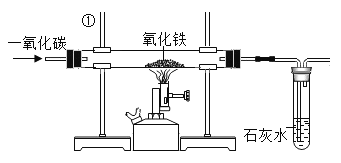
①写出炼铁的化学方程式_________________
②图中仪器①的名称是______________________
③此装置有不完善的地方,请说出其中的一种改进方法____________________
(3)铁制品锈蚀的过程,实际上是铁与空气中的_________(用化学式)等发生化学反应的过程。
(4)许多资源都是不可再生的,每个公民都应树立保护资源的观念,下列做法不利于保护金属资源的是_________(填选项字母)
A.采取各种有效防锈方法避免金属锈蚀。
B.用塑料代替钢和其他合金制造管道。
C.私挖滥采矿物
D.回收利用铝制饮料罐
(5)在实验室里称取10g铜锌合金放入烧杯中,向其中加入100g一定质量分数的稀盐酸,恰好完全反应。反应后称的烧杯中剩余物的总质量为109.8g,求合金中锌的质量__________。
]:













