我国化工先驱侯德榜发明的“侯氏制碱法”利用饱和食盐水依次吸收氨和二氧化碳最终制的碳酸钠等产品,该法的主要反应为“”。下列有关叙述正确的是
A.该方法制得的是火碱
B.析出晶体后,剩余溶液中溶质只有NH4C1
C.配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D.向饱和食盐水中先通入氨气使溶液呈碱性,能促进二氧化碳的吸收
九年级化学单选题中等难度题
我国化工先驱侯德榜发明的“侯氏制碱法”利用饱和食盐水依次吸收氨和二氧化碳最终制的碳酸钠等产品,该法的主要反应为“”。下列有关叙述正确的是
A.该方法制得的是火碱
B.析出晶体后,剩余溶液中溶质只有NH4C1
C.配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D.向饱和食盐水中先通入氨气使溶液呈碱性,能促进二氧化碳的吸收
九年级化学单选题中等难度题
我国化工先驱侯德榜发明的“侯氏制碱法”利用饱和食盐水依次吸收氨和二氧化碳最终制的碳酸钠等产品,该法的主要反应为“”。下列有关叙述正确的是
A.该方法制得的是火碱
B.析出晶体后,剩余溶液中溶质只有NH4C1
C.配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D.向饱和食盐水中先通入氨气使溶液呈碱性,能促进二氧化碳的吸收
九年级化学单选题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
某中学课外活动小组在实验室模拟我国化工专家侯德榜先生发明的“联合制碱法”(即“侯氏制碱法”),其原理是向氨化的饱和氯化钠溶液通入足量的二氧化碳,使溶解度较小的碳酸氢钠从溶液中析出,其反应的化学方程式为:NaCl+CO2+NH3+H2O=NH4CI+NaHCO3。该方法不但可以制得纯碱(将NaHCO3进一步处理即可得到纯碱),还得到优质氮肥氯化氨。
试通过计算回答下列问题:
⑴氯化氨中氮元素的质量分数为 _________(计算结果保留0.1%)
⑵实验中得到碳酸氢钠8.4g,求参加反应的氨气质量为多少?
⑶课外活动小组为了这次模拟实验,准备了8.8g二氧化碳,制取这些二氧化碳需要消耗质量分数为10%的稀盐酸的质量为多少?
九年级化学计算题中等难度题查看答案及解析
我国制碱工业先驱候德榜发明了“候氏制碱法”,其化学原理是利用饱和食盐水与NH3、CO2反应:。下列说法错误的是()
A.物质X的化学式是NH4Cl
B.该反应中各种元素的化合价都不变
C.过滤后,所得溶液中溶质只有X
D.参加反应的H2O和NH3的质量比是18:17
九年级化学单选题中等难度题查看答案及解析
(经典赏析)我国制碱工业的先驱—侯德榜,发明了将制碱与制氨结合起来的联合制碱法。生产过程是在饱和氨盐水中(NH3和NaCl都达到饱和的溶液)通入 CO2。
(查阅资料)(1)侯氏制碱法中主要反应: Ⅰ.NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl, Ⅱ.2NaHCO3 △ Na2CO3+H2O+CO2↑。
(2) NaHCO3和NH4Cl的溶解度曲线如图所示。

(思考交流)(1)30℃时,NH4Cl饱和溶液中溶质质量分数与NaHCO3饱和溶液中溶质质量分数相比,前者与后者的关系是_______(填字母)。
A.大于 B.小于 C.等于 D.无法确定
(2)反应Ⅰ中生成物NaHCO3和NH4Cl的质量比为_______(不需化简)。
(3)氨盐水吸收CO2后生成NaHCO3和NH4Cl,先结晶析出的物质是NaHCO3,原因是________。
(实验探究)某小组以粗盐和碳酸氢铵(NH4HCO3)为原料,采用以下流程制备纯碱和NH4Cl。

(1)粗盐中除了含有泥沙等不溶性杂质,还含有少量的MgCl2等。若要除去粗盐中的MgCl2,可加入过量的NaOH溶液,过滤,然后向滤液中加入适量盐酸。写出加入盐酸时反应的化学方程式_____________。
(2)过滤时玻璃棒的作用是______________ 。
(3)沉淀1表面常附有NH4+、Cl-等杂质,洗涤时最好选用下列______饱和溶液(填字母)。
A.NaCl B.NH4Cl C. NH4HCO3 D.NaHCO3
(4)步骤X包括的操作有________、冷却结晶和过滤。
(拓展延伸)小华设计下图实验装置测定某纯碱样品(含少量杂质NaCl)中碳酸钠的质量分数:取一定量的样品与足量稀盐酸反应,通过测定生成CO2的体积,计算样品中碳酸钠的质量分数。(已知常温常压下CO2的密度是1.977g/L)
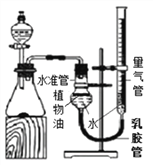
(1)如果样品质量为5.3g,则实验中选用的量气管规格最合适的是_________(填字母)。
A.500mL B.1000 mL C.1500 mL D.2000mL
(2) 反应结束后锥形瓶中有CO2残留,会导致测得的碳酸钠质量分数_________(填字母)。
A.偏大 B.偏小 C.无影响
(3)如果5.3g样品中钠元素的质量分数为42%,实验结束后将锥形瓶中溶液蒸干,则所得固体质量为__________(结果保留1位小数)。
九年级化学综合题困难题查看答案及解析
我国制碱工业先驱侯德榜发明了“侯氏制碱法”。其模拟流程如下:
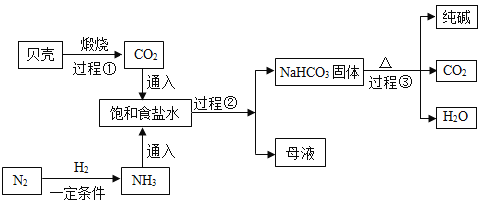
(小资料)
Ⅰ、贝壳的主要成分是CaCO3
Ⅱ、通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳
Ⅲ、饱和食盐水中发生的主要反应为: ( NaHCO3是因为饱和后析出,变成沉淀)。
(1)合成氨需要的氮气来自空气,空气属于_______________(填“混合物”或“纯净物”)。
(2)过程②中主要操作的名称是_______________________。
(3)过程①中发生反应的化学方程式为_______________________。
过程③中反应所属基本反应类型为_______________________。
(4)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入_____________ (填“NH3”或“CO2”),你的理由是:_______________________。
(5)上述流程中可以循环利用的物质是:_______________________。
九年级化学流程题简单题查看答案及解析
我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其模拟流程如下:
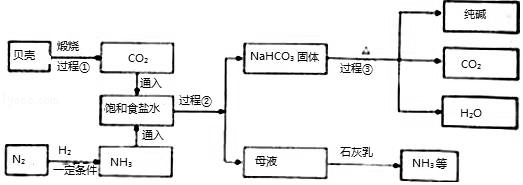
【小资料】
I、贝壳的主要成分是CaCO3
Ⅱ、通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳
Ⅲ、饱和食盐水中发生的主要反应为:NH3+CO2+H2O=NH4HCO3,NH4HCO3+NaCl=NaHCO3↓+NH4Cl
(1)合成氨需要的氮气来自空气,空气属于 (填“混合物”或“纯净物”).空气中氮气的体积分数约为 .
(2)过程②中主要操作的名称是 .
(3)过程①中发生反应的化学方程式为 ,过程③中反应所属基本反应类型为 .
(4)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入 (填“NH3”或“CO2”),你的理由是: .
(5)上述流程中可以循环利用的物质是: (填化学式)
九年级化学填空题中等难度题查看答案及解析
我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其模拟流程如下:

【小资料】
I、贝壳的主要成分是CaCO3
Ⅱ、通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳
Ⅲ、饱和食盐水中发生的主要反应为:NH3+CO2+H2O=NH4HCO3;NH4HCO3+NaCl=NaHCO3↓+NH4Cl
(1)合成氨需要的氮气来自空气,空气属于________(填“混合物”或“纯净物”)。空气中氮气的体积分数约为____。
(2)过程②中主要操作的名称是___,用到的玻璃仪器有玻璃棒、烧杯、_______。
(3)过程①中发生反应的化学方程式为__,过程③中反应所属基本反应类型为___。
(4)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入___(填“NH3”或“CO2”),你的理由是:______________。
(5)上述流程中可以循环利用的物质是:______(填化学式,写一种即可)
九年级化学流程题中等难度题查看答案及解析
我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其模拟流程如下:

【小资料】
I、贝壳的主要成分是CaCO3
Ⅱ、通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳
Ⅲ、饱和食盐水中发生的主要反应为:NH3+CO2+H2O=NH4HCO3,NH4HCO3+NaCl=NaHCO3↓+NH4Cl
(1)合成氨需要的氮气来自空气,空气属于 (填“混合物”或“纯净物”).空气中氮气的体积分数约为 .
(2)过程②中主要操作的名称是 .
(3)过程①中发生反应的化学方程式为 ,过程③中反应所属基本反应类型为 .
(4)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入 (填“NH3”或“CO2”),你的理由是: .
(5)上述流程中可以循环利用的物质是: (填化学式)
九年级化学流程题困难题查看答案及解析
(2011年·衡阳)某中学课外活动小组在实验室模拟我国化工专家侯德榜先生发明的“联合制碱法”(即“侯氏制碱法”),其原理是向氨化的饱和氯化钠溶液通入足量的二氧化碳,使溶解度较小的碳酸氢钠从溶液中析出,其反应的化学方程式为:NaCl+CO2+NH3+H2O=NH4CI+NaHCO3。该方法不但可以制得纯碱(将NaHCO3进一步处理即可得到纯碱),还得到优质氮肥氯化氨。
试通过计算回答下列问题:
⑴氯化氨中氮元素的质量分数为 _________(计算结果保留0.1%)
⑵实验中得到碳酸氢钠8.4g,求参加反应的氨气质量为多少?
⑶课外活动小组为了这次模拟实验,准备了8.8g二氧化碳,制取这些二氧化碳需要消耗质量分数为10%的稀盐酸的质量为多少?
九年级化学填空题中等难度题查看答案及解析