-
“中国制造”“一带一路”等基础建设都需要用到大量钢铁。
(1)认识铁及其应用
①从微观角度看,铁是由____(填化学符号)构成,其在地壳中的含量居所有元素第____位。
②生铁和钢均是生活中常见的金属材料,它们都属于 __(填“纯净物”或“混合物”)。
③铁锅可用以烹饪,利用了铁的_____性。很多人认为:铁锅炒菜过程中会有少量铁进入人体,与胃液中的盐酸反应,请写出铁与稀盐酸反应的化学方程式_____,该反应的基本反应类型为_____,所以用铁锅炒菜能“补铁”,这里的“铁”指______(填“原子”“单质”或“元素”)。
(2)铁的冶炼
某化学实验小组利用下图装置模拟铁的冶炼并测定某赤铁矿石中氧化铁的质量分数(假设赤铁矿中杂质不参与反应)。

①实验开始时,先进行的操作是____(填字母)。
a 通入一氧化碳 b 加热
②实验过程中观察到装置A中玻璃管内发生的现象是______。
③写出B装置发生反应的化学方程式是__________。
④从环境保护的角度看此实验存在的缺陷是__________。
⑤实验前称量赤铁矿石的质量为20g,通入足量一氧化碳充分反应,测得B装置总质量增加13.2 g。若不考虑实验过程中水分带出的影响,则装置C的作用是________;求该赤铁矿石中氧化铁的质量分数______(请写出计算过程)。
(3)铁的防护
①铁制品暴露于潮湿的空气中,易形成铁锈。由于铁锈结构特点是______,故铁制品表面的铁锈应及时清除,用稀盐酸适时浸泡是清除铁锈的方法之一,铁锈的主要成分与盐酸反应的化学方程式为_________。
②家庭使用的铁锅防锈方法有___________。
-
“中国制造”“一带一路”等基础建设都需要用到大量钢铁。
(1)认识铁及其应用
①从微观看,铁是由_____(填化学符号)构成,其在地壳中的含量居所有金属元素第_____位。
②生铁和钢均是生活中常见的铁材料,它们都属于_____(填“纯净物”或“混合物”)。
③生铁可用以铸成铁锅,利用了金属铁的_____性。很多人认为:铁锅炒菜过程中摩擦产生的“铁屑”进入人体后,会与胃液中的盐酸反应,请写出铁与稀盐酸反应的化学方程式_____,该反应的基本反应类型为_____,所以用铁锅炒菜“补铁”,这里的“铁”指_____(填“原子”“单质”或“元素”),实质生成的铁为非血红素铁,人体吸收效果甚微。
(2)铁的冶炼:下图为某钢铁公司的矿石选取、冶铁和炼钢的工艺流程。

①用赤铁矿石冶铁的反应原理是_____(用化学方程式表示)。
②分析工艺流程,三脱装置中发生反应的化学方程式是_____(任写一个)。
③向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,该过程类似于化学实验中的_____操作。
④在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是_____。
(3)铁的防护
①铁制品长期暴露于潮湿的空气中,其表面易形成_____色的铁锈,由于铁绣制品的结构特点是_____,故铁制品表面的铁锈应及时清除。
②请列举一种常见的清除铁锈的方法_____。
③家庭使用的铁锅如何防锈?_____。
-
“中国制造”、“一带一路”的基础建设都需要用到大量钢铁。工业上利用赤铁矿炼钢的流程如下:
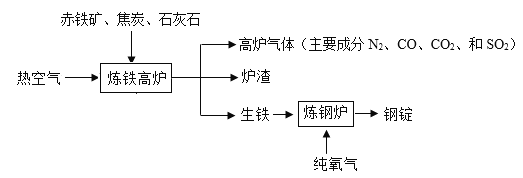
回答下列问题:
(1)炼铁高炉中,一氧化碳与赤铁矿反应制取铁的化学方程式 为_____,“高炉气体”中能形成酸雨的_____(填化学式)。
(2)炼钢炉中通入纯氧的目的是_____,钢锭轧成钢板,体现了金 属的_____性。
(3)生活中铁制品锈蚀现象非常普遍,危害极大。你认为下列措施能防止铁制品锈蚀 的是_____(填字母)。
a涂油、喷漆 b部分浸入食盐水中
c镀耐腐蚀的铬层 d久置于潮湿的空气中
-
“中国制造 “一带一路”的基础建设需要用到大量钢铁。下列有关钢铁的说法正确的是
A.钢是纯净物,生铁是混合物 B.钢的机械性能比生铁优越
C.生铁的熔点比纯铁高 D.生锈的钢铁制品没有回收价值
-
“中国制造”、“一带一路”的基础建设都需要用到大量钢铁,下列有关钢铁的说法正确的是( )
A.钢是纯净物,生铁是混合物
B.钢铁在潮湿的空气中容易生锈
C.生铁的熔点应比纯铁高
D.生锈的钢铁制品没有回收价值
-
“中国制造”、“一带一路”的基础建设都需要用到大量金属材料。下列有关金属材料的说法正确的是:
A.黄铜片比铜片硬度小
B.多数合金的熔点低于组成它的纯金属
C.生锈的钢铁制品没有回收价值
D.合金中一定不含有非金属
-
“中国制造”“一带一路”的基础建设都需要用到大量金属材料。下列有关金属材料的说法正确的是
A.黄铜片比铜片硬度小
B.合金中一定不含有非金属
C.生锈的钢铁制品没有回收价值
D.多数合金的熔点低于组成它的成分金属
-
目前,我国钢铁产量居世界第一,为国民经济的发展奠定了坚实的基础。
(一)铁的广泛应用
(1)认识铁:从宏观看,铁由______组成;从微观看,铁由_________构成。我国在西汉时期就有“曾青得铁则化为铜”之说,其化学方程式是______________________。
(2)生活中:右图是常用的铁锅。用铁锅做炊具,是利用了铁的___________性。防止铁锅生锈,通常采用的方法是____________。

(3)实验室:铁丝在纯净氧气中燃烧的化学反应方程式为__________。铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是___________(填化学式)。
(二)铁锈蚀的条件探究
(4)铁在潮湿的空气里容易发生锈蚀,证明水一定参加了反应,必须要做的对比实验是_______(填字母)。
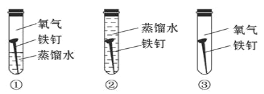
A.①② B.①③ C.②③ D.①②③
(5)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性强的金属首先被腐蚀。造船工业为了避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的是_____(填“锌块”或“铜块”)。
(6)如图所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进广口瓶(容积为150mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如下表。(滤纸包等所占体积忽略不计)
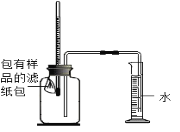
| 序号 | 样品 | 量筒起始读数 | 量筒最终读数 | 所需时间/min |
| 1 | 1g铁粉、0.2 g碳和10滴水 | 100 mL | 72 mL | 约120 |
| 2 | 1g铁粉、0.2g碳、10滴水和少量NaCl | 100 mL | 72 mL | 约70 |
| 3 | | / | / | / |
①铁锈的主要成分是______(写化学式)。
②实验1和2说明NaCl可以_______(填“加快”或“减慢”)铁锈蚀的速率。
③实验开始后广口瓶内温度上升,说明铁锈蚀过程是______(填“放热”或“吸热”)过程。④实验1和3是探究碳对铁锈蚀速率的影响,表格空白处应填写的实验3的样品组成是________。
⑤该装置还可用于测量空气中氧气的体积分数。根据上述数据计算氧气的体积含量是________%(精确到小数点后1位)。
(三)铁的冶炼
(7)某钢铁厂炼铁的主要原料是焦炭、赤铁矿(主要成分为氧化铁)、石灰石等,炼铁设备--高炉结构如图所示,请回答下列问题:
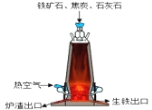
①炼铁的固体原料需预先经过粉碎,其目的是___________。
②炼铁高炉内发生的主要过程如下:
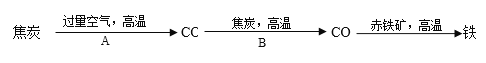
写出步骤写出A、B两步反应的化学方程式:
A:_____________,B:________________
③资料显示,炼铁中焦炭的实际用量远高于理论值,可能原因是______(填字母)。
A.部分焦炭与铁相互熔合,成为生铁中的部分碳元素
B.焦炭转变成一氧化碳后,并不能全部参加反应
C.焦炭在高温下会分解
④某炼铁厂现用100t含氧化铁80%的赤铁矿石炼铁,计算理论上可以炼出含铁96%的生铁的质量__________。(计算结果精确到0.1t)
-
从微观角度认识化学,是学好化学的基础。
(1)构成物质的微粒有分子、原子和_____。
(2)构成氯化钠的微粒是_____、_____(填化学符号)。
(3)请你从原子的角度解释质量守恒定律:_____。
(4)从Na、Mg原子结构示意图推知,金属Na,Mg化学性质不同的原因是_____。
(5)X2﹣与Ne的核外电子排布相同,则X的元素符号是_____。
-
从微观角度认识物质,是学好化学的基础.
(1)构成物质的微粒有分子、原子和________.构成氯化钠的微粒是________(填化学符号).
(2)如图 中表示化合物的是_____(填字母序号).用化学用语表示图
中表示化合物的是_____(填字母序号).用化学用语表示图 :________,图
:________,图 :________,图
:________,图 :________.
:________.

(3)在玻璃杯中加入 水,向水中加入一块冰糖,在杯子的外壁沿液面划一条水平线,过一会儿发现糖块消失了,液面比原来水平线降低了,请通过这一现象,推测分子具有的性质:①____;②___.
水,向水中加入一块冰糖,在杯子的外壁沿液面划一条水平线,过一会儿发现糖块消失了,液面比原来水平线降低了,请通过这一现象,推测分子具有的性质:①____;②___.
(4)用“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,若它们构成的分子在一定条件下发生如图
”表示氧原子,若它们构成的分子在一定条件下发生如图 所示的变化.
所示的变化.
①下列关于该反应的说法中,不正确的是_____(填字母序号)
 .有氧化物生成
.有氧化物生成
 .反应前后各种微粒的数目均煤油改变
.反应前后各种微粒的数目均煤油改变
 .原子是化学反应中的最小微粒
.原子是化学反应中的最小微粒
 .这是一个分解反应
.这是一个分解反应
②从图中你还能获得的微观信息是_____(答出一点即可).








