-
我国制碱工业先驱——侯德榜先生发明了“侯氏制碱法”,其主要的化学原理如下: ;
;
工业上以半水煤气(主要成分是N2、H2、CO、CO2和H2O)、食盐等为原料制取纯碱的流程见图1。
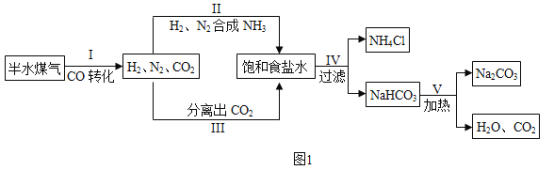
(1)X的化学式为___________,流程中循环利用的物质有H2O和____________。
(2)实验室从混合气体H2、N2、CO2中分离出CO2的实验装置如图2所示。打开k1,关闭k2时,吸收CO2;打开k2,关闭k1时,产生CO2,则广口瓶和分液漏斗中盛放的药品分别是(用化学式表示其溶质)_____________、____________。
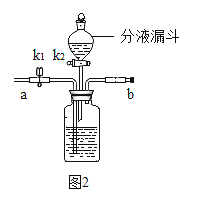
(3)将Na2CO3和NaHCO3的混合物10g充分加热,将生成的气体用浓硫酸充分干燥后,再用澄清石灰水除去剩余气体,至固体混合物的质量不再改变时,称得澄清石灰水的装置增重2.2g。则原混合物中Na2CO3的质量分数是______。
-
侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展做出了杰出贡献。工业上以半水煤气(主要成分是N2、H2、CO2)、食盐等为原料制取纯碱,相关流程如下:
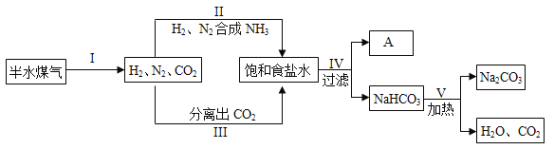
(1)流程中循环利用的物质有H2O和_____(写化学式)。
(2)请写出步骤Ⅴ中的化学反应方程式_____。
(3)已知A为铵态氮肥,请推断该物质为_____(写化学式)。
(4)侯氏制碱法制取纯碱过程中部分物质的溶解度曲线如下,试回答下列问题:
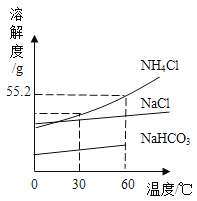
①60℃时,27.6gNH4Cl完全溶解至少需要_____g水。
②从图中可以看出温度高于60℃,NaHCO3的溶解度曲线“消失”了,原因是_____。
③结合上述化学反应方程式和物质的溶解度曲线回答,在氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵中,先结晶析出的物质是_____(填物质名称)。
-
侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。工业上以半水煤气(主要成分是N2、H2、CO、CO2和H2O)、食盐等为原料制取纯碱的流程如下:
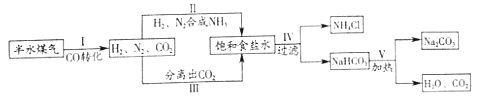
(1)流程中循环利用的物质有H2O和_____。
(2)步骤Ⅰ中,在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应实现了CO转化,化学方程式是_____。
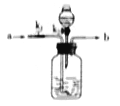
(3)实验室从混合气体H2、N2、CO2中分离出CO2的实验装置如图所示。广口瓶和分液瀾斗中盛放的药品分别是_____、_____。
(4)除去纯碱中少量碳酸氢钠杂质的方法是_____。
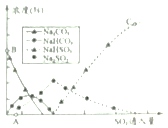
(5)纯碱用途广泛。工业上可用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3,达到减少污染、节约资源的目的。反应过程中溶液组成变化如图2所示。
①吸收初期(图中3A点以前)反应的化学方程式为_____。
②不断通入SO2,最终产物是_____。
-
我国制碱工业先驱侯德榜发明了“侯氏制碱法”,促进了世界制碱技术的发展。其主要化学反应原理如下:
NH3+CO2+H2O═NH4HCO3①
NaCl+NH4HCO3═NaHCO3↓+NH4Cl ②
x NaHCO3 Na2CO3+CO2↑+H2O ③
Na2CO3+CO2↑+H2O ③
已知NaCl、NaHCO3和NH4Cl在不同温度下的溶解度数据如下表:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 |
请回答下列问题:
(1)反应①的基本反应类型属于_____反应。
(2)反应②产生的NH4Cl在农业生产中常用作_____(选填“氮肥”、“磷肥”或“钾肥”)。
(3)反应③中的化学计量数x=_____。
(4)20℃时,反应②中的生成物溶解度较小的是_____(填化学式)
(5)20℃时,将NaCl和NaHCO3的饱和溶液各100g,分别加热蒸发20g水,再恢复至原温度,析出晶体并得到溶液,对于所得溶液下列说法正确的是_____(填序号)
A、所得溶液仍是饱和溶液
B、所得溶液的质量前者大于后者
C、所得溶液的溶质质量分数都增大
-
1921年,我国制碱工业先驱——侯德榜先生发明了侯氏制碱法:先制得NaHCO3,再利用碳酸氢钠受热分解得到纯碱,此步骤的化学方程式为_____;1915年,我国女科学家屠呦呦研究青蒿素(C15H22O5)而获得诺贝尔奖,青蒿素完全燃烧的化学方程式为_____
-
我国制碱工业先驱侯德榜先生发明了联合制碱法,其中一个化学反应的化学方程式为:2NaHCO3
 Na2CO3+X+H2O,则X的化学式为( )
Na2CO3+X+H2O,则X的化学式为( )
A.CO2
B.CO
C.O2
D.CH4
-
我国制碱工业先驱侯德榜先生发明了“侯氏制碱法”,其模拟流程如图所示:
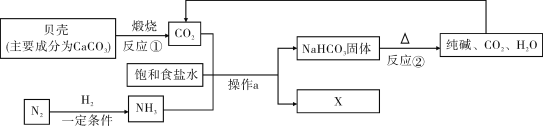
(1)操作a的名称是________。
(2)X是一种可用作氮肥的盐,其化学式可能是______________。
(3)流程图中可循环利用的物质是__________________。
-
我国制碱工业先驱侯德榜先生发明了联合制碱法,其中一个化学反应的化学方程式为:2 NaHCO3  Na2CO3 + X +H2O ,则X的化学式为
Na2CO3 + X +H2O ,则X的化学式为
A.CO2 B.CO C.O2 D.CH4
-
我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其模拟流程如下:

(小资料)
I、贝壳的主要成分是 CaCO3
Ⅱ、通常情况下,1 体积水中大约能溶解 700 体积氨气,1 体积水中大约能溶解 1 体积二氧 化碳
Ⅲ、饱和食盐水中发生的主要反应为: NH3+CO2+H2O=NH4HCO3, NH4HCO3+NaCl=NaHCO3↓+NH4Cl(NaHCO3 是因为饱和后析出,变成沉淀)。
(1)合成氨需要的氮气来自空气,空气属于______填“混合物”或“纯净物”).空 气中氮气的体积分数约为_____。
(2)过程②中主要操作的名称是_____。
(3)过程①中发生反应的化学方程式为 _____,过程③中反应所属基本反应基本类型为__________。
(4)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入_____(填“NH3” 或“CO2”),你的理由是:_____。
(5)上述流程中可以循环利用的物质是:_____(填化学式)。
-
我国制碱工业先驱侯德榜发明了“侯氏制碱法”,其模拟流程如下:

【小资料】
Ⅰ.贝壳的主要成分是CaCO3。
Ⅱ.通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳。
Ⅲ.饱和食盐水中发生的主要反应为:NH3+CO2+H2O===NH4HCO3,NH4HCO3+NaCl===NaHCO3↓+NH4Cl。
(1)过程②中主要操作的名称是________。
(2)过程①中发生反应的化学方程式为________________________________,过程③中反应所属基本反应类型为____________。
(3)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入________(填“NH3”或“CO2”),你的理由是________________________________________________________________。
(4)上述流程中可以循环利用的物质是________(填化学式)。
;









