某反应: ,则X的化学式是
A.SO2 B.H2 C.H2O D.H2SO3
九年级化学单选题简单题
某反应: ,则X的化学式是
A.SO2 B.H2 C.H2O D.H2SO3
九年级化学单选题简单题
某反应: ,则X的化学式是
A.SO2 B.H2 C.H2O D.H2SO3
九年级化学单选题简单题查看答案及解析
| A.SO2+H2O=H2SO3 | B.Cl2+2KI=2KCl+I2 |
| C.H2CO3=H2O+CO2↑ | D.HCl+KOH=KCl+H2O |
九年级化学选择题中等难度题查看答案及解析
以下化学反应属于中和反应的是( )
A.Na2O+H2O=2NaOH B.NaOH+HCl=NaCl+H2O
C.Fe+2HCl=FeCl2+H2↑ D.SO2+H2O=H2SO3
九年级化学单选题简单题查看答案及解析
我国第一艘自主建造的航母“山东舰”在建造时用到了大量钛合金,工业制钛的反应为:,则X的化学式为
A.SO2 B.SO3 C.H2SO3 D.H2O
九年级化学单选题中等难度题查看答案及解析
烟气脱硫的工艺不仅能消除SO2,还能将其转化为石膏,其主要物质的转化关系如图:

下列说法不正确的是( )
A. 步骤①喷淋水能脱去烟气中的SO2,反应的化学方程式为SO2+H2O═H2SO3
B. 步骤②中加入CaCO3的目的是将H2SO3转化为CaSO3
C. 步骤③反应前后只有硫元素的化合价发生了变化
D. 步骤④属于化学变化
九年级化学单选题简单题查看答案及解析
烟气脱硫的工艺不仅能消除SO2,还能将其转化为石膏,其主要物质的转化关系如图:

下列说法不正确的是( )
A. 步骤①喷淋水能脱去烟气中的SO2,反应的化学方程式为SO2+H2O═H2SO3
B. 步骤②中加入CaCO3的目的是将H2SO3转化为CaSO3
C. 步骤③反应前后只有硫元素的化合价发生了变化
D. 步骤④属于化学变化
九年级化学单选题简单题查看答案及解析
初中化学反应的基本类型包括:化合反应、分解反应、置换反应和复分解反应。下列反应中不属于这四种基本类型的是( )
A. CO+CuOCu+CO2 B. SO2+H2O=H2SO3
C. 2H2O2H2↑+O2↑ D. FeS+2HCl=FeCl2+H2S↑
九年级化学单选题简单题查看答案及解析
实验室用稀硫酸和亚硫酸钠反应制取二氧化硫气体,反应的化学方程式为:Na2SO3+H2SO4=SO2↑+Na2SO4+X,则 X 的化学式为( )
A. H2S B. H2O C. H2 D. O2
九年级化学单选题简单题查看答案及解析
某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一 定量的SO2(Na2SO3 +H2SO4(浓)==Na2SO4+SO2↑+H2O]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
(提出问题)①该瓶溶液中溶质的成分是什么?
②该瓶溶液中亚硫酸钠的质量分数是多少?
(查阅资料)
(1) Na2SO3有较强还原性,在空气中易被氧气氧化:2 Na2SO3 +O2==2Na2SO4;
(2) Na2SO3能与酸反应产生SO2气体;
(3)SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
(作出猜想)
猜想1:没有变质,成分是Na2SO3;
猜想2完全变质,成分是Na2SO4;
你认为还可能有的猜想3: _____________________。
(实验探究I)甲、乙两组分别进行实验探究溶液是否变质:
| 小组 | 实验操作 | 现象 | 结论 |
| 甲组 | 取少量样品于试管中加入过量稀盐酸; | 产生气泡 | 没有变质,还是Na2SO3 |
| 乙组 | 取少量样品于试管中加入氯化钡溶液,再加入足量稀盐酸。 | _____ | 已部分变质 |
(评价)有同学质疑甲组方案不合理,理由是___________。
(实验探究II)
甲组设计如下实验测定Na2SO3溶液的溶质质量分数。(注:空气中二氧化碳的影响忽略不计)
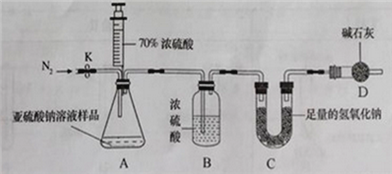
(1)连好装置并检查装置气密性,在锥形瓶中放入126g该样品
(2)实验前称量C装置的质量;
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡;
(4)打开活塞K,缓缓鼓入一定量的氮气,关闭活塞K;
(5)再次称量C装置的质量发现比反应前增重6.4g。
由此,计算出该溶液中Na2SO3的质量分数为_____________;
(解释)若没有进行第4步操作,则测得亚硫酸钠溶液的溶质质量分数比实际的____(填”偏小”或”偏大”)。
乙组仍使用第一次实验的原理,进行如下实验测定Na2SO3溶液的溶质质量分数。
第一步:称取试样ag;
第二步:在溶液中加入过量氯化钡溶液和足量稀盐酸;
第三步:过滤、洗涤、烘干沉淀;
第四步:称量沉淀的质量为bg;
第五步:计算溶液中Na2SO3的溶质质量分数=(1-142b/233a) ×100%。
试完成下列问题:
(1)加入氯化钡溶液过量的目的是________________;
(2)第三步操作要洗涤沉淀的原因是______________________;
(反思)由此可得出,保存亚硫酸钠时应___________________________。
九年级化学综合题困难题查看答案及解析
某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的SO2(Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O).老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
(提出问题)①该瓶溶液中溶质的成分是什么?②该瓶溶液中亚硫酸钠的质量分数是多少?
(查阅资料)
(1)Na2SO3有较强还原性,在空气中易被氧气氧化:2Na2SO3+O2=2Na2SO4;(2)Na2SO3能与酸反应产生SO2气体;
(3)SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
(作出猜想)
猜想1没有变质,成分是Na2SO3;猜想2完全变质,成分是Na2SO4;
你认为还可能有的猜想3______。
(实验探究I)甲、乙两组分别进行实验探究溶液是否变质:
| 小组 | 实验操作 | 现象 | 结论 |
| 甲组 | 取少量样品于试管中加入过量稀盐酸 | 产生气泡 | 没有变质,还是Na2SO3 |
| 乙组 | 取少量样品于试管中加入氯化钡溶液,再加入足量稀盐酸 | ______ | 已部分变质 |
(评价)有同学质疑甲组方案不合理,理由是______。
(实验探究Ⅱ)
甲组设计如下实验测定Na2SO3溶液的溶质质量分数。(注:空气中二氧化碳的影响忽略不计)
(1)连好装置并检查装置气密性,在锥形瓶中放入126g该样品;
(2)实验前称量C装置的质量;
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡;
(4)打开活塞K,缓缓鼓入一定量的氮气,关闭活塞K;
(5)再次称量C装置的质量发现比反应前增重6.4g;
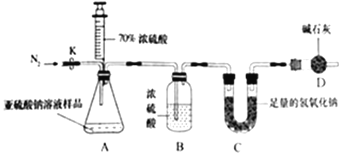
D装置的作用为______。计算出该溶液中Na2SO3的质量分数为______。
(解释)若没有进行第4步操作,则测得亚硫酸钠溶液的溶质质量分数比实际的______(填“偏小”或”偏大”)。
(反思)由此可得出,保存亚硫酸钠时应______。
九年级化学科学探究题困难题查看答案及解析