-
某研究小组利用软锰矿(主要成分MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程脱除燃煤尾气中的SO2,同时制取MnO2(反应条件已省略)。
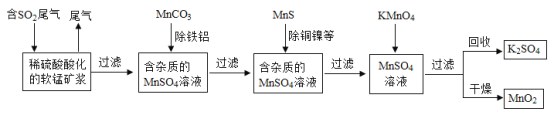
请回答下列问题:
(1)燃煤尾气中的SO2引起的环境问题是________________。
(2)利用浓硫酸稀释可以得到稀硫酸,其操作方法是_______________。
(3)上述流程中多次涉及到过滤操作,过滤中所使用的玻璃仪器有烧杯、漏斗和_______________,它的作用是___________。
(4)回收的二氧化锰可以用于实验室制取氧气,写出有关化学反应方程式:_______________。(写一个即可)
(5)写出另一回收产物的K2SO4一点用途_______________。
-
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。

(1)上述脱硫流程不能实现_____(选填字母)。
A废弃物的综合利用 B白色污染的减少 C酸雨的减少
(2)流程中的过滤操作,使用的玻璃仪器除烧杯、漏斗外,还有_____(其作用是_____)。
(3)写出实验室中MnO2催化氯酸钾分解的化学方程式:_____。
(4)燃煤尾气中含有大量的CO2,过量排放CO2将导致的环境问题是_____;实验室检验CO2通常使用_____(写一种物质)。
(5)加入MnCO3的作用是消耗溶液中的酸,促使铝、铁离子水解生成氢氧化物沉淀,离子的水解主要是指在特定条件下能跟水发生反应,如Al3++3H2O=Al(OH)3↓+3H+.试写出铁离子(Fe3+)发生水解反应的化学方程式:_____。
(6)反应制得的硫酸钾可用于农业生产,它属于_____(选填“氮肥”、“磷肥”、“钾肥”或“复合肥”)。
-
我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:
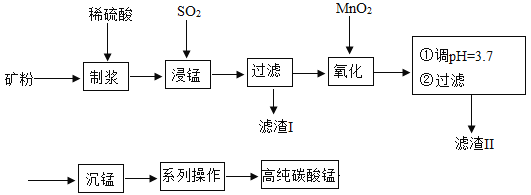
已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____、_____(写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____, 该反应中共有_____种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____%(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
| 矿酸比 | 温度/(℃) | 浸出率/(%) |
| 1 | 1:0.5 | 60 | 80.2 |
| 2 | 1:0.5 | 80 | 83.8 |
| 3 | 1:0.6 | 60 | X |
| 4 | 1:0.6 | 80 | 91.8 |
表中 X 最有可能的数值为_____。
a.79.7 b.80.8 c.87.6 d.92.8
-
我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:
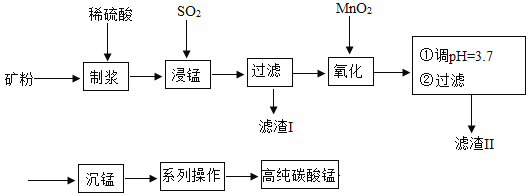
已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____、_____(写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____, 该反应中共有_____种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____%(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
| 矿酸比 | 温度/(℃) | 浸出率/(%) |
| 1 | 1:0.5 | 60 | 80.2 |
| 2 | 1:0.5 | 80 | 83.8 |
| 3 | 1:0.6 | 60 | X |
| 4 | 1:0.6 | 80 | 91.8 |
表中 X 最有可能的数值为_____。
a.79.7 b.80.8 c.87.6 d.92.8
-
工业上利用软锰矿(主要成分MnO2)制备高锰酸钾的流程如下图所示。回答下列问题:(信息提示:MnO2 不溶于水,含钾化合物均可溶于水;反应物接触面积越大,反应速率越快。)

(1)将软锰矿粉碎的目的是_____________________。
(2)流程中通入的气体X是___________(填标号)
A.N2 B.CO2 C.H2
(3)操作Y的名称叫 ,用到的玻璃仪器有烧杯和 、 。
(4)上述流程中可循环利用的物质有 和_______。
-
工业上利用软锰矿(主要成分MnO2)制备高锰酸钾的流程如下图所示。回答下列问题:(信息提示:MnO2 不溶于水,含钾化合物均可溶于水;反应物接触面积越大,反应速率越快。)
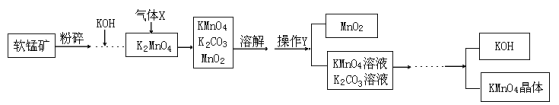
(1)将软锰矿粉碎的目的是_____________________。
(2)流程中通入的气体X是___________(填标号)
A.N2 B.CO2 C.H2
(3)操作Y的名称叫 ,用到的玻璃仪器有烧杯和 、 。
(4)上述流程中可循环利用的物质有 和_______。
-
KMnO4是锰的重要化合物,工业上常用软锰矿(主要成分为MnO2)制KMnO4。工艺流程如下(设备1~4中都含有水):
资料:K2CO3易溶于水
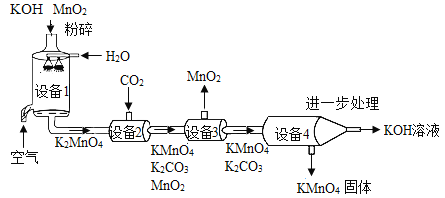
(1)设备1涉及的下列物质中,属于氧化物的是_____(填序号,下同)。
A.KOH B.MnO2 C.O2
(2)设备2涉及的物质中,锰元素化合价为+6价的是_____。
(3)在“进一步处理”过程中,可将K2CO3转化为KOH,应加入的物质是_____。
A.CaCO3 B.KCl C.Ca(OH)2
(4)上述流程中可以循环使用的物质有H2O、_____。
-
由软锰矿(主要成分为MnO2)制备KMnO4反应流程可表示如下,下列说法正确的是

A. MnO2可循环利用
B. 反应I中无元素化合价变化
C. 操作Ⅰ和操作Ⅱ是相同的操作
D. 反应Ⅱ是3K2MnO4+2H2SO4=MnO2↓+2KMnO4+2H2O+2X,则X是K2SO4
-
工业上利用软锰矿(主要成分MnO2)制备高锰酸钾的流程如图所示。回答下列问题:(信息提示:MnO2不溶于水,含钾化合物均可溶于水)
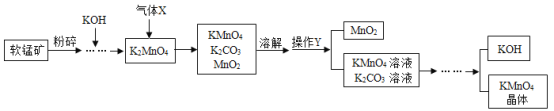
(1)将软锰矿粉碎的目的是______。
(2)流程中通入的气体X是______(填标号)。
A.N2 B.CO2 C.H2
(3)操作Y的名称是______。
(4)上述流程中可循环利用的物质有______。
-
工业上利用软锰矿(主要成分MnO2)制备高锰酸钾的流程如图所示。回答下列问题:
(信息提示:MnO2不溶于水,含钾化合物均可溶于水)
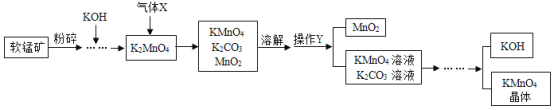
(1)将软锰矿粉碎的目的是_____。
(2)流程中通入的气体X是_____(填标号)。
A N2 B CO2 C H2
(3)操作Y的名称是_____。
(4)上述流程中可循环利用的物质有_____。









