为除去食盐水中 CaCl2、MgCl2、Na2SO4 杂质,某化学小组设计了如下方案:
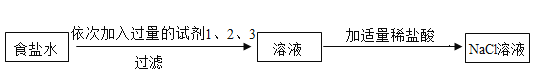
(1)过滤用到的玻璃仪器有烧杯、漏斗和_____。
(2)分别写出试剂 1、2、3 的化学式_____。
(3)最后所得溶液中 NaCl 的质量大于原混合溶液中 NaCl 的质量,写出一个可使NaCl 质量增加的化学方程式_____。
九年级化学流程题中等难度题
为除去食盐水中 CaCl2、MgCl2、Na2SO4 杂质,某化学小组设计了如下方案:

(1)过滤用到的玻璃仪器有烧杯、漏斗和_____。
(2)分别写出试剂 1、2、3 的化学式_____。
(3)最后所得溶液中 NaCl 的质量大于原混合溶液中 NaCl 的质量,写出一个可使NaCl 质量增加的化学方程式_____。
九年级化学流程题中等难度题
为除去食盐水中 CaCl2、MgCl2、Na2SO4 杂质,某化学小组设计了如下方案:

(1)过滤用到的玻璃仪器有烧杯、漏斗和_____。
(2)分别写出试剂 1、2、3 的化学式_____。
(3)最后所得溶液中 NaCl 的质量大于原混合溶液中 NaCl 的质量,写出一个可使NaCl 质量增加的化学方程式_____。
九年级化学流程题中等难度题查看答案及解析
为除去食盐水中CaCl2、MgCl2、Na2SO4杂质,某化学小组设计了如图方案:试剂1:NaOH,试剂2:BaCl2,试剂3:Na2CO3。
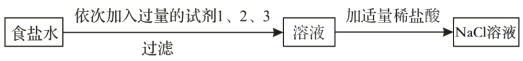
(1)过滤用到的玻璃仪器有烧杯、漏斗和_____。
(2)最后所得溶液中NaCl的质量大于原混合溶液中NaCl的质量,写出一个可使NaCl质量增加的化学方程式_____。
九年级化学填空题简单题查看答案及解析
为除去粗盐水中的可溶性杂质MgSO4、CaCl2,某化学小组同学设计了以下方案,下列说法正确的是(微溶物不形成沉淀)( )
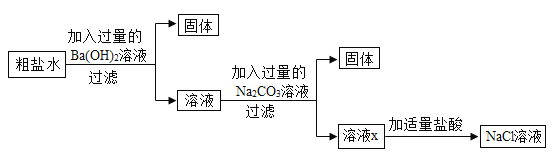
A.过滤用到的玻璃仪器有烧杯、玻璃棒、漏斗
B.溶液X中只含溶质NaCl和Na2CO3
C.加入Ba(OH)2溶液时发生化学反应的化学方程式为Ba(OH)2+MgSO4=Mg(OH)2↓+BaSO4↓
D.可以先加入过量的Na2CO3溶液再加入过量的Ba(OH)2溶液
九年级化学单选题中等难度题查看答案及解析
为了除去氯化钠样品中的碳酸钠杂质,兴趣小组最初设计了如下的方案并进行实验。

(1)写出沉淀A的化学式 。
(2)加入CaCl2溶液后,分离除去沉淀A的实验操作和蒸发所共同用到的一种玻璃仪器是 。
(3)同学在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分 (用化学式表示)。
(4)同学继续探究后又提出新的方案:将混合物溶解,若滴加过量盐酸至不再产生气体为止,则既能除去Na2CO3杂质,又能有效地防止新杂质的引入。写出有关反应的化学方程式: 。
(5)你认为物质B中是否含有杂质氯化氢 (填“是”或“否”),理由是 。
九年级化学填空题中等难度题查看答案及解析
除去食盐水中的CaCl2、和Na2SO4和MgCl2杂质的操作有:①加过量的BaCl2溶液;②过滤;③加过量Na2CO3溶液;④蒸发结晶;⑤加适量盐酸;⑥加过量Ca(OH)2溶液;。下列操作顺序正确的是(提示BaSO4、BaCO3难溶于水)
A. ①③⑥②⑤④ B. ⑥①⑤③②④ C. ⑥①③⑤④② D. ①⑥③②⑤④
九年级化学单选题中等难度题查看答案及解析
我国海水晒盐的历史悠久。粗盐中含有不溶性泥沙、可溶性 CaCl2、MgCl2 等杂质。学习小组设计了如下方案提纯粗盐:
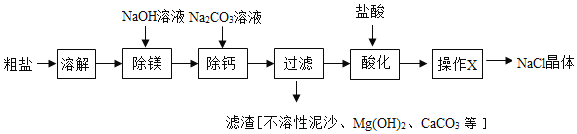
(1)用化学方程式表示 Na2CO3 溶液的作用:______。
(2)“过滤”中玻璃棒的作用为______;“操作 X”的名称为______。
(3)“酸化”过程中有气体生成的反应的化学方程式:______。
(4)酸化时加入过量的盐酸,对氯化钠晶体的纯度无影响,理由是______。
(5)若不考虑实验过程中的损耗,最终所得氯化钠晶体质量______(选填“大于”“等于”、“小于”)粗盐中氯化钠质量。
九年级化学流程题困难题查看答案及解析
利用海水晒盐的工业流程主要如下:
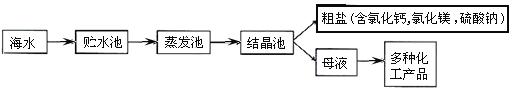
[提出问题]
怎样将析出的粗盐中含有CaCl2、MgCl2和Na2SO4都除去?
[设计实验]
方案一:工业上利用某种饱和溶液浸洗上述杂质的方法,这种饱和溶液是①________饱和溶液;
方案二:在实验室中,有人设计如下实验流程:
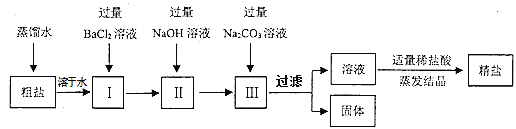
在上述方案中:
(1)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是②__________;
(2)上述流程中,过滤出的固体成分是③__________________(写化学式);
[反思交流]
(1)通过粗盐的成分可知,其中含有Cl—和SO42-,你证明这两种混合离子的方法是:将粗盐溶于水,配成溶液,然后④__________;
(2)通过上述方法,总结检验混合离子的方法是:先选试剂,后排顺序。这里的排顺序原则是指⑤_______________;
[拓展应用]
工业上得到精盐后,用给氯化钠水溶液通电的方法制取火碱,同时还生成两种气体单质,这两种单质化合后的生成物溶于水又能得到盐酸。写出给氯化钠水溶液通电的化学方程式⑥_____________
九年级化学流程题简单题查看答案及解析
利用海水晒盐的工业流程主要如下:
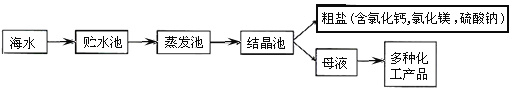
[提出问题]
怎样将析出的粗盐中含有CaCl2、MgCl2和Na2SO4都除去?
[设计实验]
方案一:工业上利用某种饱和溶液浸洗上述杂质的方法,这种饱和溶液是①________饱和溶液;
方案二:在实验室中,有人设计如下实验流程:
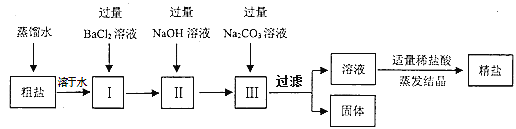
在上述方案中:
(1)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是②__________;
(2)上述流程中,过滤出的固体成分是③__________________(写化学式);
[反思交流]
(1)通过粗盐的成分可知,其中含有Cl—和SO42-,你证明这两种混合离子的方法是:将粗盐溶于水,配成溶液,然后④__________;
(2)通过上述方法,总结检验混合离子的方法是:先选试剂,后排顺序。这里的排顺序原则是指⑤_______________;
[拓展应用]
工业上得到精盐后,用给氯化钠水溶液通电的方法制取火碱,同时还生成两种气体单质,这两种单质化合后的生成物溶于水又能得到盐酸。写出给氯化钠水溶液通电的化学方程式⑥_____________
九年级化学流程题简单题查看答案及解析
宁波有较长的海岸线,每年能生产大量的食用盐。从海水中结晶的食盐一般混有MgCl2、CaCl2、Na2S04等杂质,为了除去上述杂质,设计了如下实验方案:先将固体溶解,然后向溶液中依次加人过量的BaCl2、NaOH、Na2C03溶液,充分反应后过滤,将滤液蒸发结晶,得到较纯净的食盐。
(1)溶解、过滤和蒸发操作中都要用到玻璃棒。过滤时,玻璃棒的作用是 。
(2)加入BaCl2溶液的目的是为了除去 杂质。
(3)以上方案不够完善.应在过滤后增加一个步骤:往滤液中加入适量的 。
九年级化学填空题困难题查看答案及解析
通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)在第⑤步粗盐过滤操作中要用到玻璃棒,玻璃棒的作用是_____________。
(2)第⑥步操作的目的是除去滤液中Na2CO3、_________(填化学式)。
(3)第④步操作的目的是除去滤液中CaCl2、_________(填化学式)。
九年级化学简答题中等难度题查看答案及解析