-
(1)某同学设计了如图1所示的实验装置探究影响锌和盐酸反应速率的因素。
① 该装置气密性的检查方法是__________________________
② 如图所示实验中的实验现象是__________________________。
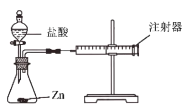
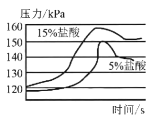
③用压强传感器替换注射器进行实验,测得等质量且过量的锌片分别与等质量、浓度为5%、15%的稀盐酸反应时压强随时间的变化关系曲线如上图所示。根据该图中的信息,你能得出的两条合理结论是:_____________;_______________;
(2)为了证明过氧化钠(Na2O2)固体可在呼吸面具和潜水艇中做供氧剂,某化学兴趣 小组的同学利用下图所示的实验装置进行探究活动。
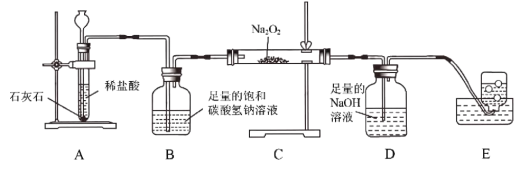
己知:2Na2O2+2CO2=2Na2CO3+ O2,2Na2O2+2H2O =4NaOH+O2↑
①用E装置收集气体时,判断气体收集满的方法是: __________________ ;
②D装置的作用是 _____________________ ;
③实验结束后,取出C装置中的固体溶于水,有气泡产生,得到无色溶液。则该无色溶液中存在的溶质是 ________________ (填化学式)。
④与高锰酸钾制氧气的方法相比,过氧化钠(Na2O2)固体作为呼吸面具和潜水艇中的供氧剂的主要优点是: _______________ (任答一点)。
-
化学实验小组设计如图装置,通过测定产生相同体积气体所用时间长短来探究影响双氧水分解速率的因素。
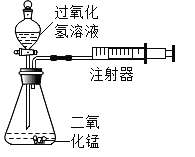
(1)检查该装置气密性的方法是关闭分液漏斗活塞,用力将注射器活塞拉出(右移),停止用力后,若观察到_______________,则气密性良好。
(2)如图反应的符号表达式为_____________。
(3)实验小组有如下设计方案,完成下表。
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 | 所需时间 |
| 实验Ⅰ | 探究_______对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 | 60秒 |
| 实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 | 30秒 |
由上表数据可知:双氧水的浓度越大,其分解速率__________,影响双氧水分解速率的因素可能还有_________________。
(4)催化剂在生产、生活和科研中的地位越来越重要。实验室用过氧化氢溶液分解制取氧气时,就常用二氧化锰作催化剂。
(提出问题)氧化铜(CuO)能否起到类似MnO2的催化剂作用呢?
(猜想假设)猜想一:CuO不是该反应的催化剂。
猜想二:CuO参与反应产生O2,反应前后质量和化学性质发生了改变。
猜想三:CuO是反应的催化剂,反应前后_____________。
(实验探究)用天平称量0.2 g CuO,取5 mL 5%的过氧化氢溶液于试管中,进行如下实验:
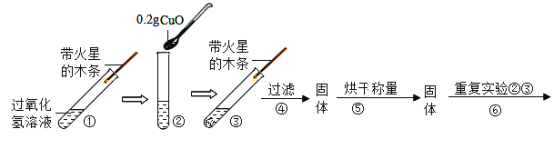
(注:氧化铜不溶于水,过滤可与水分离)
(交流讨论)
(1)填写下表:
| 步骤③现象 | 步骤⑤结果 | 结论 |
| 产生大量的气泡,带火星的木条________。 | 得到氧化铜的质量为_______g。 | 猜想一、二不成立; 猜想三成立。 |
(2)步骤①的目的是____________。步骤④需用到的玻璃仪器有:玻璃棒、烧杯和_________,其中玻璃棒的作用是___________。
(3)步骤⑥重复实验②、③的目的是___________。
-
某校化学活动小组准备测定生成O2 的体积并探究影响反应速率的因素。
(实验一)通过下列实验,利用二氧化锰粉末与过氧化氢溶液反应来测定生成 O2 的体积。
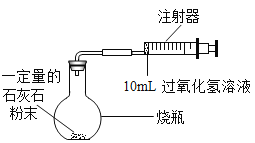
(1)实验中,先连接好装置后检查装置的气密性,然后装好药品,最后将 10mL 过氧化氢溶液_______(填“快速”或“缓慢”)推入烧瓶中,如果不这样操作,则可能造成的后果是_________。
(实验二)探究 H2O2 质量分数、溶液 pH、温度对反应速率的影响。设计如下表实验方案:
| 实验序号 | H2O2 质量分数 | pH | 温度/℃ | 30s 内收集到氧气的体积 |
| 1 | 25 | 5 | 20 | |
| 2 | 25 | 6 | 20 | |
| 3 | 25 | 11 | 20 | |
| 4 | 15 | 11 | 30 | |
| 5 | a | 11 | b | |
(2)实验 1~3 的实验目的是_____。
(3)a=_____;b=_____。
(实验三)探究催化剂对化学反应速率的影响:
取 5mL 溶质质量分数相同的 H2O2 溶液,三次实验分别加入质量均为 0.5gMnO2、红砖粉末、CuO 进行实验,记录收集相同体积氧气所用时间的数据如下:
| 试剂 | MnO2 | 红砖粉末 | CuO |
| 时间/s | 10 | 60 | 20 |
由此得出结论:MnO2、CuO 对 H2O2 分解有催化作用,红砖粉末无催化作用。
(4)你认为该结论是否正确?_____(填“正确”或“不正确”),为什么?_____。
-
现甲、乙两化学小组安装两套如图1的相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
(1)下列方法能检查该装置气密性的是 。
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)二氧化锰催化下过氧化氢分解的文字或符号表达式是 。

(3)甲小组有如下实验设计方案,完成下表
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究 对 过氧化氢分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%过氧化氢 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%过氧化氢 |
(4)甲、乙两小组得出如图2的数据
Ⅰ甲组实验得出的数据可知:浓度越大,过氧化氢分解速率 ;(填“越快”或“越慢”)
Ⅱ由乙组研究的酸、碱对过氧化氢分解影响因素的数据分析:相同条件下,过氧化氢在 (填“酸”或“碱”)性环境下放出气体速率较快。
-
科学兴趣小组安装如图装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
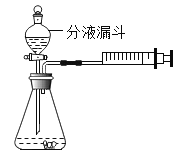
(1)下列方法能检查该装置气密性的是______。
A 将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B 关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热冷却后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C 关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)往加有二氧化锰的锥形瓶中加入过氧化氢溶液后,注射器活塞向右移动的原因是______。
-
(6分)现甲、乙两化学小组安装两套下图所示相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
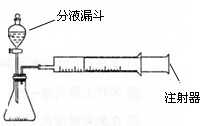
(1)下列方法不能检查该装置气密性的是______。
A.将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏
斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B.关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C.关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)甲小组有如下实验设计方案,完成下表。
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究 对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
(3)甲、乙两小组得出如图数据。
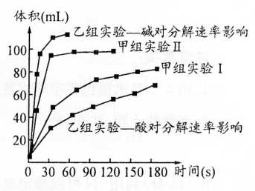
①由甲组实验得出的数据可知:浓度越大,H2O2分解速率 。
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下, H2O2在 (填“酸性”或“碱性”)环境下放出气体速率较快;乙组提出可以用Ba02固体与硫酸溶液反应制H202(已知还生成另一种物质),其化学反应方程式为 ;支持这一方案的理由是 。
-
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
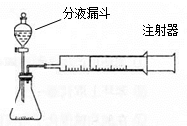
(1) 下列方法能检查该装置气密性的是______。
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)MnO2催化下H2O2分解的表达式是___________________________________。
(3)甲小组有如下实验设计方案,完成下表。
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 | 所需时间 |
| 甲组实验Ⅰ | 探究______对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 | 60s |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 | 30s |
①甲组实验得出的数据可知:浓度越大,H2O2分解速率越_____________;
实验延伸
探究实验:温度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
| ______________________ | ____________ | 温度越高,过氧化氢分解的速率越大 |
| __________________________ | _______________ |
同学们还想探究二氧化锰的颗粒大小对反应速率的影响,请设计方案进行探究。
___________________________________________________________
-
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。

(1) 下列方法能检查该装置气密性的是______。

 A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)MnO2催化下H2O2分解的化学方程式是 。
(3)甲小组有如下实验设计方案,完成下表。
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究 对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
(4)甲、乙两小组得出如图数据。
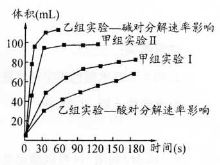
①甲组实验得出的数据可知:浓度越大,H2O2分解速率 ;
②由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下, H2O2在 (填“酸”或“碱”)性环境下放出气体速率较快;乙组提出可以用Ba02固体与硫酸溶液反应制H2O2(已知还生成另一种物质),其化学反应方程式为 ;支持这一方案的理由是 。
-
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短探究影响过氧化氢(H2O2)分解速率的因素
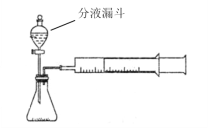
(1)检查此装置气密性的方法是:________________。
(2)甲小组有如下实验设计方案,完成下表。
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰0.2g | _____2%H2O2溶液 |
| 甲组实验Ⅱ | _____ | 二氧化锰0.2g | 10mL 5%H2O2溶液 |
(3)甲、乙两小组得出如图数据。
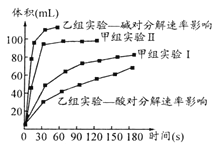
①甲组实验得出的数据可知浓度越大,H2O2分解速率 ___________ ;
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析相同条件下H2O2在________(填“酸”或“碱”)性环境下放出气体速率较快。
-
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
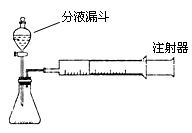
(1)下列方法能检查该装置气密性的是______。
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)MnO2催化下H2O2分解的符号表达式是 。
(3)甲小组有如下实验设计方案,完成下表。
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究 对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
(4)甲、乙两小组得出如下图数据。
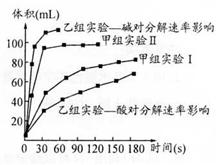
①甲组实验得出的数据可知:浓度越大,H2O2分解速率 ;
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下, H2O2在 (填“酸”或“碱”)性环境下放出气体速率较快。
















