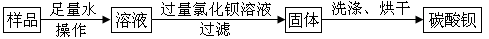-
(2011•江西)为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:

请问:①操作I的名称是______.要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和______;
②若过滤所得固体未经洗涤即烘干称重,测得样品中氯化钠的质量分数将______.(填“偏高”、“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数.若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为______ g.(用a、b、c表示)
-
(2011江西)为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:

(1)方案1:
请问:①操作Ⅰ的名称是________.要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和________________.
②若过滤所得的固体未经洗涤即烘干称重,测得样品中氯化钠的质量分数将________________(填“偏高”“偏低”或“不变”).
(2)方案2:通过测定样品和足量硫酸溶液在烧杯中反应产生气体的质量来计算样品中氯化钠的质量分数.若测得各物质质量(g)为:样品质量为a,所用硫酸溶液质量为b,完全反应后烧杯中的混合物质量为c,则生成气体的质量为________g(用a、b、c表示).
-
为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:

请问:①操作Ⅰ的名称是 。要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和 ;
②若过滤所得固体未经洗涤即烘干称量,测得样品中氯化钠的质量分数将 。(填“偏大”“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为 g。(用a、b、c表示)
-
为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:
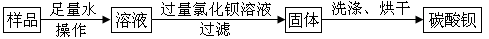
请问:①操作的名称是________。要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和;
②若过滤所得固体未经洗涤即烘干称量,测得样品中氯化钠的质量分数将________。(填“偏大”、“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为________g。(用a、b、c表示)
-
为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:

(1)【方案1】
请问:①操作II的名称是
②X的化学式为 (写一种)
(2)【方案2】 通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。
①若测得各物质的质量(g):样品质量为m1,所用硫酸溶液质量为m2,完全反应后混合溶液质量为m3,则生成气体的质量为___________ g。(用m1、m2、m3表示)
②请你再设计一种测定生成气体质量的方法,并注明需要测定哪些数据?
【拓展提高】有人提出还有第三种方案:可用AgNO3溶液作为试剂,通过称量沉淀质量来确定氯化钠的质量?你认为是否可行,为什么?(2分 )
-
为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:

请问:①操作I的名称是______.要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和______;
②若过滤所得固体未经洗涤即烘干称重,测得样品中氯化钠的质量分数将______.(填“偏高”、“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数.若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为______ g.(用a、b、c表示)
-
为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:

请问:①操作I的名称是______.要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和______;
②若过滤所得固体未经洗涤即烘干称重,测得样品中氯化钠的质量分数将______.(填“偏高”、“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数.若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为______ g.(用a、b、c表示)
-
为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:

请问:①要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和________
②若过滤所得固体未经洗涤即烘干称重,测得样品中氯化钠的质量分数将________(填“偏高”、“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。若测得各物质质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为______g。(用a、b、c表示)
-
同学们在学习了盐的化学性质以后,开展了测定碳酸钠和氯化钠的固体混合物中碳酸钠的质量分数的探究实验,他们设计了以下实验方案
【方案一】气体转化法

(1)如图1所示,把wg的混合物与足量稀硫酸反应后,测定产生的CO2的体积,检查该装置气密性的方法是______;
(2)有同学提出用图2代替图1中的收集装置,则所测得CO2气体的体积______;
(填偏大、偏小或不变)理由是______,你的改进方案是______;广口瓶内原有的空气对实验结果______(填“有”或“没有”)影响,如果利用改进后的装置测得CO2气体的体积为Vml (此时CO2的密度为Pg/ml)则原混合物中Na2CO3的质量分数的计算式为______;
(3)也有人用图3装置测定CO2的质量(碱石灰的成分是CaO和NaOH的混合物)则图3实验装置中主要存在哪些缺陷?这些缺陷对实验结果有何影响?
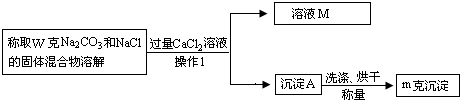
【方案二】沉淀法(如图所示)

(1)沉淀A的化学式是______,溶液M中溶质的化学式是______;
(2)确定CaCl2溶液是否过量的方法是______;
(3)该固体混合物中Na2CO3的质量分数的计算式为______;
(4)导致测定结果偏大的原因可能是______;
【方案三】盐酸滴定法

(1)“操作2”的名称是______;
(2)根据实验数据计算该固体混合物中Na2CO3的质量分数为______(保留一位小数).
-
同学们在学习了盐的化学性质以后,开展了测定碳酸钠和氯化钠的固体混合物中碳酸钠的质量分数的探究实验,他们设计了以下实验方案
【方案一】气体转化法

(1)如图1所示,把wg的混合物与足量稀硫酸反应后,测定产生的CO2的体积,检查该装置气密性的方法是______;
(2)有同学提出用图2代替图1中的收集装置,则所测得CO2气体的体积______;
(填偏大、偏小或不变)理由是______,你的改进方案是______;广口瓶内原有的空气对实验结果______(填“有”或“没有”)影响,如果利用改进后的装置测得CO2气体的体积为Vml (此时CO2的密度为Pg/ml)则原混合物中Na2CO3的质量分数的计算式为______;
(3)也有人用图3装置测定CO2的质量(碱石灰的成分是CaO和NaOH的混合物)则图3实验装置中主要存在哪些缺陷?这些缺陷对实验结果有何影响?
【方案二】沉淀法(如图所示)
(1)沉淀A的化学式是______,溶液M中溶质的化学式是______;
(2)确定CaCl2溶液是否过量的方法是______;
(3)该固体混合物中Na2CO3的质量分数的计算式为______;
(4)导致测定结果偏大的原因可能是______;
【方案三】盐酸滴定法

(1)“操作2”的名称是______;
(2)根据实验数据计算该固体混合物中Na2CO3的质量分数为______(保留一位小数).