(3分)工业上可用电解饱和食盐水的方法制备氢氧化钠,反应原理是:
2NaCl + 2H2O2NaOH + Cl2↑+ H2↑
若电解含氯化钠23.4 t的饱和食盐水,则可制得氢氧化钠多少吨?(写出计算过程)
九年级化学计算题简单题
(3分)工业上可用电解饱和食盐水的方法制备氢氧化钠,反应原理是:
2NaCl + 2H2O2NaOH + Cl2↑+ H2↑
若电解含氯化钠23.4 t的饱和食盐水,则可制得氢氧化钠多少吨?(写出计算过程)
九年级化学计算题简单题
(3分)工业上可用电解饱和食盐水的方法制备氢氧化钠,反应原理是:
2NaCl + 2H2O2NaOH + Cl2↑+ H2↑
若电解含氯化钠23.4 t的饱和食盐水,则可制得氢氧化钠多少吨?(写出计算过程)
九年级化学计算题简单题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
(3分)工业上可用电解饱和食盐水的方法制取氢氧化钠,反应原理是: 2NaCl + 2H2O 通电 2NaOH + Cl2↑+ H2↑ 若电解含氯化钠58.5 t的饱和食盐水,则可制得氢氧化钠多少吨?(写出计算过程)
九年级化学计算题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
海水晒盐得到的粗盐除去杂质后,除可做调料,还可以作为工业原料。某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的方程式为:2NaCl + 2H2O2NaOH + Cl2↑ + H2↑),这种工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。某兴趣小组同学对存放的该厂生产的烧碱样品产生兴趣,对该样品的成分进行了如下探究:
(提出问题)该烧碱样品中可能含有哪些杂质?
(猜想)甲同学:可能含有NaCl
乙同学:可能含有Na2CO3,乙同学猜想的依据是_________________。
(实验探究)为探究该烧碱样品的成分及样品的纯度(氢氧化钠在样品中所占的质量分数),甲、乙两同学通过思考分别设计了如下实验:
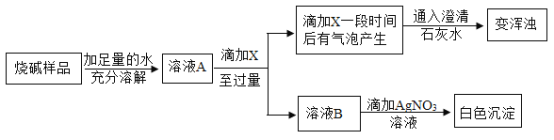
甲同学设计如下方案对烧碱样品的组成进行探究,请回答:
(1)试剂X应选用_________(填化学式)才能依据相应的现象得出正确结论。
乙同学设计了如下方案测定该烧碱样品的纯度:
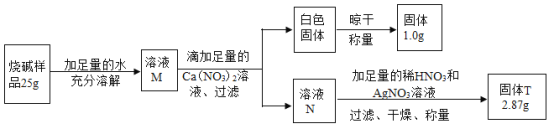
(2)滴加足量Ca(NO3)2的目的是__________________。
(3)请利用乙同学的实验数据,计算该样品中碳酸钠的质量,写出计算过程______________。
(4)该烧碱样品中氢氧化钠的质量分数为_____。(不写计算过程,结果精确到0.1%)
(5)实验结束后,两同学发现测得的该烧碱样品纯度低于工厂样品纯度,请从实验操作的角度分析,原因可能是_______________。
九年级化学科学探究题困难题查看答案及解析
氯碱工业是最基本的化学工业之一,是指工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品。反应原理是:
2NaCl + 2H2O2NaOH + Cl2↑ + H2↑
(1)工业上电解浓度为26.5%的饱和工业盐水200t,则生产氯气的质量是多少_____?(精确到0.1)
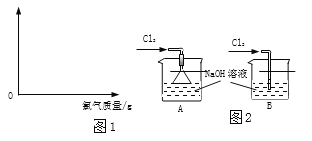
(2)取电解生产的氯气71g,通入到一定浓度的NaOH溶液中制备漂白液(主要成分为盐NaClO),反应原理为:Cl2 + 2NaOH = NaClO + NaCl + H2O。请在图1坐标中画出相应的曲线图(纵坐标为盐的质量,请设定具体物质,并标出曲线中必要的数据_____)。
(3)图2是实验室制备漂白液的部分装置。最好选用的装置是_____(填序号),理由_____。
九年级化学计算题困难题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
工业上用电解饱和NaCl溶液的方法制烧碱,其反应的化学方程式如下:
2NaCl + 2H2O2NaOH + H2↑+Cl2↑
(1)NaOH中钠、氧、氢元素的质量比为 。
(2)已知20℃时,NaCl的溶解度为36 g,其饱和溶液中溶质和溶剂的质量比为 。
(3)20℃时,取136 g饱和NaCl溶液电解,当NaCl转化了32.5%时,理论上剩余溶液的质量为多少?
九年级化学计算题中等难度题查看答案及解析