-
科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
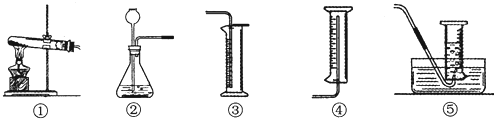
(一)选择装置并检查气密性.
(二)称取0.1克的二氧化锰粉末加入容器中.
(三)量取50毫升溶质质量分数约10%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
(四)改变二氧化锰的质量,重复上述实验,记录数据如下.
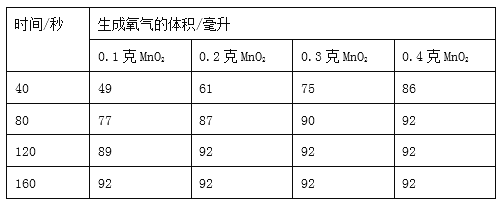
| 时间/秒 | 生成氧气的体积/毫升 |
| 0.1克MnO2 | 0.2克MnO2 | 0.3克MnO2 | 0.4克MnO2 |
| 40 | 49 | 61 | 75 | 86 |
| 80 | 77 | 87 | 90 | 92 |
| 120 | 89 | 92 | 92 | 92 |
| 160 | 92 | 92 | 92 | 92 |
(1)写出本实验的化学方程式________.随着反应的进行,溶液中________(填写化学式)在不断地减少、溶剂在不断地________(填增多、减少、不变).
(2)本实验探究的问题是________.
(3)实验中除了量筒外,还需要用到的测量仪器有________.
(4)为完成本实验,应选择右上图图气体发生和收集装置中的组合是________(选
填序号).你选择的气体发生装置的理由是________.
(5)在40秒时,通过四组数据分析,你得出的结论是________.
(6)若实验前加入MnO2 0.1g,实验后经过滤、洗涤、干燥、称量,MnO2质量为________g.
请设计实验证明该MnO2的化学性质在反应前后没有改变________.
-
科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
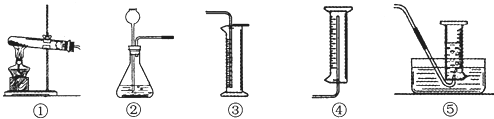
(一)选择装置并检查气密性.
(二)称取0.1克的二氧化锰粉末加入容器中.
(三)量取50毫升溶质质量分数约10%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
(四)改变二氧化锰的质量,重复上述实验,记录数据如下.
(1)写出本实验的化学方程式____.随着反应的进行,溶液中____(填写化学式)在不断地减少、溶剂在不断地____(填增多、减少、不变).
(2)本实验探究的问题是____.
(3)实验中除了量筒外,还需要用到的测量仪器有____.
(4)为完成本实验,应选择右上图图气体发生和收集装置中的组合是____(选填序号).你选择的气体发生装置的理由是____.
(5)在40秒时,通过四组数据分析,你得出的结论是____.
(6)若实验前加入MnO2 0.1g,实验后经过滤、洗涤、干燥、称量,MnO2质量为____g.请设计实验证明该MnO2的化学性质在反应前后没有改变____.
-
科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
(一)选择装置并检查气密性.
(二)称取0.1克的二氧化锰粉末加入容器中.
(三)量取50毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
(四)改变二氧化锰的质量,重复上述实验,记录数据如下.
| 时间/秒 | 生成氧气的体积/毫升 |
| 0.1克MnO2 | 0.2克MnO2 | 0.3克MnO2 | 0.4克MnO2 |
| 40 | 49 | 61 | 75 | 86 |
| 80 | 77 | 87 | 90 | 92 |
| 120 | 89 | 92 | 92 | 92 |
| 160 | 92 | 92 | 92 | 92 |
(1)本实验探究的问题是______.
(2)实验中除了量筒外,还需要用到的测量仪器有______.
(3)为完成本实验,应选择下图气体发生和收集装置中的组合是______.(选填序号)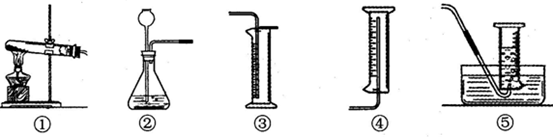
-
实验创新是中学生最为重要的科学素养,以下是化学兴趣小组的同学在学习“二氧化锰催化过氧化氢分解制氧气实验”后,对实验的创新设计。
(实验一):设计新的实验装置
实验过程如下:
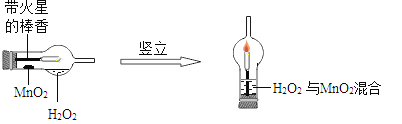
①将一支球形干燥管水平放置,用滴管吸取3ml(密度为1g/ml)质量分数为5%的H2O2加入干燥管的球泡中,再用药匙取0.2gMnO2粉末,加在干燥的进气管的管壁上;②点燃橡胶塞上固定的棒香后,塞紧干燥管并将其竖立,观察现象;
(1)可观察到带火星的棒香立即__________;
(2)下列各项是同学们对该创新实验的评价,你认为评价不合理的是 __________(填序号)
A.实验所用的仪器、材料及药品均易得到
B.实验室用的药品用量太大
C.反应速度太慢,耽误时间
D.实验现象明显,整个装置好似点燃的灯塔,趣味性强
(实验二):寻找新的催化剂
(实验探究)
| 实验步骤 | 实验现象 |
| I. 分别量取5mL 5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象。 | A试管中产生气泡,带火星木条复燃。B试管中无明显现象。 |
| II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃。 |
| III.将试验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥,称量。 | 所得的固体质量为_________________ |
| IV.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 | |
(实验结论)
(1)A中产生的气体是_________;
(2)实验II可以证明:____________,再结合实验I和III的结论可以证明氧化铁可以作为过氧化氢分解的催化剂。
(3)写出氧化铁(Fe2O3)催化过氧化氢分解的文字表达式:______;
(实验评价)
(1)设计实验IV的目的是__________;
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是_________。
(实验拓展)
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可做过氧化氢溶液分解的催化剂,下列有关催化剂的说法正确的是________________
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂能使原本不发生的反应也能快速进行
D.用作催化剂的物质不可能是其它反应的反应物或生成物
-
实验创新是中学生最为重要的科学素养,以下是化学兴趣小组的同学在学习“二氧化锰催化过氧化氢分解制氧气实验”后,对实验的创新设计.
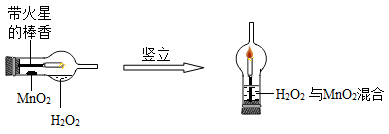
【实验一】:设计新的实验装置实验过程如下:①将一支球形干燥管水平放置,用滴管吸取3mL(密度为1g/mL)质量分数为5%的H2O2加入干燥管的球泡中,再用药匙取0.2g MnO2粉末,加在干燥的进气管的管壁上;②点燃橡胶塞上固定的棒香后,塞紧干燥管并将其竖立,观察现象;
(1)可观察到带火星的棒香立即____________;
(2)下列各项是同学们对该创新实验的评价,你认为评价不合理的是________(填序号)A.实验所用的仪器、材料及药品均易得到
B.实验室用的药品用量太大
C.反应速度太慢,耽误时间
D.实验现象明显,整个装置好似点燃的灯塔,趣味性强
【实验二】:寻找新的催化剂
【实验探究】
| 实验步骤 | 实验现象 |
| I.分别量取5mL 5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象. | A试管中产生气泡,带火星木条复燃.B试管中无明显现象. |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象. | 试管中均产生气泡,带火星木条均复燃. |
| Ⅲ.将试验II中的剩余物进行_______、洗涤、干燥,称量. | 所的固体质量为ag |
| IV.分别量取5ml5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象. | |
【实验结论】
(1)实验Ⅱ可以证明:__________________,再结合实验I和Ⅲ的结论可以证明氧化铁可以作为过氧化氢分解的催化剂。
(2)写出氧化铁(Fe2O3)催化过氧化氢分解的符号表达式:_________________
【实验评价】
(1)设计实验IV的目的是_____________________;
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是:____________________.
【实验拓展】查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可做过氧化氢溶液分解的催化剂,下列有关催化剂的说法正确的是_________
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂能使原本不发生的反应也能快速进行
D.用作催化 剂的物质不可能是其它反应的反应物或生成物.
-
实验创新是中学生最为重要的科学素养,以下是化学兴趣小组的同学在学习“二氧化锰催化过氧化氢分解制氧气实验”后,对实验的创新设计。
实验一:设计新的实验装置
实验过程如下:
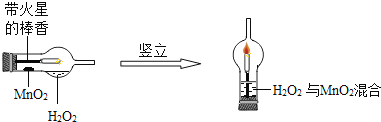
①将一支球形干燥管水平放置,用滴管吸取3mL(密度为1g/mL)质量分数为5%的H2O2加入干燥管的球泡中,再用药匙取0.2gMnO2粉末,加在干燥的进气管的管壁上;②点燃橡胶塞上固定的棒香后,塞紧干燥管并将其竖立,观察现象;
(1)可观察到带火星的棒香立即___;
(2)下列各项是同学们对该创新实验的评价,你认为评价不合理的是___(填序号)
A. 实验所用的仪器、材料及药品均易得到
B. 实验室用的药品用量太大
C. 反应速度太慢,耽误时间
D. 实验现象明显,整个装置好似点燃的灯塔,趣味性强
实验二:寻找新的催化剂
(实验探究)
| 实验步骤 | 实验现象 |
| I、分别量取5mL5%过氧化氢溶液放入A. B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A. B两支试管中插入带火星的木条,观察现象。 | A试管中产生气泡,带火星木条复燃.B试管中无明显现象。 |
| Ⅱ、待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃。 |
| Ⅲ、将试验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥,称量。 | 所的固体质量为___ |
| IV、分别量取5ml5%过氧化氢溶液放入C. D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 | |
(实验结论)
(1)A中产生的气体是___;
(2)实验Ⅱ、Ⅲ可以证明:___,再结合实验I和Ⅲ的结论可以证明氧化铁可以作为过氧化氢分解的催化剂。
(3)写出氧化铁(Fe2O3)催化过氧化氢分解的化学方程式:___________________;
(实验评价)
(1)设计实验IV的目的是___;
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是___.
(实验拓展)
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可做过氧化氢溶液分解的催化剂,下列有关催化剂的说法正确的是___
A. MnO2只能作为过氧化氢溶液分解的催化剂
B. 同一个化学反应可以有多种催化剂
C. 催化剂能使原本不发生的反应也能快速进行
D. 用作催化剂的物质不可能是其它反应的反应物或生成物
-
某化学学习小组了解到除了二氧化锰,氧化铜也可以作为双氧水分解的催化剂,为了比较两种催化剂的催化效果设计了如下实验方案。
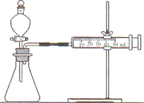
(1)连接仪器组装成如右图所示实验装置。如何检查该装置的气密性? ______。
(2)取等质量的二氧化锰和氧化铜,分别加入相同体积相 同质量分数的双氧水,写出二氧化锰催化双氧水分解的文字 表达式___________; 要比较两种催化剂的催化效果,可以测定分别加入两种催化剂得到相同体积氧气所需要的时间;还可测定________。
-
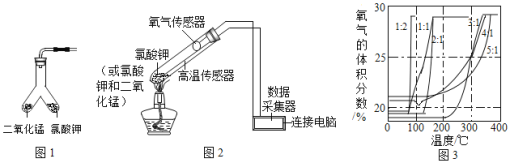
某化学兴趣小组通过实验探究分解氯酸钾制氧气的反应中二氧化锰的作用,该反应的符号表达式为______.
(设计实验)用图 1 所示装置进行实验,步骤如下:
步骤Ⅰ:检查装置气密性,操作方法是______,观察到______,则说明装置气密性良好; 步骤Ⅱ:按照如图 1 装入药品;
步骤Ⅲ:加热右侧支管,用带火星的木条在导管口检验生成的气体; 步骤Ⅳ:冷却后,将装置倾斜,使左侧支管中的药品进入右侧支管,再加热右侧支管,用带火星的木条在导 管口检验生成的气体.
(实验现象)步骤Ⅲ和步骤Ⅳ中,一段时间后都能观察到带火星的木条复燃,但不同的是______.
(交流反思)要想确认分解氯酸钾制氧气的反应中二氧化锰是催化剂,还需通过实验证明二氧化锰的_____和_____在反应前后都没有发生变化.
(拓展探究)在老师的指导下,该小组同学利用图 2 所示装置继续进行深入探究.以氧气的体积分数为纵 坐标,温度为横坐标,得到图 3 所示曲线(图中的“1:2”、“1:1”、“2:1”、“3:1”、“4:1”、“5:1”指氯 酸钾和二氧化锰的质量比).
(实 验 分 析) 根据图 3氯酸钾的分解温度随氯酸钾和二氧化锰的质量比变化的大致规律是__________________ ;分解氯酸钾制氧气的反应中二氧化锰起催化作用,可能是因为二氧化锰能_______________________.
-
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
一、为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g 10%过氧化氢溶液与1.0g MnO2均匀混合;Ⅱ.将x g10% H2O2溶液与1.0g CuO均匀混合。在相同温度下,比较两组实验产生O2的快慢。
10%过氧化氢溶液与1.0g MnO2均匀混合;Ⅱ.将x g10% H2O2溶液与1.0g CuO均匀混合。在相同温度下,比较两组实验产生O2的快慢。
(1)为了Ⅰ与Ⅱ中对比x的值应为 。
(2)甲选用下列装置测量产生O2的快慢,正确的是 (填编号)。
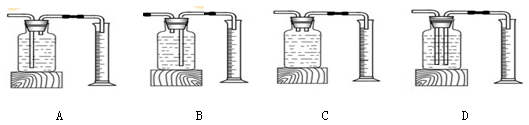
二、探究影响双氧水分解速度的某种因素。实验数据记录如下(常温通常指20℃)
| 实验 | 温度 | 药品 | 氧气体积/ml | 反应所需时间/s |
| ① | 常 温 | 5% H2O2 | | 0 | |
| 常 温 | 5% H2O2 | MnO2 | 125 | 20 |
| ② | 常 温 | 5% H2O2 | MnO2 | 125 | 20 |
| 热水中 | 5% H2O2 | MnO2 | 125 | 18 |
| ③ | 常 温 | 5% H2O2 | MnO2 | 125 | 20 |
| 常 温 | 30% H2O2 | MnO2 | 125 | 5 |
| | | | | |
(1)通过实验①对比可知,化学反应快慢与 有关。
(2)通过对比实验 可知 ,反应物浓度大,反应速率快。
,反应物浓度大,反应速率快。
(3)除了上述两个因素能影响化学反应快慢,你认为另一个影响因素是 ,其关系是 。
(4)由上述实验可知温度、浓度、催化剂等都是影响化学反应速率,实验室用过氧化氢制取氧气的最合适的条件是 。
-
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
一、为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g 10%过氧化氢溶液与1.0g MnO2均匀混合
Ⅱ.将x g10% H2O2溶液与1.0g CuO均匀混合
在相同温度下,比较两组实验产生O2的快慢。
(1)为了Ⅰ与Ⅱ中对比x的值应为 。
(2)甲选用下列装置测量产生O2的快慢,正确的是 (填编号)。
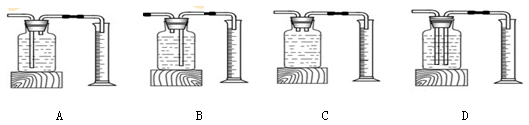
二、探究影响双氧水分解速度的某种因素。实验数据记录如下(常温通常指20℃)
| 实验 | 温度 | 药品 | 氧气体积/ml | 反应所需时间/s |
| ① | 常 温 | 5% H2O2 | | 0 | |
| 常 温 | 5% H2O2 | MnO2 | 125 | 20 |
| ② | 常 温 | 5% H2O2 | MnO2 | 125 | 20 |
| 热水中 | 5% H2O2 | MnO2 | 125 | 18 |
| ③ | 常 温 | 5% H2O2 | MnO2 | 125 | 20 |
| 常 温 | 30% H2O2 | MnO2 | 125 | 5 |
| | | | | |
(1)通过实验①对比可知,化学反应快慢与 有关。
(2)通过对比实验 可知,反应物浓度大,反应速率快。
(3)除了上述的两个因素能影响化学反应快慢,你认为另一个影响因素是 ,其关系是 。
(4)由上述实验可知温度、浓度、催化剂等都是影响化学反应速率,实验室用过氧化氢制取氧气的最合适的条件是 。










