-
(8分)生活中常遇见铜制品生锈的情况。活动课上,同学们设计实验对铜锈进行了如下探究活动。
探究活动一:验证铜锈的组成
【查阅资料】
① 铜锈为绿色,其主要成分是Cu2(OH)2CO3。
② 白色的硫酸铜粉末遇水能变为蓝色。
③ 碳不与稀硫酸反应。
④ 氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液。
【进行实验1】
同学们设计了下图所示装置并进行实验。

| 实验操作 | 实验现象 | 实验结论 |
| ① 按上图组装仪器,装入药品。 ② 加热铜锈,直至不再有气体产生,停止加热。 | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊。 | 加热铜锈生成的物质有_____;铜锈由_____元素组成;烧杯中发生反应的化学方程式为______。 |
| ③ 冷却后,向试管中固体加入适量稀硫酸,稍加热。 | 黑色固体溶解,溶液变为蓝色。 |
探究活动二:探究铜生锈的条件
【进行实验2】
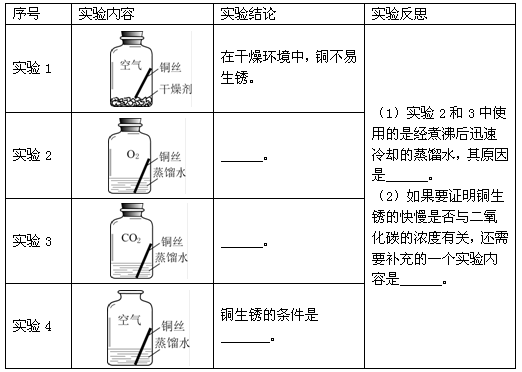
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显。
-
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.
探究活动一:验证铜锈的组成
(查阅资料)
①铜锈为绿色,其主要成分是Cu2(OH)2CO3.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应.
④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
(进行实验1)
同学们设计了如图所示装置并进行实验.
| 
实验操作 | 实验现象 | 实验结论 |
| ①按上图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有__;铜锈由___元素组成;烧杯中发生反应的化学方程式为___. |
| ③冷却后,向试管中固体加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变为蓝色. |
探究活动二:探究铜生锈的条件
(进行实验2)
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 
| 在干燥环境中,铜不易生锈. | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是___. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是___. |
| 实验2 | 
| ___. |
| 实验3 | 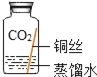
| ___. |
| 实验4 | 
| 铜生锈的条件是___. |
-
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.
探究活动一:验证铜锈的组成
(查阅资料)
①铜锈为绿色,其主要成分是Cu2(OH)2CO3.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应.
④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
(进行实验1)
同学们设计了如图所示装置并进行实验.
| 
实验操作 | 实验现象 | 实验结论 |
| ①按上图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有__;铜锈由___元素组成;烧杯中发生反应的化学方程式为___. |
| ③冷却后,向试管中固体加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变为蓝色. |
探究活动二:探究铜生锈的条件
(进行实验2)
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 
| 在干燥环境中,铜不易生锈. | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是___. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是___. |
| 实验2 | 
| ___. |
| 实验3 | 
| ___. |
| 实验4 | 
| 铜生锈的条件是___. |
-
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.
探究活动一:验证铜锈的组成
(查阅资料)
①铜锈为绿色,其主要成分是Cu2(OH)2CO3.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应.
④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
(进行实验1)
同学们设计了如图所示装置并进行实验.
| 
实验操作 | 实验现象 | 实验结论 |
| ①按上图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有__;铜锈由___元素组成;烧杯中发生反应的化学方程式为___. |
| ③冷却后,向试管中固体加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变为蓝色. |
探究活动二:探究铜生锈的条件
(进行实验2)
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 
| 在干燥环境中,铜不易生锈. | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是___. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是___. |
| 实验2 | 
| ___. |
| 实验3 | 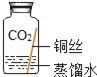
| ___. |
| 实验4 | 
| 铜生锈的条件是___. |
-
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.

探究活动一:验证铜锈的组成
【査阅资料】①铜锈为绿色,其主要成分是Cu2(OH)2CO3.②白色的硫酸铜粉末遇水能变为蓝色.③碳不与稀硫酸反应.④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
【进行实验1】同学们设计了如图所示装置并进行实验.
| 实验橾作 | 实验现象 | 实验结论 |
| ①按如图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有 ; 铜绣由 元素组成; 烧杯中发生反应的化学方程式为 . |
| ③冷却后,向试管中固体 加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变 为蓝色. |
【进行实验2】同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 
| 在干燥环境中,铜不易生锈 | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是 . (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是 |
| 实验2 | 
| |
| 实验3 | 
| |
| 实验4 | 
| 铜生锈的条件是 |
-
某些铜制品在空气中久置,表面会生成绿色的铜锈(又称铜绿)。某化学兴趣小组设计并进行如下实验,以探究铜锈的组成和铜生锈的条件。
Ⅰ.探究铜锈的组成
(查阅资料)①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
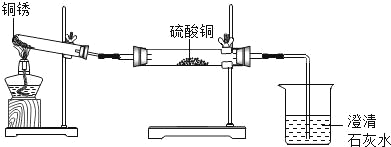
(进行实验)兴趣小组同学从铜器上取下适量的干燥铜锈,按下图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。
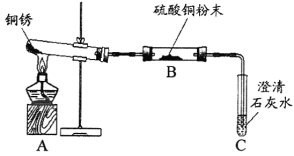
(解释与结论)
(1)C中反应的化学方程式为_________________。
(2)依据以上现象分析,铜锈中一定含有的元素为铜和________(填元素名称)。
Ⅱ.探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
(进行实验)兴趣小组同学取直径、长度均相同的铜丝,打磨光亮,并设计了如下图所示的5个实验,一周后观察到的实验现象如下表:
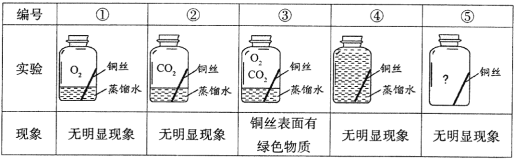
(解释与结论)
(3)实验中都使用了经煮沸并迅速冷却的蒸馏水,“煮沸并迅速冷却”的目的是_____________。
(4)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是___________(填编号)。
(5)对比实验②和③,得出的结论是_____________。
(6)为验证猜想,请在图中将实验⑤补充完整_____________。
(7)由上述实验可推知,铜生锈的条件是_____________。
(反思与应用)
(8)结合上述实验,你对日常生活中保存铜制品的建议是_____________。
-
某些铜制品在空气中久置,表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜锈的组成和铜生锈的条件。
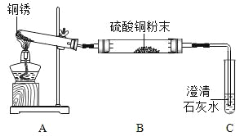
Ⅰ. 探究铜锈的组成
(查阅资料)①铜锈受热易分解②硫酸铜粉末遇水由白色变为蓝色
(进行实验)小组同学从铜器上取下适量的干燥铜锈,按如图所示装置实验(部分夹持装置已略去)。观察到 B 中白色粉末变为蓝色,C 中澄清石灰水变浑浊。
(解释与结论)(1)C 中反应的化学方程式是__________。
(2)依据以上现象分析,铜锈中一定含有的元素:Cu 和_________。
Ⅱ.探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示5个实验并持续观察。
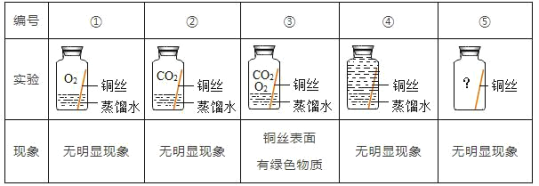
(解释与结论)
(3)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是___________。
(4)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_______(填编号)。
(5)对比实验②和③,得出的结论是________。
(6)为验证猜想,请在图中将实验⑤补充完整___________。
(7)由上述实验可推知,铜生锈的条件是_____________。
(反思与应用)
(8)结合上述实验,你对保存铜制品的建议是__________________。
-
某些铜制品在空气中久置,表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜锈的组成和铜生锈的条件。
I.探究铜锈的组成
(查阅资料)①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
(进行实验)小组同学从铜器上取下适量的干燥铜锈,按图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。
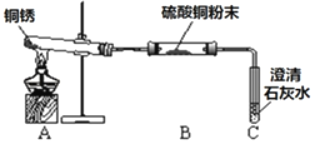
(解释与结论)依据以上现象分析,铜锈中一定含有的元素:Cu和_____。
II.探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
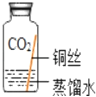
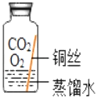
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如图所示的5个实验并持续观察。
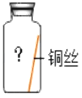
| 编号 | ① | ② | ③ | ④ | ⑤ |
| 实验 | 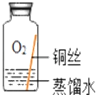
| 
| 
| 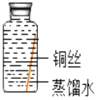
| 
|
| 现象 | 无明显现象 | 无明显现象 | 铜丝表面 有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
(1)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是_____。
(2)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验②和③,得出的结论是_____。
(4)为验证猜想,实验⑤的集气瓶中的气体是_____。
(5)由上述实验可推知,铜生锈的条件是_____。
(反思与应用)
(6)防止金属锈蚀的方法是_____(写一种)。
-
某些铜制品在空气中久置。表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜锈的组成和铜生锈的条件。
I.探究铜锈的组成
[查阅资料]①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
[进行实验]小组同学从铜器上取下适量的干燥铜锈,按如图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。
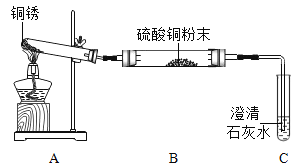
[解释与结论](1)依据以上现象分析,铜锈中一定含有的元素: Cu、O、_____
II.探究铜生锈的条件
[提出猜想]根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
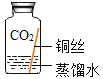
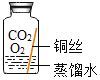
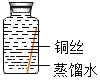
[进行实验]实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
| 编号 | ① | ② | ③ | ④ | ⑤ |
| 实验 | 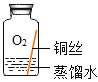
| 
| 
| 
| 
|
| 现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
[解释与结论]
(2)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验②和③,得出的结论是_____。
(4)为验证猜想,请在图中将实验⑤补充完整。补充的物质应为_____。
(5)由上述实验可推知,铜生锈的条件是_____。
-
某些铜制品在空气中久置,表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜锈的组成和铜生锈的条件。
I.探究铜锈的组成
(查阅资料)①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
(进行实验)小组同学从铜器上取下适量的干燥铜锈,按如图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。
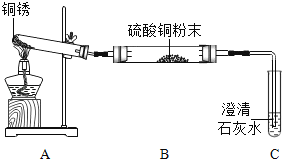
(解释与结论)(1)C中反应的化学方程式是_____。
(2)依据以上现象分析,铜锈中一定含有的元素:Cu和_____。
II.探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
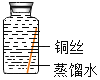
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
| 编号 | ① | ② | ③ | ④ | ⑤ |
| 实验 | 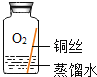
| 
| 
| 
| 
|
| 现象 | 无明显现象 | 无明显现象 | 铜丝表面 有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
(3)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是_____。
(4)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(5)对比实验②和③,得出的结论是_____。
(6)为验证猜想,请在图中将实验⑤补充完整______________。
(7)由上述实验可推知,铜生锈的条件是_____。
(反思与应用)
(8)结合上述实验,你对保存铜制品的建议是_____。









































