钯是1803年英国化学家武拉斯顿从铂矿中发现的化学元素,它是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。下列说法错误的是()
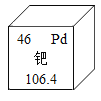
A.钯属于金属元素
B.钯原子的核外电子数为46
C.钯的元素符号是Pd
D.钯的相对原子质量是106.4 g
九年级化学单选题中等难度题
钯是1803年英国化学家武拉斯顿从铂矿中发现的化学元素,它是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。下列说法错误的是()

A.钯属于金属元素
B.钯原子的核外电子数为46
C.钯的元素符号是Pd
D.钯的相对原子质量是106.4 g
九年级化学单选题中等难度题
钯是1803年英国化学家武拉斯顿从铂矿中发现的化学元素,它是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。下列说法错误的是()

A.钯属于金属元素
B.钯原子的核外电子数为46
C.钯的元素符号是Pd
D.钯的相对原子质量是106.4 g
九年级化学单选题中等难度题查看答案及解析
钯是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。其元素相关信息如下图所示,下列说法不正确的是

A.钯属于金属元素
B.钯的相对原子质量为106.4
C.金属钯的化学式为Pd2
D.钯原子的核外电子数为46
九年级化学单选题简单题查看答案及解析
(一)铝及其化合物是我们日常生活中不可缺少的物质,如航空航天材料—硬铝。
(1)Al和CuSO4溶液反应的化学方程式为____,该反应说明____;
(2)生活中铝比铁更耐腐蚀的原因____(用化学反应方程式解释)。
(二)某学生在学习盐的性质时做了氯化铝溶液和氢氧化钠溶液反应的实验。该学生向氯化铝溶液中逐滴滴加氢氧化钠溶液时,发现溶液中有沉淀生成,且沉淀量先增多后减少直至消失。经查资料知:
Al(OH)3是一种两性氢氧化物,它既可以与酸反应又可以与碱反应都生成盐和水。它与碱反应的化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O,NaAlO2可溶于水。
(1)该学生将100.0g53.4%的AlCl3溶液和100.0gNaOH溶液混合,充分反应后过滤得到27.3g沉淀,则所加NaOH溶液的质量分数为__。
(2)该学生另将ag硬铝(Mg、Al、Cu、Si合金)溶于200.0g盐酸中,充分反应后过滤,向滤液中逐滴滴加20.0%的NaOH溶液至过量,产生的沉淀与NaOH溶液的质量关系如下图:
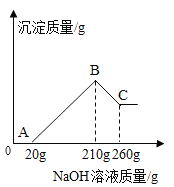
①O→A段的化学反应方程式为____;
②盐酸的质量分数是____。
九年级化学综合题困难题查看答案及解析
我国西南铝锻造厂采用物理冶金新技术代替了现行化学冶金,成功研制出性能更优越的航空航天工程的关键铝合金材料,将用于未来的空间站、新型运载火箭以及高速列车铝合金板。则回答:
(1)在地壳中,铝是含量最多的金属元素。下图是铝的原子结构示意图,铝原子的核电荷数为______,在化学反应中容易____(填“得到”或“失去”)电子,形成铝离子____(填符号).

(2)炼制时以氧化铝为原料,在熔融状态下电解生成铝和一种常见的气体,则反应的化学方程式为______________,该反应的基本类型为__________。
(3)金属矿物的储量有限,而且不能再生,据估计铝矿资源可供开采年限大概只有257年。下面几种做法中,可有效保护金属资源的是______(填序号)。
A 回收利用废旧金属制品 B 任意开采金属矿产资源
C 铝制品因抗腐蚀则可随意处置 D 寻找、开发金属的代用品
九年级化学填空题简单题查看答案及解析
铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、 船舶及化学工业中已大量应用。工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入。已知某铝合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对铝合金粉末中铁、铜的存在情况进行了探究。
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水); Fe、Cu不与氢氧化钠溶液反应。
猜想1:该合金粉末中除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有铜。
猜想3:该合金粉末中除铝外,还含有铁、铜。
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的___________,充分反应后过滤,滤渣备用。 | 粉末部分溶解,并有气体放出。 | 合金中一定含有________ 。 |
| ②取步骤①所得滤渣,加过量的___________,充分反应。 | 滤渣部分溶解,并有气体放出,溶液呈浅绿色。 | 合金中一定含有_________ 。 |
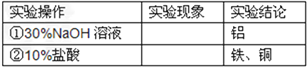
【探究结论】猜想 _________成立。
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。写出铝与稀盐酸反应的化学方程式 ___________________。
【拓展与分析】
为了验证铝、铁的金属活动性强弱,小刘同学设计了如下实验方案:把表面积相同的铝丝和铁片同时投入到相同体积的稀盐酸中,比较反应的剧烈程度。请你评价该方案在操作过程中和控制变量上的不足之处。
操作过程中的不足之处___________________。
控制变量上的不足之处________________________。
请你再设计一种不同类型的实验方案,验证铝、铁的金属活动性强弱。________________。
九年级化学科学探究题中等难度题查看答案及解析
铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用。工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入。已知某合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究。
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应。
猜想1:该合金粉末中除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有___________(填名称)。
猜想3:该合金粉末中除铝外,还含有铁、铜。
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的_______________,充分反应后过滤,滤渣备用。 | 粉末部分溶解,并有气体放出。 | 合金中一定含有__________。 |
| ②取步骤①所得滤渣,加过量的______________,充分反应。 | 滤渣部分溶解,并有气体放出,溶液呈浅绿色。 | 合金中一定含有__________。 |
探究结论:猜想__________成立。
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。写出铝与稀盐酸反应的化学方程式________________________________。
【拓展与分析】
请设计两个不同的实验方案,验证铝、铜的金属活动性强弱。
方案一:__________________。
方案二:_____________。
【总结归纳】由上述实验得出比较金属活动性强弱的方法有:
①_________________;②___________________。
九年级化学科学探究题困难题查看答案及解析
铝合金材料在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用。用铝土矿(含有Al2O3)与NaOH溶液反应可以得到NaAlO2,NaAlO2被CO2酸化生成Al(OH)3,Al(OH)3受热分解生成Al2O3和H2O。
(1)铝合金材料属于___________。(填选项)
A.单质 B.化合物 C.纯净物 D.混合物
(2)Al2O3+2NaOH====2NaAlO2+___________。
(3)HAlO2读作偏铝酸,则NaAlO2读作__________ 。
(4)NaAlO2中铝元素的化合价为___________。
(5)Al(OH)3受热分解的化学方程式为________________________________。
(6)电解熔融的Al2O3可以制得Al和O2,其基本反应类型为_____________________。
九年级化学填空题中等难度题查看答案及解析
稀土是一类重要的金属资源,有“工业维生素”的美誉。广泛应用于新能源、新材料、航空航天、电子信息等尖端科技领域。我国是稀土资源大国。据估算,目前我国稀土产量约占世界80%左右。
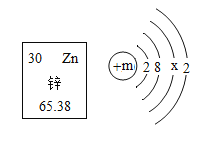
结合信息回答下列问题。
(1)金属材料包括纯金属和它们形成的_____;
(2)如图是锌元素有关信息及原子结构示意图,则锌元素位于元素周期表第_____周期,图中x的值为_____;
(3)铁制品表面镀锌是防止铁生锈的方法之一。从铁制品生锈的条件来看,镀锌能防锈的原因是_____;
(4)下图是几种常见元素的原子结构示意图。
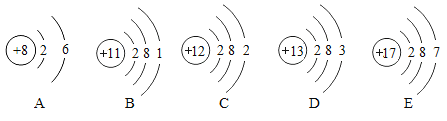
①上述元素中,金属活动性最强的是_____(填元素符号)。
②A.D形成的化合物化学式为_____;
(5)关于稀土资源,下列说法错误的是_____;
a.稀土属于不可再生资源
b.我国稀土资源丰富,可任意开采
c.回收利用是保护稀土资源的重要途径
d.稀土开采与生产过程中要防止生态破坏
九年级化学填空题简单题查看答案及解析
九年级化学选择题中等难度题查看答案及解析
中国航天科技一直以来备受世界瞩目。2017年9月2日,我国成功提纯了“超级金属”铼。铼及其合金被广泛应用到航空航天领域。金属铼硬度大,熔点很高,在高温下能与硫化合形成二硫化铼。如图为铼在元素周期表中的信息。请结合图5回答:

(1)铼的相对原子质量是_______。
(2)二硫化铼的化学式是______,七氧化二铼(Re2O7)是铼最常见的氧化物,其中铼元素的化合价为_______。
(3)上述信息中,属于金属铼的物理性质的是_________。
九年级化学填空题简单题查看答案及解析