-
金属钴(Co)在国防工业中有重要应用。在实验室用硫酸酸浸的方法从钴矿石中提取钴元素,并探究最佳提取条件。
(查阅资料)酸浸时发生如下反应:
① CoO + H2SO4 === CoSO4 + H2O
② 2Co2O3 + 4H2SO4 === 4CoSO4 + O2↑ + 4H2O
③ Co2O3 + 2H2SO4 + Na2SO3 === 2CoSO4 + 2H2O + Na2SO4
反应①~③中,化合价发生改变的元素有________。
(进行实验)将矿石在一定条件下酸浸4小时,测量钴元素的浸出率。部分数据如下:
实验
矿石用量/g
硫酸用量/g
Na2SO3用量/g
温度/℃
钴元素的浸出率/%
1
85.71
12.62
0
85
56.39
2
85.71
6.31
0
85
49.98
3
85.71
6.31
0
65
43.33
4
85.71
6.31
0.43
65
73.95
5
85.71
6.31
0.86
65
74.77
(解释与结论)
(1)对比实验1和2,可得出的结论是___________。
(2)欲得出“其他条件不变,Na2SO3用量对钴元素的浸出率有影响”的结论,需要对比的实验是____________(填序号)。
(3)由上述实验可知,影响钴元素浸出率的因素有______________。
(反思与评价)
(4)工业生产中采用实验__________(填序号) 的提取条件更合理。
九年级化学科学探究题简单题查看答案及解析
-
金属钴(Co)在国防工业中有重要应用。某矿石中含钻的氧化物(CoO、Co2O3)研究人员在实验室用硫酸酸浸的方法提取钴元素,并探究最佳提取条件。
(1)写出下列化合物中Co元素的化合价:CoO_________,Co2O3______________。(2)酸浸时钴的氧化物发生如下反应:
反应I CoO+H2SO4=CoSO4+H2O
反应Ⅱ 2Co2O3+4H2SO4=4CoSO4+O2↑+4H2O
反应Ⅲ Co2O3+2H2SO4+Na2SO3=2CoSO4+2H2O+Na2SO4
①反应后溶液中含钴元素的微粒是_________ (填化学符号)
②已知反应前矿石中CoO的质量为ag,Co2O3的质量为bg,则理论上可以生成CoSO4____g(用含a、b的式子表示)
(3)为探究最佳提取条件,将矿石在一定条件下酸浸4小时,测量钴元素的浸出率部分数据如下:
编号
矿石用量(g)
硫酸用量(g)
Na2SO3用量(g)
温度(℃)
钻元素浸出率(%)
1
85.71
12.62
0
85
56.39
2
85.71
6.31
0
85
49.98
3
85.71
6.31
0
65
43.33
4
85.71
6.31
0.43
65
73.95
5
85.71
6.31
0.86
65
74.77
①本实验研究了哪些因素对钴元素浸出率的影响__________________________________;
②根据上表数据,其他条件不变,温度升高,钴元素的浸出率___________________________;
③工业生产中采用实验______________(填编号)的提取条件更合理。
九年级化学综合题中等难度题查看答案及解析
-
金属钴(Co)在国防工业中有重要应用。某矿石中含钻的氧化物(CoO、Co2O3)研究人员在实验室用硫酸酸浸的方法提取钴元素,并探究最佳提取条件。
(1)写出下列化合物中Co元素的化合价:CoO_________,Co2O3______________。(2)酸浸时钴的氧化物发生如下反应:
反应I CoO+H2SO4===CoSO4+H2O
反应Ⅱ 2Co2O3+4H2SO4===4CoSO4+O2↑+4H2O
反应Ⅲ Co2O3+2H2SO4+Na2SO3===2CoSO4+2H2O+Na2SO4
①反应后溶液中含钴元素的微粒是_________ (填化学符号)
②已知反应前矿石中CoO的质量为ag,Co2O3的质量为bg,则理论上可以生成CoSO4____g(用含a、b的式子表示)
(3)为探究最佳提取条件,将矿石在一定条件下酸浸4小时,测量钴元素的浸出率部分数据如下:

①本实验研究了哪些因素对钴元素浸出率的影响__________________________________;
②根据上表数据,其他条件不变,温度升高,钴元素的浸出率___________________________;
③工业生产中采用实验______________(填编号)的提取条件更合理。
九年级化学综合题中等难度题查看答案及解析
-
蔗糖是应用最广泛的食品添加剂,也是食品工业的重要原料。实验小组对蔗糖的元素组成进行研究。
(查阅资料)
蔗糖是一种有机化合物,能与浓硫酸(H2SO4)反应,可以燃烧,受热易分解。
(进行实验)
实验方案
实验步骤
实验现象
初步分析
方案1
与浓硫酸反应

蔗糖由白色变成黑色,体积膨胀,变蓬松,有刺激性气味气体生成
生成C和SO2
方案2在空气中点燃

干冷烧杯内壁有雾产生,澄清石灰水变浑浊
生成H2O和CO2
方案隔绝氧气加热

蔗糖由白色变成黑色,烧杯内壁有雾产生
____。
(解释与结论)
(1)方案1,分析生成了SO2,从元素守恒角度说明理由________。
(2)方案1可证明蔗糖中一定含有的元素是________。
(3)方案3, 初步分析生成的物质中有________。
(4)能证明蔗糖中一定含有碳和氧元素的实验方案是________。
(反思与评价)
(5)利用方案2,测定蔗糖分子中原子的个数比,需要测定________的质量。
(6)关于以上实验的下列说法中,正确的是________。
A 方案1中生成的大量气体只含有SO2
B 方案2中倒扣的烧杯能收集到CO2
C 方案3中先通入氮气再点燃酒精灯
九年级化学科学探究题中等难度题查看答案及解析
-
(7分)科学探究是学习化学常用的一种重要方法,下面某校化学兴趣小组同学的探究过程.
[发现问题] 加热铜与浓硫酸的混合物,能生成一种无色有刺激性气味的气体和蓝色溶液。
[查阅资料] ① 某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成二氧化硫和铜盐。
② 硫酸铜溶液呈酸性。
[知识回顾] 铜、银________(填能或不能)与稀硫酸反应产生氢气。
[分析讨论]
(1)对于生成的蓝色溶液,小东认为可能是Cu(NO3)2溶液,小楠认为不可能是Cu(NO3)2溶液,而应该是硫酸铜溶液,小楠的理由是。
(2)写出铜与浓硫酸共热的化学方程式________。
(3)小东根据化学方程式说,该方法适用于以铜为原料大量制取硫酸铜,小田认为不适宜,你能说出小田的一个理由吗________。
[提出问题]上述蓝色溶液中有无硫酸剩余?
[讨论交流]
①小坤认为可向蓝色溶液中滴加氯化钡溶液,观察有无沉淀产生,经大家讨论后该方案被否定,你觉得否定该方案的理由是________。
②小东同学认为可以直接用石蕊试液来进行检验。小田认为不对,她的理由是________。
[反思评价]同学们又发现:将足量的铜和一定量的浓硫酸置于容器中加热,反应一段时间后,会逐渐变慢,最后停止,其中可能的原因是________。
九年级化学探究题中等难度题查看答案及解析
-
为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
(查阅资料)碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;铜不能与稀硫酸反应。氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+H2SO4═CuSO4+H2O+Cu。
(进行实验)实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
序号
1﹣1
1﹣2
装置


反应后物质的颜色、状态
黑色粉末中混有少量红色固体
红色固体有金属光泽,混有极少量黑色物质
实验2:取一定量的混合物,用1﹣2装置进行实验。
序号
木炭粉与氧化铜的质量比
反应后物质的颜色、状态
2﹣1
1:9
红色固体有金属光泽
混有少量黑色物质
2﹣2
1:10
混有很少量黑色物质
2﹣3
1:11
混有极少量黑色物质
2﹣4
1:12
无黑色物质
2﹣5
1:13
混有较多黑色物质
(解释与结论)
(1)氧化铜是_____色固体。
(2)①配平化学方程式:C+_____CuO
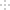 _____Cu+____CO2↑。
_____Cu+____CO2↑。②该反应前后化合价发生改变的元素是:_______。
(3)实验1﹣2中,证明产生了CO2的现象是_____。
(4)实验1的目的是_____。
(5)实验2的结论是_____。
(反思与评价)
(6)实验2没有进行质量比为1:14的实验,理由是_____。
(7)为检验2﹣4的红色固体中是否含Cu2O,所需试剂是_____。
九年级化学科学探究题中等难度题查看答案及解析
-
科学探究是学习化学常用的一种重要方法,下面某校化学兴趣小组同学的探究过程.
【发现问题】
加热铜与浓硫酸的混合物,能生成一种无色有刺激性气味的气体和蓝色溶液.
【查阅资料】
①某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成二氧化硫和铜盐.②硫酸铜溶液呈酸性.
【知识回顾】
铜、银______(填能或不能)与稀硫酸反应产生氢气.
【分析讨论】
(1)对于生成的蓝色溶液,小东认为可能是Cu(NO3)2溶液,小楠认为不可能是Cu(NO3)2溶液,而应该是硫酸铜溶液,小楠的理由是______.
(2)写出铜与浓硫酸共热的化学方程式______ CuSO4+2H2O+SO2↑九年级化学解答题中等难度题查看答案及解析
-
科学探究是学习化学常用的一种重要方法,下面某校化学兴趣小组同学的探究过程.
【发现问题】
加热铜与浓硫酸的混合物,能生成一种无色有刺激性气味的气体和蓝色溶液.
【查阅资料】
①某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成二氧化硫和铜盐.②硫酸铜溶液呈酸性.
【知识回顾】
铜、银______(填能或不能)与稀硫酸反应产生氢气.
【分析讨论】
(1)对于生成的蓝色溶液,小东认为可能是Cu(NO3)2溶液,小楠认为不可能是Cu(NO3)2溶液,而应该是硫酸铜溶液,小楠的理由是______.
(2)写出铜与浓硫酸共热的化学方程式______ CuSO4+2H2O+SO2↑九年级化学解答题中等难度题查看答案及解析
-
科学探究是学习化学常用的一种重要方法,下面某校化学兴趣小组同学的探究过程.
【发现问题】
加热铜与浓硫酸的混合物,能生成一种无色有刺激性气味的气体和蓝色溶液.
【查阅资料】
①某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成二氧化硫和铜盐.②硫酸铜溶液呈酸性.
【知识回顾】
铜、银______(填能或不能)与稀硫酸反应产生氢气.
【分析讨论】
(1)对于生成的蓝色溶液,小东认为可能是Cu(NO3)2溶液,小楠认为不可能是Cu(NO3)2溶液,而应该是硫酸铜溶液,小楠的理由是______.
(2)写出铜与浓硫酸共热的化学方程式______ CuSO4+2H2O+SO2↑九年级化学解答题中等难度题查看答案及解析
-
科学探究是学习化学常用的一种重要方法,下面某校化学兴趣小组同学的探究过程.
【发现问题】
加热铜与浓硫酸的混合物,能生成一种无色有刺激性气味的气体和蓝色溶液.
【查阅资料】
①某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成二氧化硫和铜盐.②硫酸铜溶液呈酸性.
【知识回顾】
铜、银______(填能或不能)与稀硫酸反应产生氢气.
【分析讨论】
(1)对于生成的蓝色溶液,小东认为可能是Cu(NO3)2溶液,小楠认为不可能是Cu(NO3)2溶液,而应该是硫酸铜溶液,小楠的理由是______.
(2)写出铜与浓硫酸共热的化学方程式______ CuSO4+2H2O+SO2↑九年级化学解答题中等难度题查看答案及解析