-
半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和水蒸气。半水煤气经过下列步骤转化为合成氨的原料。

(1)在铜作催化剂的条件下,半水煤气实现CO的转化,其反应的微观示意图如下:

①该反应的化学方程式为_______________________。
②关于铜作为催化剂,下列说法正确的是______(填字母序号)。
A.不加入铜,该反应就不能进行
B.铜可以作为任何化学反应的催化剂
C.加入铜的目的是为了提高该反应的速率
(2)合成的氨气可以用来制造化肥硝酸铵(NH4NO3),该肥料属于化学肥料中的______肥。
-
半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2 和H2O(g)。半水煤气经过下列步骤转化为合成氨的原料N2和H2。

(1)在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应实现了 CO 变换,其化学方程式为:________。
(2)吸收法是脱除CO2的方法之一。已知:
| 溶质 | Na2CO3 | K2CO3 |
| 20℃1L饱和溶液中溶质的物质的量mol | 2.0 | 8.0 |
| 溶质价格(元/kg) | 1.25 | 9.80 |
若选择Na2CO3溶液作吸收液,其优点是_;缺点是_。如果选择K2CO3溶液作吸收液,用某种方法可以降低成本,写出这种方法涉及的化学方程式:_。
(3)将一定体积半水煤气依次通过装置Ⅰ~Ⅴ(最后通入氮气确保反应、吸收完全),可以 测定其中H2以及 CO 的物质的量。

可供选用的装置如下所示(省略夹持仪器):

为装置Ⅰ~Ⅴ选择合适的装置与试剂:
| 装置 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| a | a | _ | _ | b |
| 试剂 | _ | 浓硫酸 | CuO | _ | _ |
装置Ⅰ、Ⅱ的作用是____________。要确定半水煤气中H2物质的量,应测量的数据是______。
-
半水煤气的主要成分是H2、CO、CO2、N2和水蒸气。工业上用半水煤气合成氨(NH3)的过程如下所示。
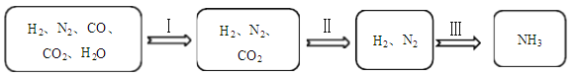
(1)过程Ⅰ中,反应为CO + H2O  H2 + CO2,其中属于氧化物的是__________。
H2 + CO2,其中属于氧化物的是__________。
(2)过程Ⅲ中,发生的化学反应属于基本反应类型中的______反应。
-
半水煤气的主要成分是H2、CO、CO2、N2和水蒸气。工业上用半水煤气合成氨(NH3)的过程如下所示。

(1)过程Ⅰ中,反应为CO + H2O  H2 + CO2,其中属于氧化物的是__________。
H2 + CO2,其中属于氧化物的是__________。
(2)过程Ⅲ中,发生的化学反应属于基本反应类型中的______反应。
-
工业上以半水煤气(主要成分是 N2、H2、CO、CO2和H2O)、食盐等为原料制取纯 碱的流程如图 1:
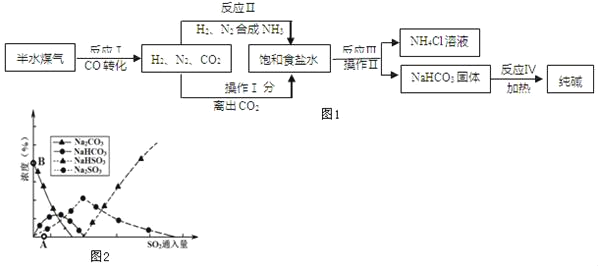
(1)反应Ⅰ是在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应,实现了 CO 转化,化学方程式是_____。
(2)将反应Ⅱ生成的 NH3和操作Ⅰ分离出的CO2通入饱和食盐水中即可得 NaHCO3固体,下列两种操作,你觉得更为合理的是_____。
a先通 NH3再通入CO2 b先通 CO2再通入 NH3
(3)操作Ⅱ的名称是_____,实验室进行该项操作时,需要用到的玻璃仪器有:普通漏斗、烧杯和_____,该仪器在此操作中的作用是_____。
(4)反应Ⅲ的成功实现说明该实验条件下,NaHCO3的溶解度_____(填“>”“<”或“=”)NH4Cl 的溶解度。
(5)纯碱用途广泛。工业上可用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2,制备无水Na2SO3,达到减少污染、节约资源的目的。反应过 程中溶液组成变化如图 2 所示。
①吸收初期(图2中A点以前)反应的化学方程式为_____。
②不断通入 SO2,最终产物是_____。
-
工业上以半水煤气(主要成分是 N2、H2、CO、CO2和H2O)、食盐等为原料制取纯 碱的流程如图 1:

(1)反应Ⅰ是在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应,实现了 CO 转化,化学方程式是_____。
(2)将反应Ⅱ生成的 NH3和操作Ⅰ分离出的CO2通入饱和食盐水中即可得 NaHCO3固体,下列两种操作,你觉得更为合理的是_____。
a先通 NH3再通入CO2 b先通 CO2再通入 NH3
(3)操作Ⅱ的名称是_____,实验室进行该项操作时,需要用到的玻璃仪器有:普通漏斗、烧杯和_____,该仪器在此操作中的作用是_____。
(4)反应Ⅲ的成功实现说明该实验条件下,NaHCO3的溶解度_____(填“>”“<”或“=”)NH4Cl 的溶解度。
(5)纯碱用途广泛。工业上可用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2,制备无水Na2SO3,达到减少污染、节约资源的目的。反应过 程中溶液组成变化如图 2 所示。
①吸收初期(图2中A点以前)反应的化学方程式为_____。
②不断通入 SO2,最终产物是_____。
-
以天然气为原料合成氨,并且进一步制备尿素和纯碱的主要步骤如图所示(图中某些转化步骤及生成物未列出):

根据以上流程图回答下列问题
(1)写出由水蒸气和甲烷造合成气的化学方程式;
(2)在合成氨的过程中,循环利用的物质有;
(3)写出合成尿素的化学方程式;
(4)在生产纯碱的过程中,能否将①②两个步骤颠倒?,为什么?.
-
如图是实验室提供的实验装置,以供下列各种实验选择.工业上使用的未经净化的水煤气中含有CO、H2、CO2和水蒸气.请你利用
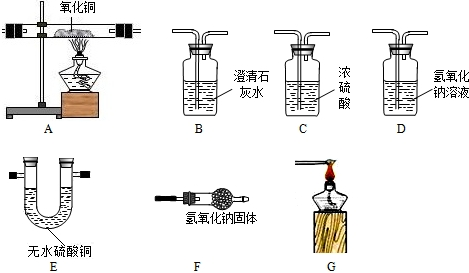
以上实验装置装配一套证明水煤气的主要成分是CO和H2的实验装置.
(1)若气体由左至右,则实验装置连接顺序一次是(用字母表示).
(2)各装置的作用依次是.
-
用水蒸气通过灼热的煤层制得水煤气,其主要成分是CO H2和少量CO2 H2O,如用下列装置设计一个实验,以证明水煤气中含有CO和H2.
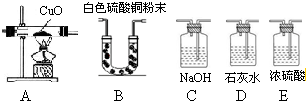
(1)水煤气通过上述装置的顺序应是______,
(2)气体经过C、D、E 装置时都应从(长管或短管)通入______,
(3)说明各装置的作用
A、______B、______C、______D、______E、______.
-
水煤气是一种工业上常用的气体燃料,一般用焦炭和水蒸气在高温下反应制得,含有少量的CO2和水蒸气杂质.某化学兴趣小组对水煤气的主要成分进行研究.
【查阅资料】
(1)白色的无水硫酸铜粉末遇水变成蓝色;
(2)Na2CO3与少量盐酸反应生成NaHCO3和NaCl,与过量盐酸反应时生成NaCl,H2O,CO2
【实验假设】
①可燃气只是CO
②可燃气体只是H2
③可燃气体是CO,H2的混合气.
【实验过程】
实验小组按以下流程进行实验(水煤气中CO2,H2O已被充分吸收);

实验中,发现黑色氧化铜变红,且______,证明水煤气含有H2;还观察到澄清石灰水变浑浊,证明水煤气含有另一可燃气体为______
【实验反思】
根据实验结论,甲同学认为实验应保证安全,防止中毒,对尾气的处理方法是______
【实验拓展】
(1)实验后,乙同学认为欲检验所用NaOH是否完全消耗,可向溶液中滴入几滴稀盐酸,若没有气体产生,则溶液中还有NaOH剩余,但丙同学认为乙同学的设计是错误的,理由是______
(2)丁同学通过本次实验,结合查阅的资料发现,不用任何其它试剂,只用试管和胶头滴管就可以鉴别稀盐酸和碳酸钠两种无色溶液.正确的鉴别方案及结论是______.












