-
侯德榜是中国化学工业先驱者,一生致力于化工事业,1943年他创立了“侯氏制碱法”,其核心原理是:NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl.工长里可将二氧化碳温室气体回收用于生产碳酸氢钠(NaHCO3).现有22kg二氧化碳完全参与反应,计算可制得多少千克的碳酸氢钠?(已知NaHCO3的相对分子质量84)
九年级化学计算题中等难度题查看答案及解析
-
侯德榜是中国化学工业先驱者,一生致力于化工事业,1943年他创立了“侯氏制碱法”,其核心原理是:工长里可将二氧化碳温室气体回收用于生产碳酸氢钠(NaHCO3).现有22kg二氧化碳完全参与反应,计算可制得多少千克的碳酸氢钠?
(已知NaHCO3的相对分子质量84)九年级化学解答题中等难度题查看答案及解析
-
(共4分)我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献.其生产工艺流程示意图如下:
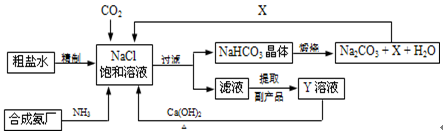
制碱原理可表示为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
(1)X的化学式为 .
(2)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,Y的化学式为 ,此反应产生的可循环利用的物质的名称为 .
(3)Y常用作氮肥使植物生长茂盛,叶色浓绿,现有用熟石灰改良过的酸性土壤需要施加氮肥, (填“可以”或“不可以”)使用Y.
九年级化学填空题中等难度题查看答案及解析
-
我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献.其生产工艺流程示意图如下:
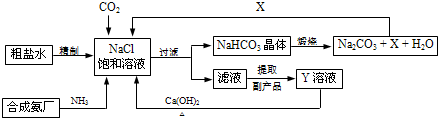
制碱原理可表示为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
(1)X的化学式为________.
(2)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,Y的化学式为________,此反应产生的可循环利用的物质的名称为________.
(3)Y常用作氮肥使植物生长茂盛,叶色浓绿,现有用熟石灰改良过的酸性土壤需要施加氮肥,________(填“可以”或“不可以”)使用Y.九年级化学填空题中等难度题查看答案及解析
-
我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如图:
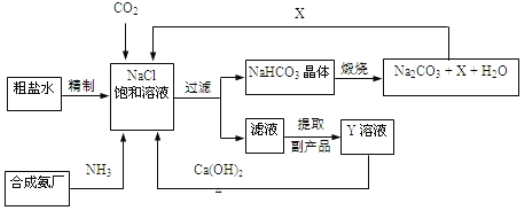
制碱原理中重要的一步反应表示为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
(1)粗盐水精制过程中需除去氯化钠中含有的可溶性杂质MgCl2、CaCl2、Na2SO4,现在有以下除杂操作 ①加入过量的Na2CO3溶液; ②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④加入适量的稀盐酸;⑤过滤。除杂时正确的操作顺序为:③_____。(填序号)过量的Na2CO3溶液的作用是_____。
(2)X的化学式为_____。
(3)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,Y的化学式为_____,此反应产生的可循环利用的物质的名称为_____。
(4)草木灰可作钾肥,现有一农田,生长的作物叶色发黄、茎秆细小。施肥时_____(填“可以”或“不可以”)同时施用Y和草木灰。
九年级化学流程题简单题查看答案及解析
-
我国制碱工业先驱侯德榜发明了“侯氏制碱法”,促进了世界制碱技术的发展。其主要化学反应原理如下:
NH3+CO2+H2O═NH4HCO3①
NaCl+NH4HCO3═NaHCO3↓+NH4Cl ②
x NaHCO3
Na2CO3+CO2↑+H2O ③
已知NaCl、NaHCO3和NH4Cl在不同温度下的溶解度数据如下表:
温度(℃)
0
10
20
30
40
溶解度/g
NaCl
35.7
35.8
36.0
36.3
36.6
NaHCO3
6.9
8.1
9.6
11.1
12.7
NH4Cl
29.4
33.3
37.2
41.4
45.8
请回答下列问题:
(1)反应①的基本反应类型属于_____反应。
(2)反应②产生的NH4Cl在农业生产中常用作_____(选填“氮肥”、“磷肥”或“钾肥”)。
(3)反应③中的化学计量数x=_____。
(4)20℃时,反应②中的生成物溶解度较小的是_____(填化学式)
(5)20℃时,将NaCl和NaHCO3的饱和溶液各100g,分别加热蒸发20g水,再恢复至原温度,析出晶体并得到溶液,对于所得溶液下列说法正确的是_____(填序号)
A、所得溶液仍是饱和溶液
B、所得溶液的质量前者大于后者
C、所得溶液的溶质质量分数都增大
九年级化学简答题简单题查看答案及解析
-
我国科学家侯德榜创立候氏制碱法为纯碱和化肥工业的发展做出了杰出贡献。下图1是候氏制碱法的反应原理,图2是相关物质的溶解度曲线,请结合图示回答下列问题:
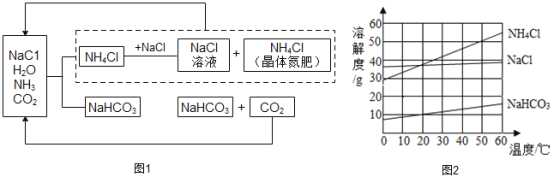
(1)制碱的主要反应原理:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3,生成的碳酸氢钠和氯化铵哪种物质首先析出?_______;理由是_______;
(2)该过程中除水外.能够循环利用的物质是_______;
(3)写出NaHCO3→Na2CO3 反应的化学方程式____________;
(4)50°C时,向100g水中加入55g氯化铵充分搅拌,所得溶液为____(填“饱和”或“不饱和”)溶液;
(5)60°C时,向等质量的氯化钠、碳酸氢钠、氯化铵中,分别加人水配成饱和溶液,所得溶液的质量由小到大的顺序是_______。
九年级化学流程题中等难度题查看答案及解析
-
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出突出的贡献。以NH3、CO2、NaCl 等为原料先制得NaHCO3, 进而生产纯碱。该生产工艺的一个反应原理为:
。现用如下图所示装置和上述原理制取碳酸氢钠晶体,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去。
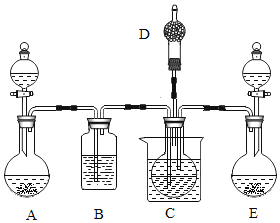
制取碳酸氢钠晶体可供选用的药品有:①石灰石②生石灰③浓盐酸④稀盐酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液。
请回答下列问题:
(1)A中所选用的药品为①和_________(填序号,下同),发生反应的化学方程式为________;
(2)B中应选用的药品是________,作用是____________。
(3)E中产生NH3气体,所选用的药品为____________,能顺利产生氨气的原因是________。
(4)在实验过程中,应先向C中通入的气体的化学式是________,其原因是_____________。
(5)由E向C装置通气的导管不能插入液面以下的原因是____________________。
(6)“侯氏制碱法”最后一步用NaHCO3制备纯碱的化学方程式为____________。
九年级化学科学探究题困难题查看答案及解析
-
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),反应原理为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3(析出),促进了世界制碱技术的发展。下列说法正确的是( )
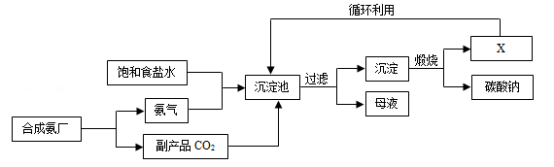
A. 沉淀池中的反应物共含有4种元素
B. 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀
C. 图中X可能是氨气
D. 过滤得到的“母液”中一定只含有两种溶质
九年级化学选择填充题困难题查看答案及解析
-
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),反应原理为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3(析出),促进了世界制碱技术的发展。下列说法正确的是( )
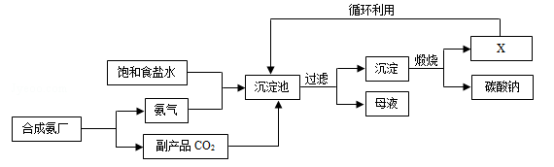
A. 沉淀池中的反应物共含有4种元素
B. 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀
C. 图中X可能是氨气
D. 过滤得到的“母液”中一定只含有两种溶质
九年级化学选择填充题困难题查看答案及解析