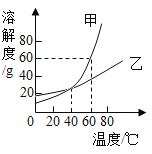
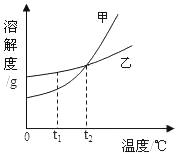
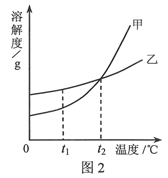
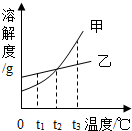
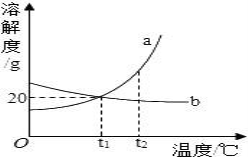
根据下图所示的溶解度曲线判断,下列说法正确的是( )
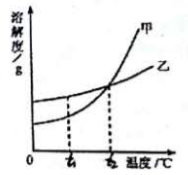
A. 甲物质的溶解度大于乙物质的溶解度
B. 甲物质的不饱和溶液温度升高后变成饱和溶液
C. t2℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有相等质量的溶质
D. 将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体
【答案】D
【解析】A、由于固体物质的溶解度会随温度的变化而变化,从图中可以看出,只有在高于t2℃时,甲的溶解度大于乙的溶解度,错误;B、甲的溶解度随着温度的升高而增大,物质甲的不饱和溶液温度升高后仍为不饱和溶液,错误;C、由于甲乙两饱和溶液的质量不一定相等,故无法比较所含溶质的质量,错误;D、甲乙的溶解度都随着温度的降低而减小,故将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体,正确。故选C。
点睛:对于溶解度的意义的表达一般有两种方式:一种是在某温度时,100g水里最多能溶解多少克某物质;另一种是在某温度时,100g水里溶解多少克某物质,溶液达到饱和状态。
【题型】单选题
【结束】
28
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如下图所示。根据图中所提供的信息,得出的结论正确的是( )(A、B、C在生成物中均为+2价)

A. 消耗稀盐酸的质量是:A>B>C B. 金属活动性顺序是A>B>C
C. 反应速率最快的是A D. 相对原子质量的大小关系是A>B>C
【答案】A
【解析】A、根据质量守恒定律可知,氢元素全部来自酸,生成氢气的质量A>B>C,所以消耗稀盐酸的质量是A>B>C,正确;B、根据反应生成H2的质量与反应时间的关系图所示,当三种金属都在发生反应时,相同时间内B放出氢气的质量大于A、大于C,可判断三种金属中B的活动性最强;错误;C、根据反应生成H2的质量与反应时间的关系图所示,等质量的三种金属B最先完全反应,因此反应速度最大的是B而不是A;错误;D、三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是A>B>C;因此可判断相对原子质量是C>B>A,错误。故选A。
点睛:对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比。
【题型】单选题
【结束】
29
将等质量的镁、铁、锌分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2的质量与反应时间的关系如图所示.根据图中的信息,作出的判断不正确的是( )

A. 图线X表示镁的反应情况
B. 铁消耗的稀盐酸的质量最大
C. 镁、锌一定过量,铁可能反应完
D. 镁一定过量,锌、铁可能反应完
九年级化学单选题中等难度题