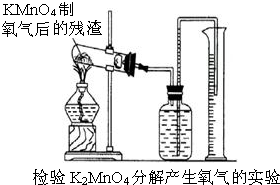
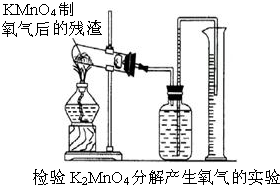
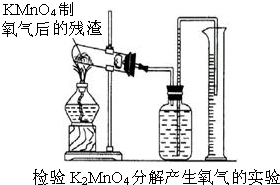
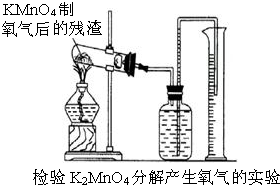
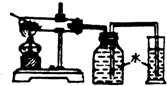
由实验测知:取3.5gKMnO4晶体加热到220°C,分解放出的氧气多于按下式计算的理论量.按下式计算的理论量为放出氧气0.354g,2KMnO4 K2MnO4+MnO2 +O2↑(溶于水呈紫红色)(溶于水呈绿色) (黑色,不溶)
K2MnO4+MnO2 +O2↑(溶于水呈紫红色)(溶于水呈绿色) (黑色,不溶)
换算成标准状况下的体积为248mL,而实际测得的氧气为308mL(标准状况),超过理论量为:(308-248)m1,=60mL.
试回答:
(1)怎样用实验证明:超理论量的氧气不是来自MnO2?______
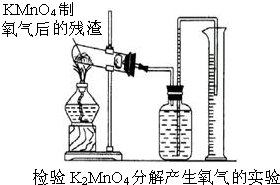
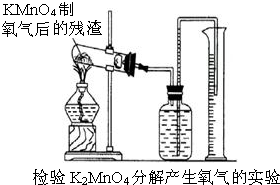
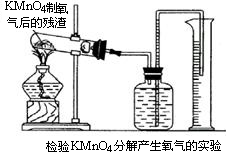
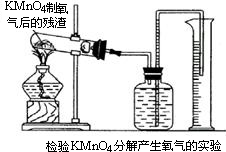
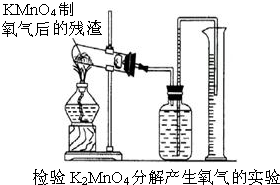
(2)怎样用实验证明超理论量的氧气是由K2MnO4分解产生的?(要求用KMnO4制取氧气后的残渣实验,如图所示.)______
(3)怎样从“最后残渣”中分离出MnO2?______.
换算成标准状况下的体积为248mL,而实际测得的氧气为308mL(标准状况),超过理论量为:(308-248)m1,=60mL.
试回答:
(1)怎样用实验证明:超理论量的氧气不是来自MnO2?______
(2)怎样用实验证明超理论量的氧气是由K2MnO4分解产生的?(要求用KMnO4制取氧气后的残渣实验,如图所示.)______
(3)怎样从“最后残渣”中分离出MnO2?______.

九年级化学解答题中等难度题