-
(2010•海珠区一模)金属在生产、生活中都有着广泛的应用.
(1)下列说法正确的是______.
A.钢的性能比纯铁好
B.铝合金比纯铝的硬度大
C.金属都是银白色的固体,具有良好的导电性和导热性
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:

请写出②、③反应的化学方程式:
②______ 2CO
-
金属在生产、生活中都有着广泛的应用.
(1)下列说法正确的是______.
A.钢的性能比纯铁好
B.铝合金比纯铝的硬度大
C.金属都是银白色的固体,具有良好的导电性和导热性
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:

请写出②、③反应的化学方程式:
②______ 2CO
-
金属在生产、生活中都有着广泛的应用。
(1)下列说法正确的是________。
A.钢的性能比纯铁好
B.铝合金比纯铝的硬度大
C.金属都是银白色的固体,具有良好的导电性和导热性
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:
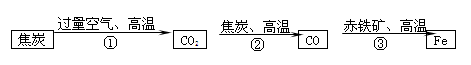
请写出②、③反应的化学方程式:
②_____________________________________ ____;
③______________________________________ ___。
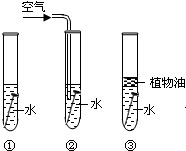
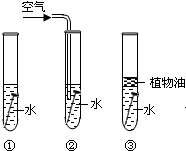
(3)生活中铁制品容易锈蚀,某课外学习小组探究铁生锈的条件,用洁净无锈的铁钉、试管、经煮沸迅速冷却的蒸馏水、植物油、棉花和干燥剂氯化钙,实验装置图如下。
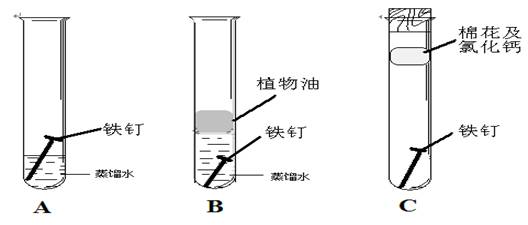
一周后观察到只有A中的铁钉生锈,而B、C中铁钉均无变化,请回答下列问题:
①蒸馏水需要煮沸并迅速冷却的原因是________ 。
②设计实验B的目的是________;设计实验C的目的是________。
③由A、B、C三支试管中的实验现象可以得到铁钉锈蚀的条件是________
________。
(4)请你写出一种防锈措施。________
-
金属在生活生产中有着非常广泛的应用。请回答下列问题:
(1)常用铜做导线,是因为铜的__________性好。
(2)路边的太阳能路灯灯柱为铝合金材质。铝合金灯柱硬度比纯铝__________ (填“大” 或“小”)。
(3)金属的回收不仅节约资源和能源,还能减少对环境的污染。某化学实验室从含少量硝酸锌的硝酸银废液中提取贵金属Ag,其主要操作流程如图:

①固体A的成分有_______________。
②步骤I中发生的化学反应方程式____________________。
③步骤Ⅰ、Ⅱ共同的实验操作名称是_____________,若往溶液D中加入适量某物质后,可得到只含一种溶质的溶液。则该反应的化学方程式为_________________。
(4)目前世界上60%的镁单质是从海水中提取的,已知海水提镁的主要步骤如下:

①操作2中玻璃棒的作用是_______________。
②下列说法正确的是____________________。
A加入的试剂a为石灰乳,试剂b为稀盐酸
B向溶液X中加入硝酸银溶液,若产生白色沉淀,则海水中的氯化镁没有完全转化为沉淀
C上述过程中一共涉及了三种基本反应类型
③海水中本来已有氯化镁,为什么人们还要通过上述过程获得氯化镁?请简述原因_________________。
-
金属材料在生产、生活中应用广泛.
(1)黄铜是铜、锌合金,下列说法中不正确的是 ______ .
A 黄铜属于纯净物  黄铜属于金属材料
黄铜属于金属材料
C 黄铜的硬度比铜大  黄铜的抗腐蚀性能更好
黄铜的抗腐蚀性能更好
(2)铜可以拉成铜丝,这是利用金属的 ______ .
(3)黄铜是铜锌合金,将纯铜片和黄铜片互相刻画(如图所示),纯铜片上留下明显的划痕,该实验说明了 ______ .
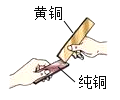
(4)铜器在潮湿的空气中也容易生锈,铜锈(俗称铜绿)的主要成分是 ,结合其组成分析,铜生锈是铜与氧气、 ______ 和 ______ 共同作用的结果;铜生成铜锈的化学方程式为 ______ .
,结合其组成分析,铜生锈是铜与氧气、 ______ 和 ______ 共同作用的结果;铜生成铜锈的化学方程式为 ______ .
(5)常温下一些金属的物理性质数据如下:
| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 
|
| 密度 | 
| 
| 
| 
| 
|
| 熔点 | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 
| 
| 
| 
| 
|
分析上述数据,碎石用的大锤常用铁制而不用铝制,原因是 ______ .
-
金属材料在生产、生活中有广泛的应用,人类的生产和生活都离不开金属。
(一)铁的应用和防护
(1)常州地铁的轨道主要材料是铁合金制作的,其硬度比纯铁________。
(2)钢铁的锈蚀主要是铁与空气中的_________等物质发生化学反应的结果。
(3)为防止铁生锈,通常会对铁制品进行“烤蓝”处理,烤蓝是用化学方法在铁表面生成层致密的四氧化三铁(Fe3O4)保护膜。烤蓝的原理是:在高温下,铁与水发生反应,生成四氧化三铁和一种单质气体,写出该反应的化学反应方程式:_______。
(二)铁的冶炼
我国劳动人民在春秋战国时期就会治铁炼钢,实验室模拟炼铁实验装置如下图所示。
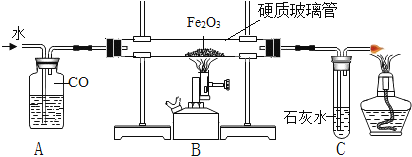
(1)实验时,应先注水片刻后再加热的目的是___________。
(2)实验过程中,硬质玻璃管中发生的化学方程式为___________。
(3)有同学提出黑色粉末中还可能含有Fe3O4。已知:Fe3O4能溶于稀H2SO4,且有Fe3+生成;Fe3+遇到硫氰化钾溶液显血红色。为证明黑色粉末成份,该同学取少量样品于烧杯中,加过量稀H2SO4,充分反应后,滴加少量硫氰化钾,证明黑色粉末中含有Fe和Fe3O4的现象是_________。
(4)若取16g氧化铁粉末进行实验,反应一段时间后,经检测剩余黑色固体成份是Fe和Fe3O4,称量固体的质量为X,则X的范围为_____。
-
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
(1)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 (填“大”或“小”)。
(2)用下列试剂验证这三种金属的活动性顺序,能达到目的是 (填序号)。
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
(3)铁生锈是铁与 发生的复杂的化学反应,硫酸和盐酸都能除铁锈,写出硫酸与铁锈的主要成分发生反应的化学方程式 。
-
金属材料在生产、生活中有广泛的应用。
⑴生铁是常用的铁合金,其硬度比纯铁____(填“大”或“小”)。
⑵空气中,铝比铁具有更好的抗腐蚀性。原因是__________。
⑶铁制品容易锈蚀,可用稀硫酸除去其表面的铁锈,反应的化学方程式为_______________。如果把100g溶质质量分数为98%的浓硫酸配制成除铁锈所需要的溶质质量分数为20%稀硫酸,需要水的质量是____g。
⑷小强用实验研究金属的化学性质时产生的废液中含有少量的硫酸铜。他取一定量的废液,加入一定质量的铁粉,充分反应后过滤,得到滤渣和滤液。然后向滤渣中加入稀盐酸,发现有气泡产生。则滤渣中一定含有的金属是____,向废液中加入铁粉发生的反应化学方程式是____________。
-
金属在当前科技、生产中应用广泛。
(1)我国自行研发的大型客机选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金硬度和强度__________(“大于“或小于”) 纯铝。
(2)开采海域“可燃冰”的钻井平台“蓝鲸一号”使用了大量的金属材料。下列措施中哪一项不能有效防止金属锈蚀?__________(填字母序号)
A.在金属表面涂油或剧漆 B.制成耐腐蚀的合金 C.打磨掉铝制品表面的氧化膜
(3)某化工厂的废液中主要含有硝酸银、硝酸铜。取一定量的该废液样品,加入铁粉,充分反应后过滤,得到滤液和滤渣。写出铁与硝酸银溶液反应的化学方程式__________。反应后得到滤液的质量__________(填“小于”、“大于”或“等于”)反应前所取废液样品的质量。
(4)某钢铁厂每天需消耗4900t 含Fe2O3 76%的赤铁矿石,该厂理论上每天生产含Fe98%的生铁的质量是_____________t。
(5)为比较铝和铁的金属活动性,某同学设计实验方案:将铝和铁分别放入盐酸中,比较反应的剧烈程度。你认为该方案__________(填“合理”或“不合理”),理由是__________。
-
下列失金属材料的说法正确的是
A. 为防止铁制品生锈,可在其表面涂油 B. 钢的性能优良,钢是纯铁
C. 沙漠地区的铁制品锈蚀较快 D. 硬铝片比纯铝片硬度小









