得到如下数据:
| 装置 | B | C |
| 反应前质量 | 86.3g | 284.2g |
| 反应后质量 | 83.9g | 286.9g |
(2)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为______(不用化简);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会______(选填“偏大”、“偏小”或“不变”).
九年级化学解答题中等难度题
| 装置 | B | C |
| 反应前质量 | 86.3g | 284.2g |
| 反应后质量 | 83.9g | 286.9g |

九年级化学解答题中等难度题
| 装置 | B | C |
| 反应前质量 | 86.3g | 284.2g |
| 反应后质量 | 83.9g | 286.9g |

九年级化学解答题中等难度题查看答案及解析
| 装置 | B | C |
| 反应前质量 | 86.3g | 284.2g |
| 反应后质量 | 83.9g | 286.9g |
九年级化学解答题中等难度题查看答案及解析
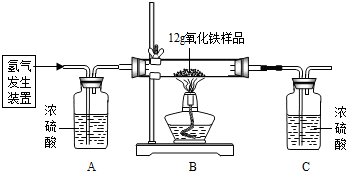
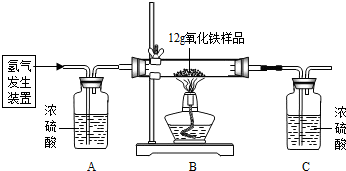
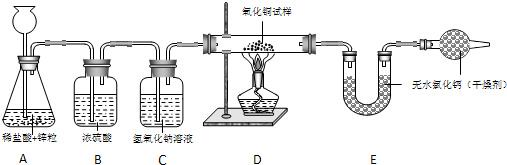
某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O32Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:
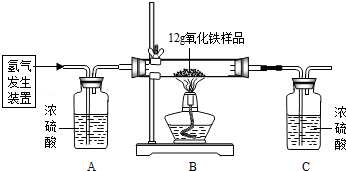
得到如下数据:
| 装置 | B | C |
| 反应前质量 | 86.3g | 284.2g |
| 反应后质量 | 83.9g | 286.9g |
(1)请计算样品中氧化铁的质量分数.(写出计算步骤,计算结果精确到0.l%)
(2)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为 ________ (不用化简);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会________ (选填“偏大”、“偏小”或“不变”).
九年级化学探究题困难题查看答案及解析
某同学为测定10g某赤铁矿石中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O32Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
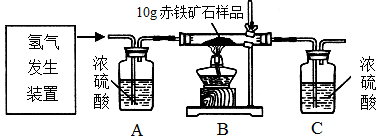
得到如下数据:
| 装置 | B | C |
| 反应前质量 | 84.3g | 294.1g |
| 反应后质量 | 81.9g | 296.8g |
(1)请计算该赤铁矿石样品中氧化铁的质量分数。(写出计算过程)
(2)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为_______________________________________________(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会__________(选填“偏大”、“偏小” 或“不变”)。
九年级化学计算题困难题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
| 装置丙 | 装置丁 | |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 46.5克 | 163.9克 |
九年级化学解答题中等难度题查看答案及解析
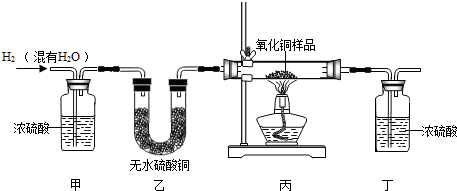
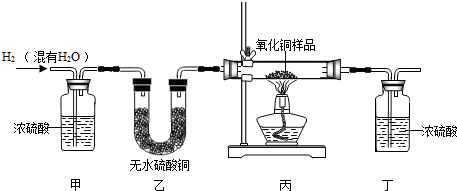
用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取15克干燥样品进行实验.
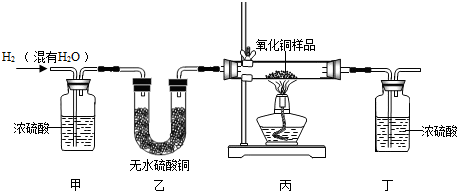
【查阅资料】①无水硫酸铜为白色固体,遇水变成蓝色。
②浓硫酸具有吸水性,可做干燥剂。
请根据资料回答:
(1)在实验中,乙装置的作用是 ________ .
(2)准确称取完全反应前后装置丙和丁的质量如表:
| 装置丙 | 装置丁 | |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 46.5克 | 163.9克 |
小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度(写出计算过程).
(3)小明根据装置丙的质量变化计算,发现小丽结果偏大。请分析导致这一结果的原因可能是 ________ .
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.氧化铜没有完全被还原
九年级化学计算题中等难度题查看答案及解析
| 装置丙 | 装置丁 | |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 46.5克 | 163.9克 |
九年级化学解答题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析