-
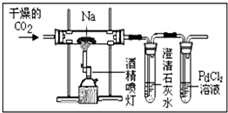
已知,钠在较高温度下能与二氧化碳反应.该反应后含碳产物是什么?不同的同学提出如下四种猜想:甲认为是CO,乙认为是Na2CO3,丙认为是CO和Na2CO3,丁认为是NaHCO3.为确定该反应的含碳产物,四位同学用如图装置进行实验探究.
[查阅资料]:
①CO通入PdCl2溶液能生成黑色物质,可利用该反应检测CO是否存在.
②Na2CO3 和NaHCO3都是白色易溶于水的固体,与Ca(OH)2溶液反应均能生
成CaCO3白色沉淀.
回答下列问题:
(1)不用实验就可知道丁的猜想是错误的,因为该猜想违背了______.
(2)实验时应先往装钠的玻璃直管通CO2一段时间,装澄清石灰水的试管中的现象是______.
(3)实验开始后,观察到PdCl2溶液的试管中有黑色物质产生,且充分反应后玻璃直 管中的固体能全部溶解于水.取所得溶液并加入澄清石灰水,观察到浑浊现象.据此可知:
①猜想正确的同学的是______.
②钠与二氧化碳反应的化学方程式为______ Na2CO3+CO
-
已知,钠在较高温度下能与二氧化碳反应.该反应后含碳产物是什么?不同的同学提出如下四种猜想:甲认为是CO,乙认为是Na2CO3,丙认为是CO和Na2CO3,丁认为是NaHCO3.为确定该反应的含碳产物,四位同学用如图装置进行实验探究.
[查阅资料]:
①CO通入PdCl2溶液能生成黑色物质,可利用该反应检测CO是否存在.
②Na2CO3 和NaHCO3都是白色易溶于水的固体,与Ca(OH)2溶液反应均能生
成CaCO3白色沉淀.
回答下列问题:
(1)不用实验就可知道丁的猜想是错误的,因为该猜想违背了______.
(2)实验时应先往装钠的玻璃直管通CO2一段时间,装澄清石灰水的试管中的现象是______.
(3)实验开始后,观察到PdCl2溶液的试管中有黑色物质产生,且充分反应后玻璃直 管中的固体能全部溶解于水.取所得溶液并加入澄清石灰水,观察到浑浊现象.据此可知:
①猜想正确的同学的是______.
②钠与二氧化碳反应的化学方程式为______ Na2CO3+CO

-
已知,钠在较高温度下能与二氧化碳反应.该反应后含碳产物是什么?不同的同学提出如下四种猜想:甲认为是CO,乙认为是Na2CO3,丙认为是CO和Na2CO3,丁认为是NaHCO3.为确定该反应的含碳产物,四位同学用如图装置进行实验探究.
[查阅资料]:
①CO通入PdCl2溶液能生成黑色物质,可利用该反应检测CO是否存在.
②Na2CO3 和NaHCO3都是白色易溶于水的固体,与Ca(OH)2溶液反应均能生
成CaCO3白色沉淀.
回答下列问题:
(1)不用实验就可知道丁的猜想是错误的,因为该猜想违背了______.
(2)实验时应先往装钠的玻璃直管通CO2一段时间,装澄清石灰水的试管中的现象是______.
(3)实验开始后,观察到PdCl2溶液的试管中有黑色物质产生,且充分反应后玻璃直 管中的固体能全部溶解于水.取所得溶液并加入澄清石灰水,观察到浑浊现象.据此可知:
①猜想正确的同学的是______.
②钠与二氧化碳反应的化学方程式为______ Na2CO3+CO

-
已知,钠在较高温度下能与二氧化碳反应.该反应后含碳产物是什么?不同的同学提出如下五种猜想:甲认为是C,乙认为是CO,丙认为是Na2CO3,丁认为是CO和Na2CO3,戊认为是NaHCO3.为确定该反应的含碳产物,五位同学用右图装置进行实验探究.

已知:CO能与PdCl2生产黑色的Pd,可利用该反应检测CO是否存在.回答下列问题:
(1)不用实验就可知道戊的猜想是错误的,因为该猜想违背了______.
(2)实验室制取二氧化碳的化学方程式为______.
(3)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应选用的装置是______(选填右图中的I”、“II”或“III”).

(4)实验时应先往装钠的玻璃直管通CO2一段时间,装澄清石灰水的试管中的现象是______.
(5)实验开始后,观察到PdCl2溶液的试管中有黑色物质产生,且充分反应后玻璃直管中的固体全部溶解于水.取所得溶液并加入澄清石灰水,观察到浑浊现象.据此可知:
①哪位同学的猜想是正确的?答:______.
②钠与二氧化碳反应的化学方程式为______ Na2CO3+CO
-
已知,钠在较高温度下能与二氧化碳反应.该反应后含碳产物是什么?不同的同学提出如下五种猜想:甲认为是C,乙认为是CO,丙认为是Na2CO3,丁认为是CO和Na2CO3,戊认为是NaHCO3.为确定该反应的含碳产物,五位同学用右图装置进行实验探究.

已知:CO能与PdCl2生产黑色的Pd,可利用该反应检测CO是否存在.回答下列问题:
(1)不用实验就可知道戊的猜想是错误的,因为该猜想违背了______.
(2)实验室制取二氧化碳的化学方程式为______.
(3)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应选用的装置是______(选填右图中的I”、“II”或“III”).

(4)实验时应先往装钠的玻璃直管通CO2一段时间,装澄清石灰水的试管中的现象是______.
(5)实验开始后,观察到PdCl2溶液的试管中有黑色物质产生,且充分反应后玻璃直管中的固体全部溶解于水.取所得溶液并加入澄清石灰水,观察到浑浊现象.据此可知:
①哪位同学的猜想是正确的?答:______.
②钠与二氧化碳反应的化学方程式为______ Na2CO3+CO
-
(10龙岩市17).已知,钠在较高温度下能与二氧化碳反应。该反应后含碳产物是什么?不同的同学提出如下五种猜想:甲认为是C,乙 认为是CO,丙认为是Na2CO3,丁认为是CO和Na2CO3,戊认为是NaHCO3。为确定该反应的含碳产物,五位同学用右图装置进行实验探究。
认为是CO,丙认为是Na2CO3,丁认为是CO和Na2CO3,戊认为是NaHCO3。为确定该反应的含碳产物,五位同学用右图装置进行实验探究。

已知:CO能与PdCl2生产黑色的Pd,可利用该反应检测CO是否存在。回答下列问题:
(1)不用实验就可知道戊的猜想是错误的,因为该猜想违背了___________________。
(2)实验室制取二氧化碳的化学方程式为_____________________________。
(3)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应选用的装置是__________(选填右图中的“I”、“II”或“III”)。

(4)实验时应先往装钠的玻璃直管通CO2一段时间,装澄清石灰水的试管中的现象是
______________________________。
(5)实验开始后,观察到PdCl2溶液的试管中有黑色物质产生,且充分反应后玻璃直管中的固体全部溶解于水。取所得溶液并加入澄清石灰水,观察到浑浊现象。据此可知:
①哪位同学的猜想是正确的?答:___________。
②钠与二氧化碳反应的化学方程式为_____________________。
-
学了课本中C和CuO的反应后,小明同学为了探究木炭还原氧化铜所生成的气体产物是什么,提出了猜想:a.可能是二氧化碳;b.可能是一氧化碳.并设计如如图所示装置进行实验,预期的实验现象及结论如下:
①若澄清的石灰水变浑浊,则气体为二氧化碳;
②若澄清的石灰水不变浑浊,则气体为一氧化碳.
请你回答:
(1)该同学的猜想是否严谨?若不严谨,请作补充.______
(2)请你对该实验装置予以评价.______
小亮同学对反应后产生的红色固体的成分提出了疑问,并进一步进行探究.
【查阅资料】①C也能将CuO还原为红色固体Cu2O(氧化亚铜) ②Cu2O+H2SO4(稀)=Cu+CuSO4+H2O ③+2价铜盐的水溶液呈蓝色.
【猜 想】(a)红色固体只是Cu (b)______ (c)红色固体是Cu和Cu2O的混合物
【实验探究】 | 实验操作 | 实验现象 | 实验结论 |
| 取7.2g红色固体于烧杯中加入足量稀硫酸,充分搅拌,静置. | 若无现象 | 证明红色故题为:______ |
| 若:___________________ | 证明红色固体肯定含_____ 可能含有___________ |
| 取上述反应液过滤、洗涤、干燥、和称重,得固体6.8g | | 确认红色固体是_________ |

-
已知草酸(H2C2O4)加热时在浓硫酸的作用下会发生分解反应,某化学兴趣小组对其分解产物进行了如下探究.
【提出猜想】
(1)分解产物是一氧化碳和水蒸气的混合物.
(2)分解产物是二氧化碳和水蒸气的混合物.
(3)分解产物是一氧化碳、二氧化碳和水蒸气的混合物.
你认为合理的猜想是______(选填序号),依据是______.
【查阅资料】
(1)浓硫酸具有脱水性,可以将有机物中的氢、氧元素按水的组成脱去.
(2)白色的无水硫酸铜遇水会变为蓝色.
(3)碱石灰是固体氢氧化钠和氧化钙的混合物.
【进行实验】为了检验草酸的分解产物的成份,该小组同学将草酸的分解产物通过下图所示的装置(部分夹持仪器已略去).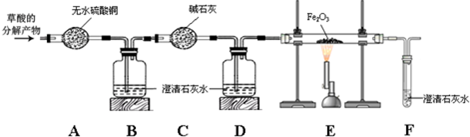
(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊,证明草酸分解产生了______.
(2)装置D的作用是______.
(3)证明草酸分解产生了一氧化碳的现象应包括______.
(4)装置B中发生反应的化学方程式为______;装置E中发生反应的化学方程式为______ 2Fe+3CO2
-
已知草酸(H2C2O4)加热时在浓硫酸的作用下会发生分解反应,某化学兴趣小组对其分解产物进行了如下探究.
(提出猜想)
(1)分解产物是一氧化碳和水蒸气的混合物.
(2)分解产物是二氧化碳和水蒸气的混合物.
(3)分解产物是一氧化碳、二氧化碳和水蒸气的混合物.
你认为合理的猜想是 _________(选填序号),依据是_________。
(查阅资料)
(1)浓硫酸具有脱水性,可以将有机物中的氢、氧元素按水的组成脱去.
(2)白色的无水硫酸铜遇水会变为蓝色.
(3)碱石灰是固体氢氧化钠和氧化钙的混合物.
(进行实验)为了检验草酸的分解产物的成份,小组同学将草酸的分解产物通过下图所示的装置(部分夹持仪器已略去).
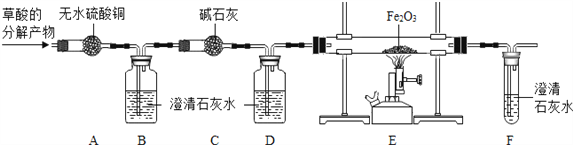
(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊,证明草酸分解产生了________________ 。
(2)装置D的作用是________________ 。
(3)证明草酸分解产生了一氧化碳的现象应包括_________________.
(4)装置B中发生反应的化学方程式为___________,装置E中发生反应的化学方程式为________.
(得出结论)草酸分解的化学方程式为_________________.
(反思与评价)从环保角度考虑,上述实验的不足之处是____________ .
-
化学小组同学在课外读物中看到:“通常CO2可作灭火剂,但有些物质(如Na)着火,不能用CO2熄灭。”他们决定探究CO2与Na反应的产物。
(提出猜想)小明认为CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3。
小红认为CO2与Na反应还可能生成NaOH。
经过小组讨论,同学们一致认为不可能生成NaOH,理由是________。
(查阅资料) ①Na是非常活泼的金属,常温下与O2、H2O等物质反应。
②Na2CO3溶液与石灰水反应生成白色沉淀。
③Na2O是白色固体,与H2O反应生成NaOH。
④向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀。
⑤浓硫酸能吸收气体中的水分,干燥气体。
⑥NaHCO3溶液能与HCl气体反应生成二氧化碳,故可用于除去HCl气体。
(实验过程)同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)

(1)实验记录:________________________、________

(2)实验反思:
①组装好装置后应该进行的操作是____________。
②实验记录②中,E中出现浑浊,再点燃酒精灯的目的是_____________。
③若无装置C,对实验有影响的物质是__________。
④该装置存在明显的缺陷:__________。
⑤数据若在实验过程中至少需要8.8g二氧化碳参加反应,则最少需要含杂质20%的石灰石的质量是多少_______?(写出计算过程)













