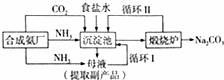
侯德榜创造了一种著名的纯碱生产方法--“联合制碱法”.
“联合制碱法”生产过程:
(1)第一步主要反应为NH3+CO2+H2O=NH4HCO3该反应属于基本反应类型中的______反应.
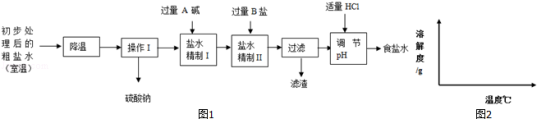
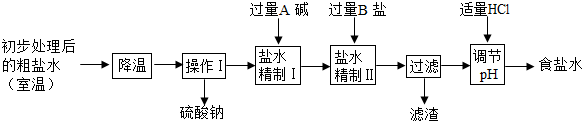
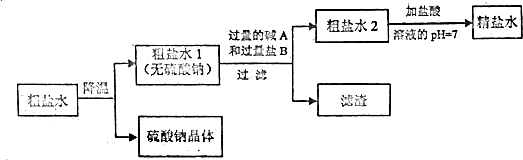
(2)第二步用食盐与NH4HCO3反应.食盐来源于某盐田,该粗盐主要含有氯化钠,此外还含有少量硫酸钠,氯化钙和氯化镁.经净化、精制得到生产碳酸钠所需要的食盐水.
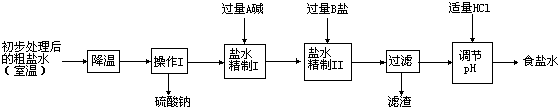
其主要流程如下:
①通过降温使硫酸钠从粗盐水中析出,说明硫酸钠的溶解度随温度的变化较______(填“大”或“小”).
②“精制I”操作中,加入过量含钙元素的碱的化学式是______,其反应化学方程式为______.
③“精制II”操作中,加入B盐的有关反应方程式为______,______.
④为保证“精制II”操作中过量B盐把杂质全部除去,写出检验溶液中B盐是否过量的实验方案:______
______.
⑤查阅资料得知NaCl、NH4HCO3、NaHCO3、NH4Cl在30℃时的溶解度如下表所示:
| 温度 | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30℃ | 41.1g | 27.0g | 11.1g | 36.3g |
(3)第三步处理制得碳酸钠,反应原理为2NaHCO
(4)用“联合制碱法”制得的纯碱中常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的质量分数,小雯同学称取该样品5.6g加入到盛有100g足量稀盐酸的烧杯中,完全反应后称得烧杯中的溶液质量为103.4g.求该纯碱样品中碳酸钠的质量分数.
九年级化学解答题中等难度题