-
硫酸亚铁可用于制颜料、净水剂、防腐剂等。
(1)写出下列反应的化学方程式:
①实验室可制得FeSO4的反应_____。
②FeSO4溶液与NaOH溶液反应_____。
(2)FeSO4溶液能与O2反应,溶液颜色由绿色变为黄色。为研究影响FeSO4溶液与O2反应速率的因素,小明同学进行了以下实验:
实验编号
FeSO4溶液
温度
/℃
溶液
酸碱性
实验现象
体积
/mL
溶质质量分数/%
实验前
30分钟
120分钟
1
30
20
20
溶液为浅绿色
溶液略显黄色
溶液黄色略有加深
2
30
10
20
溶液为浅绿色
溶液明显变黄
溶液黄色明显加深
3
30
10
40
溶液立即变黄
4
30
10
20
5滴稀H2SO4
溶液为浅绿色
溶液为浅绿色
溶液为浅绿色
请回答:
①小明的实验中,研究影响上述反应速率的因素是_____。
②若要研究溶液酸碱性对反应速率的影响,需要对比_____(填实验编号)。
③对比实验2和3,得出的结论是_____。
九年级化学科学探究题简单题查看答案及解析
-
绿矾又名七水硫酸亚铁(FeSO4•7H2O),其用途广泛,可用于制铁盐、氧化铁颜料、净水剂、防腐剂、消毒剂等.绿矾(FeSO4•7H2O)的一种综合利用工艺如下:
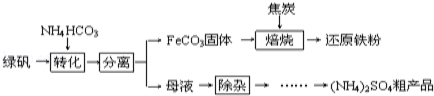
(1)隔绝空气进行“焙烧”,铁元素的转化途径是:(提示:该过程中所用的还原剂的是CO )
FeCO3
FeO
Fe
资料:【难溶性碳酸盐受热分解成金属氧化物、二氧化碳气体】
写出高温条件下进行“焙烧”过程中①②反应的化学方程式:
① ②
(2)粗产品(NH4)2SO4还可以作 肥.
九年级化学填空题简单题查看答案及解析
-
(10分)绿矾又名七水硫酸亚铁(FeSO4·7H2O),其用途广泛,可用于制铁盐、氧化铁颜料、净水剂、防腐剂、消毒剂等。绿矾(FeSO4·7H2O)的一种综合利用工艺如下:
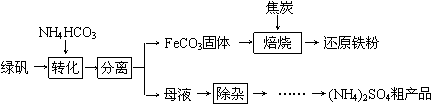
(1)细铁丝在氧气中可以燃烧,请写出铁在氧气中燃烧的化学方程式 。
(2)绿矾与NH4HCO3在溶液中反应,有CO2生成,反应的化学方程式为 。
(3)隔绝空气进行“焙烧”,铁元素的转化途径是
,实际作还原剂的是CO。写出“焙烧”过程中各步反应的化学方程式:
A.
;
B.____________________________________________;
C.____________________________________________。
(4)母液“除杂”后,欲得到(NH4)2SO4粗产品,操作步骤依次为蒸发浓缩、______、过滤、洗涤、干燥。
九年级化学填空题简单题查看答案及解析
-
硫酸亚铁可用于制颜料、净水剂和防腐剂等。课外活动小组探究利用硫酸厂排出的炉渣(含Fe2O3、CuO、CuSO4,杂质不溶于水也不溶于酸)制取硫酸亚铁,主要步骤如下:
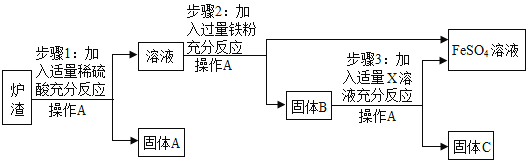
(1)操作A是_____。
(2)步骤2中主要发生两个化学反应,一个是
,另一个反应的化学方程式为:_____。
(3)步骤3中X溶液中溶质的化学式为:_____。
九年级化学流程题中等难度题查看答案及解析
-
绿矾(FeSO4•7H2O)用途广泛,可用作净水剂,医学上可用作补血剂,还可用于制颜料。
(1)绿矾是一种絮凝剂,利用其溶于水后生成的胶状物对杂质的____________,使杂质沉降来达到净水的目的。
(2)缺铁会引起贫血,铁是一种人体必需的__________(填“常量元素”或“微量元素”)。
(3)《本草纲目》中记载,绿矾“煅过变赤,则为绛矾”。绛矾是古代壁画、彩塑中使用的一种红色颜料。
某化学兴趣小组同学对绿矾高温分解的产物很感兴趣,进行了如下探究。
(查阅资料)
①绿矾高温分解的产物是一种固态金属氧化物和几种气态非金属氧化物。
②在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低。
③无水硫酸铜遇水变蓝。
④硫有两种常见的氧化物,部分性质如下表:
硫的氧化物
熔点
沸点
水溶性
能否使高锰酸钾溶液褪色
SO2
-75.5℃
-10℃
易溶于水
能
SO3
16.8℃
44.8℃
易溶于水
不能
(提出问题)
《本草纲目》中记载绿矾“煅过变赤”,经实验验证绿矾高温分解确实产生红色固体,说明绿矾高温分解产生的一种固态金属氧化物是____________,那么产生的几种气态非金属氧化物是什么呢?
(进行猜想)猜想1:H2O 和____________;
猜想2:H2O 和SO3 ;
猜想3:H2O、SO2和SO3 。
甲同学认为无需通过进一步实验即可判定猜想2错误,理由是_______________________。
(设计实验)
乙同学用以下装置检验绿矾高温分解产生的气态非金属氧化物:
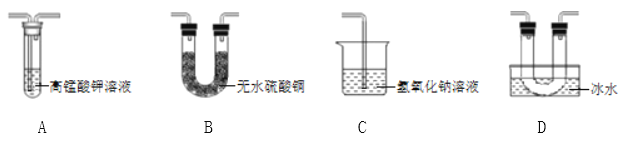
需将绿矾高温分解产生的气体依次通过______________(填字母,且每套装置限用一次)。
(分析现象)进行上述实验,观察到A中试管内溶液________,B中U形管内固体________,D中U形管内出现无色晶体,说明猜想3正确。
(得出结论)绿矾高温分解的化学方程式为_______________________________________。
(拓展延伸)生产硫酸最古老的方法是使绿矾高温分解,将生成的SO3和H2O同时冷凝并发生反应SO3+H2O=H2SO4 ,所以古代称硫酸为“绿矾油”。假定SO3和H2O全部冷凝并充分反应,SO2全部逸出,则通过这个方法得到的硫酸的质量分数为____________(计算结果保留一位小数)。
九年级化学科学探究题中等难度题查看答案及解析
-
无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂、工业上作防腐剂、制造白色颜料(锌钡白)等。实验室通常用粗锌(含有铁等杂质)和稀硫酸反应制取氢气。为了充分利用制氢废液,某实验小组用制氢废液为原料制备硫酸锌晶体并探究其性质。
(制备硫酸锌晶体)
已知:①开始生成氢氧化物沉淀到沉淀完全的pH值的范围分别为:Fe(OH)3:2.7—3.7 Fe(OH)2:7.6—9.6 Zn(OH)2:5.7—8
②硫酸锌微溶于酒精
实验流程如图所示:
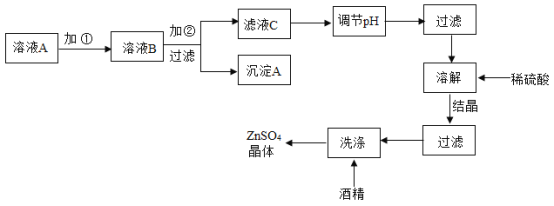
试回答下列问题:
(1)实验室制取氢气的原理_______ (用化学方程式表示)。
(2)溶液A中加入试剂①的目的是使FeSO4转化为Fe2(SO4)3,通常用过氧化氢溶液,该反应的化学方程式为
,X的化学式为____________。
(3)加试剂②的目的是使铁元素完全沉淀,加入试剂②最好选用_________。
A ZnO
B Zn(OH)2
C NaOH
D ZnSO4
(4)结晶操作的过程包括:蒸发浓缩、_________。
(5)最后一次过滤得到的晶体用酒精洗涤晶体而不用水洗的目的是_____。
(测定硫酸锌晶体ZnSO4·xH2O中结晶水的含量)
实验小组同学将回收到的皓矾晶体(ZnSO4·xH2O)用下面的装置测定晶体中结晶水的含量(图中半透膜可让气体通过又可防止固体粉末进入导管)。测定方法:称取28.7g晶体置于C装置的硬质玻璃管中,加热至完全失去结晶水:(
),冷却至常温后,称量玻璃管中固体,其质量为16.1g。
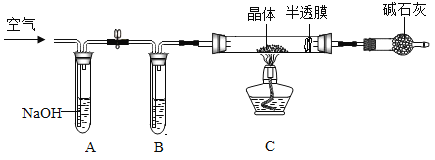
(1)A中的化学方程式是_____,B中的试剂可从下列物质中选取,你的选择是_____。
A 浓硫酸
B 硝酸银溶液
C 饱和碳酸钠溶液
D 澄清石灰水
(2)实验过程中若不通入空气测得的结果将_______(填“偏大”或“偏小”或“无影响”)。根据实验结果,计算皓矾晶体中结晶水的x值为____________。(写出计算过程)
九年级化学流程题困难题查看答案及解析
-
(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为________.
废铁屑与硫酸反应产生的气体中含有有毒气体H2S,用CuSO4溶液可以吸收这种气体并产生黑色沉淀,该反应的化学方程式为________.
(2)为了探究CO的还原性,某同学将绕成螺旋状的铜丝放在酒精灯上加热至铜丝变黑后,立即将铜丝伸入盛满CO的集气瓶中(内装适量澄清石灰水),铜丝又恢复光亮的红色,振荡集气瓶,还可以看到集气瓶中________.
上述实验过程中,能表明CO具有还原性的反应的化学方程式是________.将上述表面变黑的铜丝冷却后放入稀硫酸中,可以看到的现象是________________,________.
(3)一包白色固体可能含有NaCl、CuSO4、NH4NO3、BaC12、K2 C O3中的一种或几种.有同学进行下列实验来确定该固体的成分:
(a)取少许固体放入试管,加入NaOH浓溶液并微热,把湿润的红色石蕊试纸放在试管口,试纸变为蓝色.
(b)取一些白色固体放入试管加水溶解,得无色透明溶液.
(c)向实验b所得溶液中滴2滴酚酞试液,溶液变为红色,再向其中加入过量CaC12溶液,红色褪去,产生白色沉淀.
(d)将实验c所得溶液中的沉淀滤去,向滤液中加入AgNO3溶液,又产生白色沉淀.
①根据以上实验现象判断:这包白色固体中一定有________,肯定没有________.
②若用这包白色固体配成稀溶液来浇花,可产生的作用是________(填下列选项的字母序号).
A.促进花草的茎、叶生长茂盛,叶色浓绿
B.促进花草的根系发达,增强抗寒抗旱能力
C.促进花草生长健壮,茎杆粗硬,增强对病虫害和倒伏的抵抗能力
(4)实验室需用20%的稀硫酸460mL,若用如图标签所示的硫酸来配制,则至少需用这种硫酸________
mL.
九年级化学填空题中等难度题查看答案及解析
-
(5分)硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:Fe+H2SO4=FeSO4+H2↑
②与碳酸钠溶液反应:
③与氯化钡溶液反应:
上述反应中,属于酸的共同性质的是 (填编号)。
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
九年级化学填空题中等难度题查看答案及解析
-
分类是学习化学的重要方法。请依据所学知识,从利用物质性质的角度将下列应用分类。
①用活性炭净水 ②用水洗涤试管壁上的硫酸铜 ③用食醋除热水壶中的水垢
④食品充氮气防腐 ⑤干冰用于人工降雨 ⑥用炉具清洁剂去除油垢
(1)选出的一组是___________(填序号);(2)分类依据是_________________。
(3)在考虑物质的用途时,除了考虑物质的性质外。还需要考虑价格、资源、是否美观、使用是否便利,以及废料是否易于回收和对环境的影响等多种因素。用铜做导线而不用银,主要是考虑了①_________;用可降解塑料袋代替聚乙烯塑料袋,主要考虑了②___________。
九年级化学选择填充题中等难度题查看答案及解析
-
实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:

(1)步骤①中,金属X是_____。
(2)写出步骤①中反应的化学方程式_____。
(3)步骤①和②中涉及到的化学反应的基本反应类型为_____。
(4)在步骤②中,还能将金属混合物分离开的物理方法是_____。
九年级化学流程题中等难度题查看答案及解析