-
(7分)氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
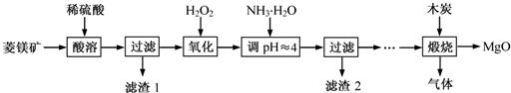
(1)MgCO3与稀硫酸反应的化学方程式为 ;
(2)加入H2O2 氧化时,发生反应的化学方程式为(已经配平,X属于常见的化合物):
 ,则X的化学式为 ;
,则X的化学式为 ;
(3)NH3·H2O是氨水的主要成分,溶液显 性,加入氨水时,溶液的PH值 (填“增大”、“减少”或“不变”),当PH≈4时,会产生红褐色沉淀,则滤渣2 的成分是 (填化学式)。
(4)通常用PH试纸测定溶液的PH值,其操作方法是 。
(5)煅烧过程存在以下反应:木炭和硫酸镁在高温下除得到氧化镁外,还得两种气体,一种会造成酸雨,另一种大量排放则会引起温室效应。请写出该反应的化学方程式: 。
-
氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:
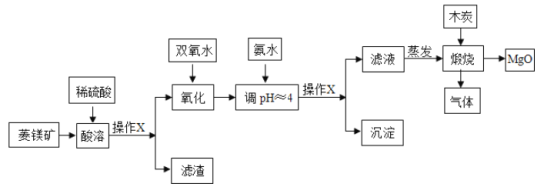
(1)操作X的名称是_____,该操作需要用到的玻璃仪器主要有:烧杯、_____、玻璃棒.
(2)蒸发过程中,要用玻璃棒不断地搅拌,其目的是_____.
(3)碳酸镁与稀硫酸反应的化学方程式为_____;该反应属于_____反应.
(4)加入双氧水氧化时,发生反应的化学方程式为:2FeSO4+H2O2+H2SO4═Fe2(SO4)3+2X.则X的化学式为_____.
(5)煅烧过程存在以下反应:2MgSO4+C 2MgO+2SO2↑+CO2↑;MgSO4+C
2MgO+2SO2↑+CO2↑;MgSO4+C MgO+SO2↑+CO↑;MgSO4+3C
MgO+SO2↑+CO↑;MgSO4+3C MgO+S↑+3CO↑.利用下图装置对煅烧产生的气体进行分步吸收或收集.
MgO+S↑+3CO↑.利用下图装置对煅烧产生的气体进行分步吸收或收集.
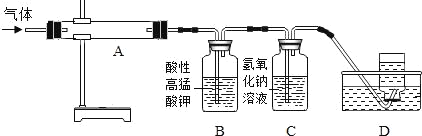
资料:酸性高锰酸钾能吸收二氧化硫;硫蒸气在A装置冷凝成固体.
①上述反应产生的气态氧化物中_____(填化学式)不会对空气造成污染.
②D中收集到的气体具有_____(填一种化学性质).
③C中发生反应的化学方程式为_____.
(6)若直接煅烧100t含碳酸镁84%的菱镁矿,理论上可制得氧化镁多少_____?
-
氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于酸)为原料制备高纯氧化镁的实验流程如下:
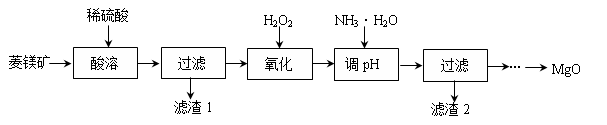
(1)酸溶之前要将矿石粉碎的目的是 。稀硫酸需要过量的目的是 。酸溶步骤中碳酸镁溶解的反应方程式为 。
(2)已知Mg2+、Fe2+和Fe3+在溶液中遇到氨水均可以转化成难溶性碱沉淀,开始沉淀和沉淀完全的pH如下表:
| Mg2+ | Fe2+ | Fe3+ |
| 开始沉淀 | 9.4 | 7.9 | 2.7 |
| 沉淀完全 | 12.4 | 9.6 | 3.7 |
流程“氧化”一步中H2O2的作用是将溶液中的Fe2+转化成Fe3+,不能直接沉淀Fe2+的原因是 。
(3)加氨水调节溶液的PH范围为 。
(4)滤渣2的化学式是 。
-
氧化镁在医药、建筑等行业应用广泛,以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶,也不参加反应)为原料制备高纯氧化镁的实验流程如下:
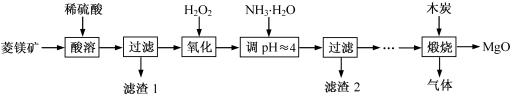
资料:① 不同氢氧化物沉淀的pH范围:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 8.6 |
| 完全沉淀的pH | 3.2 | 11.1 |
② 硫在常温下是一种淡黄色固体,硫的熔点约为115.2℃,沸点约为444.7℃;
③ 高锰酸钾溶液只吸收SO2,不吸收CO2;
④ 碱溶液既吸收SO2,又吸收CO2。
试回答下列问题:
(1)MgCO3与稀硫酸反应的化学方程式为 。
(2)加入H2O2目的是在酸性条件下将FeSO4氧化成Fe2(SO4)3,同时生成水,发生反应的化学方程式为 。
(3)加氨水调节溶液的pH约为4的目的是 ,反应的化学方程式为
。
(4)煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。(假设每步反应都完全进行)
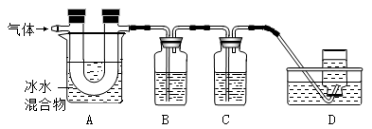
① A中现象是:玻璃管壁出现 色固体;
② B中盛放的溶液可以是 (填字母),实验现象为 ;
a.Ca(OH)2 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③ D中收集的气体是 (填化学式)。
-
氧化镁在医药等行业应用广泛。实验室以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于水和酸)为原料制备高纯氧化镁的实验流程如下:
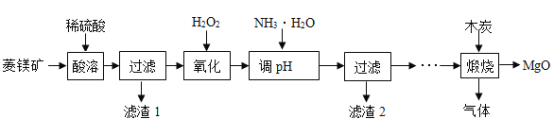
(1)为了提高“酸浸”的效果,可采取的措施有:适当升高温度、____________。MgCO3与稀硫酸反应的化学方程式为_________________。
(2)“氧化”过程中,将FeSO4全部转化为Fe2(SO4) 3,然后加氨水,调节溶液的PH范围为______________。(已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表)
| 对应离子 | Fe3+ | Fe2+ | Mg2+ |
| 开始沉淀时的pH | 2.7 | 7.9 | 9.4 |
| 完全沉淀时的pH | 3.7 | 9.6 | 11.4 |
(3)过滤后得到滤渣2和滤液,滤渣2是______(填化学式),此时滤液中的阳离子一定含有____________(填离子符号)。
(4)煅烧过程存在以下反应: ;
; ;
;
已知:①硫在常温下是一种淡黄色固体,硫的熔点约为115.2°C,沸点约为444.7°C;②高锰酸钾溶液与SO2反应会褪色,且只吸收SO2,不吸收CO2;③碱溶液既吸收SO2,又吸收CO2。利用下图装置对煅烧产生的气体进行检验并收集。
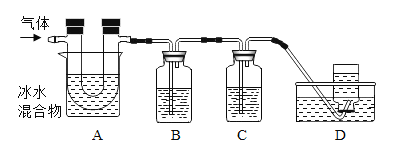
①集气瓶B中盛放的溶液是_______________(填字母),C中盛放的溶液是_____________(填字母)。
a Ca(OH)2溶液
b KMnO4溶液
c NaOH溶液
d BaCl2溶液
②装置D的作用是__________________________。
-
(题文)我国高纯氧化镁产品供不应求,工业上可以用硫酸镁还原热解制备,工业流程如下:
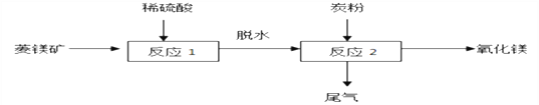
(1)菱镁矿主要成分是碳酸镁,反应前要粉粹,目的是________,反应1化学反应方程式为________。
(2)反应2中的化学方程式为:2MgSO4+C  2MgO+2SO2↑+________。
2MgO+2SO2↑+________。
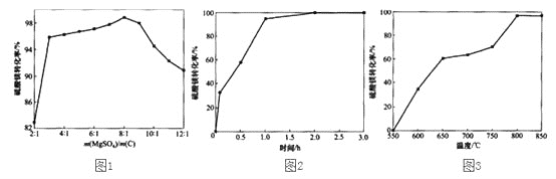
(3)反应2中硫酸镁与炭的配比对硫酸镁转化率的影响如下图1,硫酸镁转化率最高时m(MgSO4):m(C)=________,当配炭比2:1~3:1时硫酸镁转化率低的原因是________。
(4)反应2中时间和温度对硫酸镁转化率的影响分别如下图2、图3,则最佳的时间和温度分别为_____h、____℃。
(5)尾气直接排放到空气中会引起________、________两个当今世界全球性问题,可以用石灰浆吸收其中的有毒气体,化学方程式为:________。
-
我国高纯氧化镁产品供不应求,工业上可以用硫酸镁还原热解制备,工业流程如下:
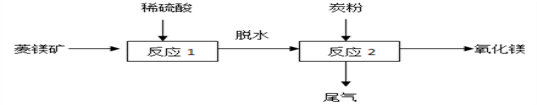
(1)菱镁矿主要成分是碳酸镁,反应前要粉粹,目的是______,反应1化学反应方程式为___________。
(2)反应2中的化学方程式为:2MgSO4+C 2MgO+2SO2↑+______。
2MgO+2SO2↑+______。
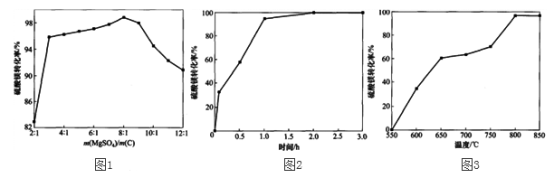
(3)反应2中硫酸镁与炭的配比对硫酸镁转化率的影响如下图1,硫酸镁转化率最高时m(MgSO4):m(C)=______,当配炭比2:1~3:1时硫酸镁转化率低的原因是______。
(4)反应2中时间和温度对硫酸镁转化率的影响分别如下图2、图3,则最佳的时间和温度分别为______h、______℃。
(5)尾气直接排放到空气中会引起______、______两个当今世界全球性问题,可以用石灰浆吸收其中的有毒气体,化学方程式为:______。
-
以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶,也不参加反应)为原料制备硫酸镁的实验流程如下图
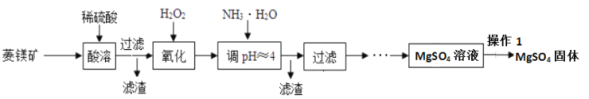
(1)菱镁矿原料属于________________。(“混合物”、“纯净物”)
(2)该过程中加入双氧水的反应为:H2O2 + 2FeSO4 + H2SO4 = Fe2(SO4)3 + 2H2O,反应物H2O2中O元素的化合价为____________,溶液颜色由浅绿色变为_______色。
(3)实验室模拟调节溶液pH≈4的步骤, 用________蘸取待测液点pH试纸的中部,然后迅速与标准比色卡对比读数,且读数为___________(“小数”、“整数”),该过程中若提前润湿pH试纸,则可能导致________(填“升高”、“降低”或“不变”)。
(4)操作1与过滤均要用到一种玻璃仪器,该仪器在操作1中的作用是___________。
-
高纯氧化铁(Fe2O3)又称“引火铁”,可作催化剂,在现代工业上有广泛应用前景。以下是用赤铁矿(含少量 SiO2 等杂质)为原料,制备高纯氧化铁的生产流程示意图。
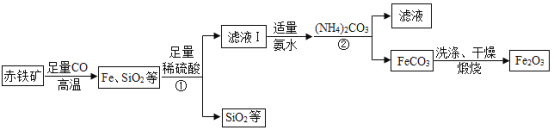
已知:氨水呈碱性(主要成分 NH3·H2O 是一种碱);(NH4)2CO3溶液呈碱性,40℃以上易分解。
(1)写出高温时赤铁矿中的Fe2O3与CO发生反应的化学方程式______________。
(2)①处发生反应的化学方程式为_______________________。
(3)加入(NH4)2CO3后,该反应必须控制的条件是____________;(NH4)2CO3与FeSO4发生复分解反应而生成FeCO3,则②处反应的化学方程式为__________________________。
(4)用蒸馏水洗涤FeCO3的目的是除去表面附着的杂质,洗涤干净的标志是:取最后一次洗涤液,向其中加入适量的BaCl2溶液,无____________(填现象)产生,即为洗涤干净。
-
高纯氧化铁(Fe2O3)又称“引火铁”,可作催化剂,在现代工业上有广泛应用前景。以下是用赤铁矿(含少量 SiO2 等杂质)为原料,制备高纯氧化铁的生产流程示意图。
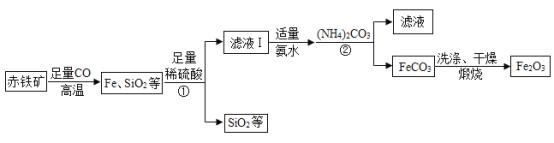
已知:氨水呈碱性(主要成分NH3·H2O是一种碱);(NH4)2CO3溶液呈碱性,40℃以上易分解。
(1)写出高温时赤铁矿中的Fe2O3 与 CO 发生反应的化学方程式_____。
(2)①和②处的操作是_____,这个操作中玻璃棒的作用是_____。
(3)加入(NH4)2CO3 后,该反应必须控制的条件是_____;(NH4)2CO3与FeSO4 发生复分解反应而生成FeCO3,则②处反应的化学方程式为_____。
(4)用蒸馏水洗涤FeCO3 的目的是除去表面附着的杂质,洗涤干净的标志是:取最后一次洗涤液,向其中加入适量的 BaCl2 溶液,无_____(填现象)产生,即为洗涤干净。

2MgO+2SO2↑+CO2↑;MgSO4+C
MgO+SO2↑+CO↑;MgSO4+3C
MgO+S↑+3CO↑.利用下图装置对煅烧产生的气体进行分步吸收或收集.













