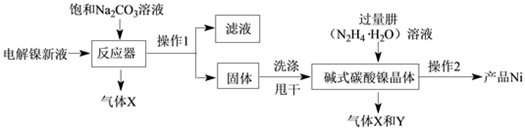-
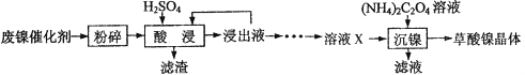
草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如下:
已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Ni2+ | 6.7 | 9.5 |
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为 _______(填字母)。
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min

(3)“酸浸”中发生的复分解反应方程式为________。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是_____(填字母)。
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH_____(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和_________。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、_____ 、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、___________;
③烘干温度不超过110℃的原因是______。
-
草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如下:

已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Ni2+ | 6.7 | 9.5 |
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为 _______(填字母)。
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min

(3)“酸浸”中发生的复分解反应方程式为________。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是_____(填字母)。
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH_____(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和_________。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、_____ 、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、___________;
③烘干温度不超过110℃的原因是______。
-
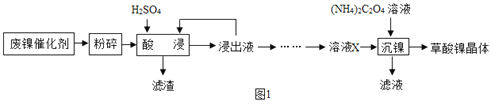
草酸镍晶体(NiC2O4•2H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如图所示:
已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Ni2+ | 6.7 | 9.5 |
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为______(填字母)。
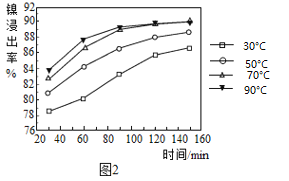
A 30℃、30min B 90℃、150min C 70℃、120min D 90℃、120min
(3)“酸浸”中发生的反应方程式为______(写1个即可)。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是______(填字母)
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液加NaOH溶液调节pH______(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和______,其中玻璃棒的作用是______。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、______、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、______。
③烘干温度不超过110℃的原因是______。
-
目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。可以说镍行业发展蕴藏着巨大的潜力。
Ⅰ制备草酸镍
工业上可利用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍(NiC2O4)。
根据下列工艺流程图回答问题:
(资料卡片1)
(1)过氧化氢(H2O2)俗称双氧水,是一种液体,受热易分解,可用于实验室制取氧气;过氧化氢具有强氧化性,所以常作为氧化剂、漂白剂和消毒剂。
(2)氧化反应可以从元素化合价升降的角度进行物质所含元素化合价升高的反应就是氧化反应。
(3)金属镍的化学性质类似于铁,与盐酸反应能生成氯化镍(NiCl2)。

(1)“酸溶”之后的滤渣中含有的金属是_______________。
(2)写出酸溶过程中Ni与盐酸反应的化学方程式_________________________。
(3)加H2O2时,温度不能太高,其原因是_______________________。若H2O2在“酸溶”步骤即与盐酸同时加入,则与原方案相比滤液中会增加的金属离子是Cu2+和_______(写离子符号)。
(4)已知Na2C2O4溶液加入NiCl2溶液发生复分解反应,写出该反应的化学方程式____________。
Ⅱ制备镍粉
工业用电解镍液(主要含NiSO4)制备碱式碳酸镍晶体xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉,过程如下:
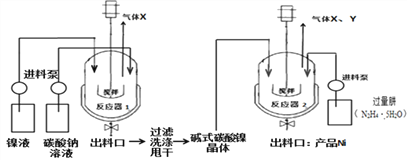
(5)反应器1中的一个重要反应为3NiSO4+3Na2CO3+2H2O  NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
(6)反应器1的出料口获得的固体洗涤时,需用纯水洗涤,可以用来检验固体已洗涤干净的试剂是____________。
(7)反应器2中产生的气体Y是空气中含量最多的气体,该气体是_________(填名称)。
Ⅲ 测定碱式碳酸镍晶体的组成
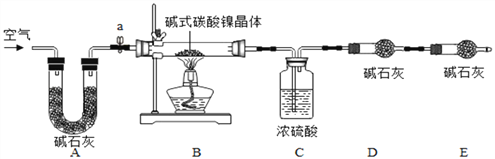
为测定碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)组成,某小组设计了如下实验方案及装置:
(资料卡片2)
(1)碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(2)在温度控制不当导致温度过高时,NiO会被氧化成Ni2O3
(3)碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
(实验步骤)
①检查装置气密性;②准确称取3.77g碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
| 装置C/g | 装置D/g | 装置E/g |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
(实验分析及数据处理)
(8)实验过程中步骤⑤鼓入空气的目的是__________________。
(9)计算3.77g碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)中镍元素的质量_________(写出计算过程,计算结果准确到小数点后两位)。
(实验反思)
(10)另一小组同学在实验中发现,实验结束后,称得装置B中残留固体质量明显偏大,老师带领全组同学经过仔细分析后发现,这是由于该组同学加热时在酒精灯上加了铁丝网罩,温度过高所导致。请问该组同学称得的残留固体中镍元素的质量分数可能是__________。
A.70.08% B.75.88% C.78.67% D.79.58%
-
目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。可以说镍行业发展蕴藏着巨大的潜力。
Ⅰ制备草酸镍
工业上可利用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍(NiC2O4)。
根据下列工艺流程图回答问题:
【资料卡片1】
(1)过氧化氢(H2O2)俗称双氧水,是一种液体,受热易分解,可用于实验室制取氧气;过氧化氢具有强氧化性,所以常作为氧化剂、漂白剂和消毒剂。
(2)氧化反应可以从元素化合价升降的角度进行分析:物质所含元素化合价升高的反应就是氧化反应。
(3)金属镍的化学性质类似于铁,与盐酸反应能生成氯化镍(NiCl2)。
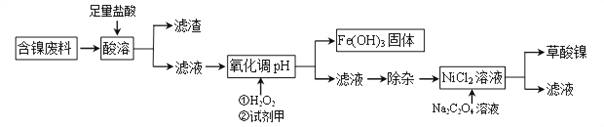
(1)“酸溶”之后的滤渣中含有的金属是_______________。
(2)写出酸溶过程中Ni与盐酸反应的化学方程式_________________________。
(3)加H2O2时,温度不能太高,其原因是_______________________。若H2O2在“酸溶”步骤即与盐酸同时加入,则与原方案相比滤液中会增加的金属离子是Cu2+和_______(写离子符号)。
(4)已知Na2C2O4溶液加入NiCl2溶液发生复分解反应,写出该反应的化学方程式____________。
Ⅱ制备镍粉
工业用电解镍液(主要含NiSO4)制备碱式碳酸镍晶体xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉,过程如下:
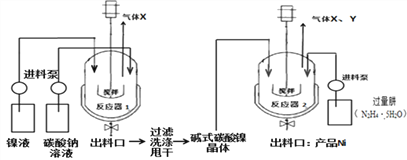
(5)反应器1中的一个重要反应为3NiSO4+3Na2CO3+2H2O  NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
(6)反应器1的出料口获得的固体洗涤时,需用纯水洗涤,可以用来检验固体已洗涤干净的试剂是____________。
(7)反应器2中产生的气体Y是空气中含量最多的气体,该气体是_________(填名称)。
Ⅲ 测定碱式碳酸镍晶体的组成
为测定碱式碳酸镍晶体【xNiCO3•yNi(OH)2•zH2O】组成,某小组设计了如下实验方案及装置:
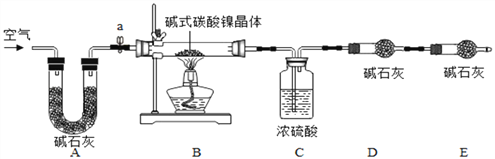
【资料卡片2】
(1)碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(2)在温度控制不当导致温度过高时,NiO会被氧化成Ni2O3
(3)碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
【实验步骤】
①检查装置气密性;②准确称取3.77g碱式碳酸镍晶体【xNiCO3•yNi(OH)2•zH2O】放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
| 装置C/g | 装置D/g | 装置E/g |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
【实验分析及数据处理】
(8)实验过程中步骤⑤鼓入空气的目的是__________________。
(9)计算3.77g碱式碳酸镍晶体【xNiCO3•yNi(OH)2•zH2O】中镍元素的质量_________(写出计算过程,计算结果准确到小数点后两位)。
【实验反思】
(10)另一小组同学在实验中发现,实验结束后,称得装置B中残留固体质量明显偏大,老师带领全组同学经过仔细分析后发现,这是由于该组同学加热时在酒精灯上加了铁丝网罩,温度过高所导致。请问该组同学称得的残留固体中镍元素的质量分数可能是__________。
A.70.08% B.75.88% C.78.67% D.79.58%
-
目前,全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
I、制备草酸镍(NiC2O4,其中Ni为+2价):
工业上用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍。
(资料卡片1):
(1).过氧化氢(H2O2)俗称双氧水,是一种液体,受热易分解,可用于实验室制取氧气;过氧化氢能将+2价铁氧化为+3价铁。
(2).金属镍的化学性质类似于铁,与盐酸反应能生成氯化镍(NiCl2)。
根据下列工艺流程图回答问题:
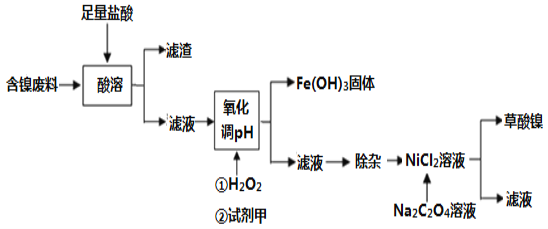
(1)酸溶之后的滤渣中含有的金属是____________(填化学式)。
(2)写出酸溶过程中Ni与盐酸反应的化学方程式____________。
(3)加H2O2时,温度不能太高,其原因是______________________,若H2O2在一开始酸溶时便与盐酸一起加入,则与原步骤酸溶过滤后的滤液相比,该滤液中会增加的金属离子是Cu2+和____________(写离子符号)。
(4)已知Na2C2O4溶液加入NiCl2溶液发生复分解反应,写出该反应的化学方程式_________。
II、镍粉制备:
工业用电解镍液(主要含NiSO4)制备碱式碳酸镍晶体xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉,过程如下:
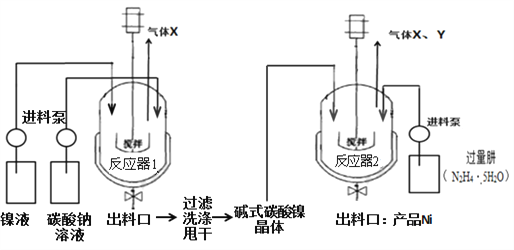
(5)反应器1中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2 +3Na2SO4+2X,X的化学式为_______________。
+3Na2SO4+2X,X的化学式为_______________。
(6)反应器1的出料口获得的固体洗涤时,需用纯水洗涤,可以用来检验固体洗涤干净的试剂是_______________。
(7)反应器2中产生的气体Y是空气中含量最多的气体,该气体是________(填化学式)。
III、测定碱式碳酸镍晶体的组成:
测定碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)组成的实验方案及装置如下图:
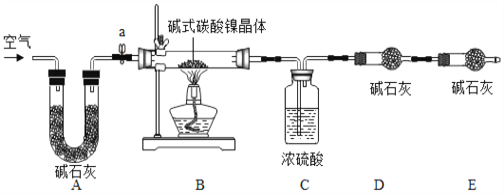
(资料卡片2):
碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(实验步骤):
①检查装置气密性;②准确称取3.77g碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
| 装置C/g | 装置D/g | 装置E/g |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
(实验分析及数据处理):
(8)计算3.77g碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)中镍元素的质量_____g。(写出计算过程,精确到小数点后两位)
-
镍粉常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
I.(镍粉制备):工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体 xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:
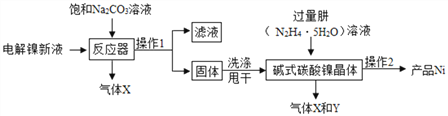
(1)反应器中一个重要反应为:3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2↓+3Na2SO4+2X,X的化学式为____。
(2)操作1名称是_____ , 洗涤操作1所得固体时,需用纯水洗涤,检验其洗净的方法(写出步骤、现象)___________________ 。
(3)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中95%酒精浸泡的目的 ______。
(4)物料在反应器中反应时需控制反应条件。分析下图,反应器中最适合的温度及pH分别为 ________________________ 。
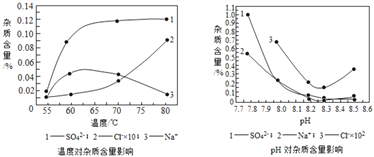
(5)生产中,pH逐渐增加,生成Ni(OH)2量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将__________填“升高”、“降低”或“不变”)。
Ⅱ.(测定碱式碳酸镍晶体的组成)
为测定碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O组成,某小组设计了如下实验方案及装置:
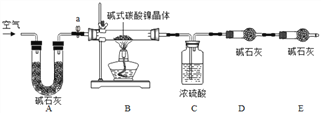
(资料卡片)
(1)碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(2)400℃左右,NiO会氧化生成Ni2O3.
(实验步骤):
①连接装置,_______ ;②准确称取3.77g xNiCO3•yNi(OH)2•zH2O放在B装置中,连接仪器;③打开弹簧夹a,缓缓鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤___________;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如下表)
| 装置C/g | 装置D/g | 装置E/g |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
(实验分析及数据处理):
(1)完善实验步骤中的填空:① 连接装置,_______ ;⑤___________。
(2)装置A的作用: 实验开始前、实验完毕时分别是__________________________
(3)计算xNiCO3•yNi(OH)2•zH2O中x:y:z 的值是______________。(写出计算过程)
-
镍粉常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
I、【镍粉制备】:
工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体xNiCO3·yNi(OH)2·zH2O,并利用其制备镍粉的流程如下:
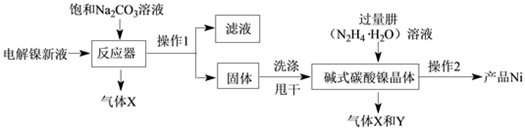
(1)反应器中的一个重要反应为3NiSO4 + 3Na2CO3 + 2H2O = NiCO3·2Ni(OH)2 +3Na2SO4 + 2X,X的化学式为______。
(2)物料在反应器中反应时需要控制反应条件。
分析下图,反应器中最适合的温度及pH分别为______℃、______。
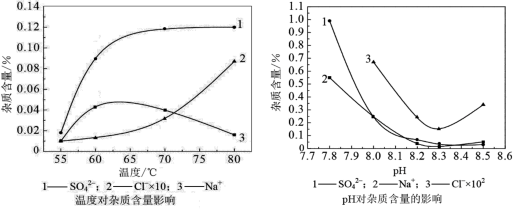
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将______(填“升高”、“降低”或“不变”)。
(4)操作1的名称是_______________,实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒及_________,其中玻璃棒的作用是_____。
(5)固体洗涤时,需用纯水洗涤,检验其洗涤干净的试剂是______。
(6)气体Y是空气中含量最多的气体,其是______(填名称)。
(7)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中用95%酒精浸泡的目的是______。
II、【测定碱式碳酸镍晶体的组成】:为测定碱式碳酸镍晶体(xNiCO3·yNi(OH)2·zH2O)组成,某小组设计了如下实验方案及装置:
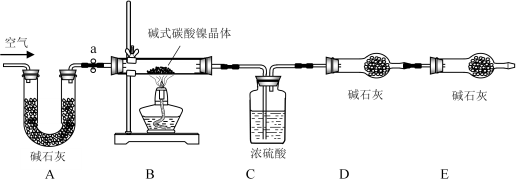
【资料卡片】:
①碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O。
②400℃左右,NiO会氧化生成Ni2O3。
③碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O。
【实验步骤】:
①______;②准确称取3.77g xNiCO3·yNi(OH)2·zH2O放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,______;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如表)。
| 装置C / g | 装置D / g | 装置E / g |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
【实验分析及数据处理】:
(8)完善实验步骤中的填空:①______;⑤______。
(9)计算xNiCO3·yNi(OH)2·zH2O中x:y:z的值______。
(10)左侧通空气的目的是______、______。
【实验反思】:
(11)实验结束后,称得装置B中残留固体质量为2.33g。请通过计算确定残留固体的组成及各成分的质量(写出计算过程,精确到小数点后两位)_____。
-
目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
Ⅰ.(镍粉制备)
工业用电解镍新液(主要含NiSO4,NiCl2等)制备碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O],并利用其制备镍粉的流程如下:
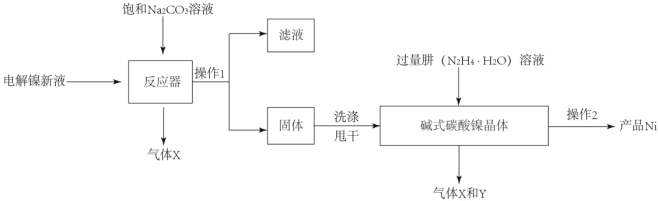
(1)反应器中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO3▪2Ni(OH)2+3Na2SO4+2X,X的化学式为_____。
(2)物料在反应器中反应时需要控制反应条件。
分析下图,反应器中最适合的温度及pH分别为_____℃、_____。
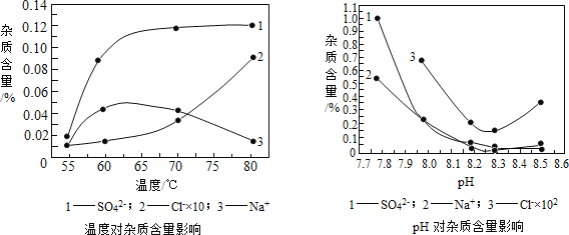
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将_____(填“升高”、“降低”或“不变”)。
(4)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中用95%酒精浸泡的目的是_____。
Ⅱ.(测定碱式碳酸镍晶体的组成)
为测定碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]组成,某小组设计了如下实验方案及装置:
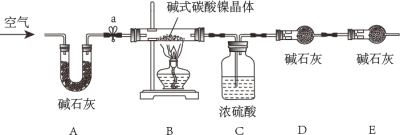
(资料卡片)
①碱式碳酸镍晶体受热会完全分解生成NiO、CO2和H2O
②碱石灰是NaOH和CaO的混合物,可以吸收CO2和H2O
(实验步骤)
①检查装置气密性;②准确称量3.77g碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;
④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)
| 装置C/g | 装置D/g | 装置E/g |
| 加热前 | 250.00 | 190.00 | 190.00 |
| 加热后 | 251.08 | 190.44 | 190.00 |
(实验分析及数据处理)
(1)实验过程中步骤⑤鼓入空气的目的是_____。
(2)计算3.77g碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]中镍元素的质量_____。最终通过计算得到了碱式碳酸镍晶体的组成。
(实验反思)
(3)另一小组同学加热时在酒精灯上加了铁丝网罩,实验结束后,称得装置B中残留固体质量明显增大。经查阅资料发现:在温度控制不当导致温度过高时,NiO会被氧化成Ni2O3。该组同学称得残留的固体中镍元素的质量分数可能是_____。
A 70.1% B 75.9% C 78.7% D 79.6%
-
目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
Ⅰ.(镍粉制备):
工业用电解镍新液(主要含NiSO4、NiCl2等)制备碱式碳酸镍晶体[xNiCO3·yNi(OH)2·zH2O],并利用其制备镍粉的流程如下:
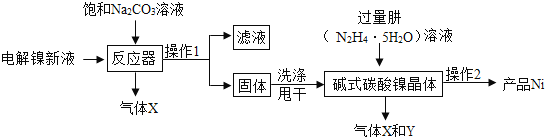
(1)反应器中的一个重要反应为3NiSO4 + 3Na2CO3 + 2H2O = NiCO3·2Ni(OH)2 +3Na2SO4 + 2CO2↑,生成的气体直接排放对环境的影响是___________。
(2)物料在反应器中反应时需要控制反应条件。
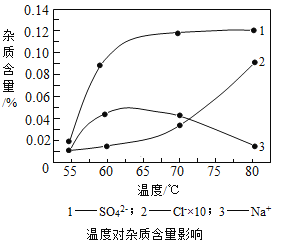
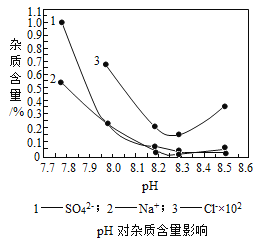
分析上图,反应器中最适合的温度及pH分别为__________、8.3。
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将_____________(填“升高”、“降低”或“不变”)。
(4)操作2含过滤、水洗、95%酒精浸泡、晾干等操作。其中使用95%酒精浸泡的目的是_________
Ⅱ.(测定碱式碳酸镍晶体的组成):
为测定碱式碳酸镍晶体[xNiCO3·yNi(OH)2·zH2O]组成,某小组设计了如下实验方案及装置:
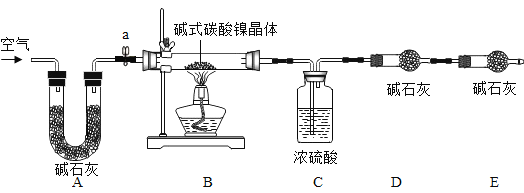
(资料卡片)
①碱式碳酸镍晶体受热会完全分解生成NiO、CO2和H2O
②碱石灰是NaOH和CaO的混合物,可以吸收CO2和H2O
(实验步骤)
①检查装置气密性;②准确称取7.54g碱式碳酸镍晶体[xNiCO3·yNi(OH)2·zH2O]放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
| 装置C/g | 装置D/g | 装置E/g |
| 加热前 | 250.00 | 190.00 | 190.00 |
| 加热后 | 252.16 | 190.88 | 190.00 |
(实验分析及数据处理)
(5)实验过程中步骤③鼓入空气的目的是__________。装置A的作用是______。
(6)计算7.54g碱式碳酸镍晶体[xNiCO3·yNi(OH)2·zH2O]完全分解中镍元素的质量__。最终通过计算得到了碱式碳酸镍晶体的组成,x:y:z=_______
(实验反思)
(7)另一小组同学加热时在酒精灯上加了铁丝网罩,实验结束后,称得装置B中残留固体质量明显偏大。经查阅资料发现:在温度控制不当导致温度过高时,NiO会部分被氧化成Ni2O3。 该组同学称得的残留固体混合物的质量可能是_____________。
A 4.5g B 4.6g C 4.98g D 5.2g