某同学设计的工业制备氢氧化钠的流程如图,下列说法正确的是( )
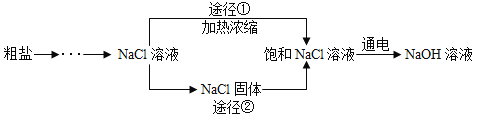
资料:2NaCl+2H2O2NaOH+H2↑+Cl2↑,两电极一端得到NaOH和H2,另一端得到Cl2。
A. 晾晒海水得到粗盐的原理是降温结晶
B. 实验室测定水的组成时,为了增强水的导电性,可以在水中加入氯化钠
C. 工业生产应选择途径①进行生产,因为该途径步骤简单,节约能源
D. 生产过程中得到的Cl2可用于自来水的消毒杀菌
九年级化学多选题中等难度题
某同学设计的工业制备氢氧化钠的流程如图,下列说法正确的是( )

资料:2NaCl+2H2O2NaOH+H2↑+Cl2↑,两电极一端得到NaOH和H2,另一端得到Cl2。
A. 晾晒海水得到粗盐的原理是降温结晶
B. 实验室测定水的组成时,为了增强水的导电性,可以在水中加入氯化钠
C. 工业生产应选择途径①进行生产,因为该途径步骤简单,节约能源
D. 生产过程中得到的Cl2可用于自来水的消毒杀菌
九年级化学多选题中等难度题
某同学设计的工业制备氢氧化钠的流程如图,下列说法正确的是( )

资料:2NaCl+2H2O2NaOH+H2↑+Cl2↑,两电极一端得到NaOH和H2,另一端得到Cl2。
A. 晾晒海水得到粗盐的原理是降温结晶
B. 实验室测定水的组成时,为了增强水的导电性,可以在水中加入氯化钠
C. 工业生产应选择途径①进行生产,因为该途径步骤简单,节约能源
D. 生产过程中得到的Cl2可用于自来水的消毒杀菌
九年级化学多选题中等难度题查看答案及解析
某同学设计的工业制备氢氧化钠的流程如图。
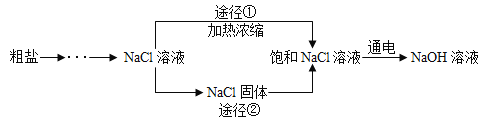
资料:①2NaCl + 2H2O2NaOH + H2↑+ Cl2↑,电极一端得到 NaOH 和 H2, 另一端得到Cl2。
②Cl2 用于生产 84 消毒液,其反应原理为:Cl2 + 2NaOH = NaCl + NaClO + H2O
(1)晾晒海水得到粗盐的原理是_________。
(2)实验室蒸发用到的仪器材料有铁架台、坩埚钳、石棉网、玻璃棒、酒精灯和______________。
(3)工业生产中应选择途径___________________获得饱和 NaCl 溶液。
(4)84 消毒液有效成分 NaClO 中氯元素的化合价为______________。
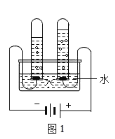
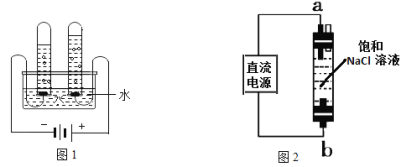
(5)图 1 实验探究水的组成,不能加入NaCl 增强水的导电性的理由是_____________;电解水的化学方程式___________________________________。
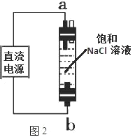
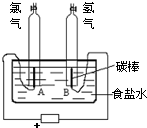
(6)图 2 实验获得 84 消毒液,直流电源正极应与______________ (填 a 或 b)连接, 才能使 NaClO 的含量更高。
九年级化学流程题简单题查看答案及解析
某同学设计的工业制备氢氧化钠的流程如图。
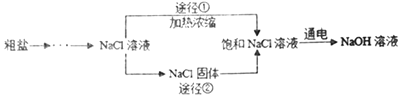
资料:2NaCl+2H2O2NaOH+H2↑+C12↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
(1)晾晒海水得到粗盐的原理是______。
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、坩埚钳、石棉网、酒精灯、玻璃棒和______。
(3)工业生产中应选择途径______(填“①”或“②”),理由是______。
(4)Cl2可用于生产84消毒液(有效成分NaClO),反应原理为:Cl2+2NaOH=NaCl+NaClO+H2O,反应前后氯元素的化合价有______种。
九年级化学流程题简单题查看答案及解析
某同学设计的工业制备氢氧化钠的流程如图。
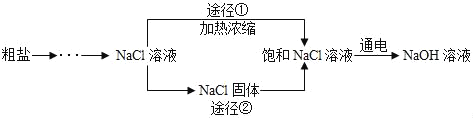
资料:2NaCl+2H2O2NaOH+H2↑+C12↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
(1)晾晒海水得到粗盐的原理是_____。
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、坩埚钳、石棉网、酒精灯、玻璃棒和_____。
(3)工业生产中应选择途径_____(填“①”或“②”),理由是_____。
(4)Cl2可用于生产84消毒液(有效成分NaClO),反应原理为:Cl2+2NaOH=NaCl+NaClO+H2O,反应前后氯元素的化合价有_____种。
九年级化学流程题简单题查看答案及解析
(9分)某同学设计的工业制备氢氧化钠的流程如下图。

资料:
2NaCl+2H2O2NaOH+H2↑+Cl2↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
(1)晾晒海水得到粗盐的原理是_______
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、坩埚钳、石棉网、酒精灯、玻璃棒和________
(3)工业生产中应选择途径______ (“①”或“②”),理由是______
(4)Cl2可用于生产84消毒液(有效成分NaClO),反应原理为:Cl2+2NaOH=NaCl+NaClO+H2O,反应前后氯元素的化合价有___种。
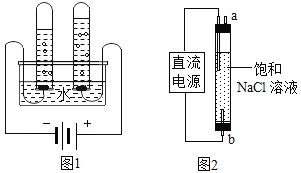
(5)图1实验测定水的组成,不能加入NaCl增强水的导电性的理由是____。电解水的化学方程式为________
(6)图2实验获得84消毒液,直流电源正极应与___(填a或b)连接,才能使NaClO的含量更高。
九年级化学流程题困难题查看答案及解析
(9分)某同学设计的工业制备氢氧化钠的流程如下图。
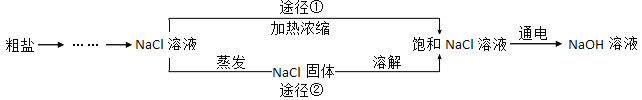
资料:
2NaCl+2H2O2NaOH+H2↑+Cl2↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
(1)晾晒海水得到粗盐的原理是_______
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、坩埚钳、石棉网、酒精灯、玻璃棒和________
(3)工业生产中应选择途径______ (“①”或“②”),理由是______
(4)Cl2可用于生产84消毒液(有效成分NaClO),反应原理为:Cl2+2NaOH=NaCl+NaClO+H2O,反应前后氯元素的化合价有___种。
(5)图1实验测定水的组成,不能加入NaCl增强水的导电性的理由是____。电解水的化学方程式为________
(6)图2实验获得84消毒液,直流电源正极应与___(填a或b)连接,才能使NaClO的含量更高。
九年级化学流程题困难题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
九年级化学选择题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析