黄铜是铜和锌的合金。为了测定某黄铜中铜的质量分数,称取10.0 g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时共用去98.0 g稀硫酸,将反应后的剩余物过滤、干燥,称得剩余固体3.5 g。试计算:(Zn + H2SO4 = ZnSO4 + H2↑)
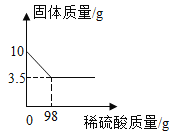
求:(1)铜样品中锌的质量_____(直接填结果);
(2)产生氢气的质量_____;
(3)所用稀硫酸溶液的溶质质量分数_____。
九年级化学计算题中等难度题
黄铜是铜和锌的合金。为了测定某黄铜中铜的质量分数,称取10.0 g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时共用去98.0 g稀硫酸,将反应后的剩余物过滤、干燥,称得剩余固体3.5 g。试计算:(Zn + H2SO4 = ZnSO4 + H2↑)

求:(1)铜样品中锌的质量_____(直接填结果);
(2)产生氢气的质量_____;
(3)所用稀硫酸溶液的溶质质量分数_____。
九年级化学计算题中等难度题
黄铜是铜和锌的合金。为了测定某黄铜中铜的质量分数,称取10.0 g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时共用去98.0 g稀硫酸,将反应后的剩余物过滤、干燥,称得剩余固体3.5 g。试计算:(Zn + H2SO4 = ZnSO4 + H2↑)

求:(1)铜样品中锌的质量_____(直接填结果);
(2)产生氢气的质量_____;
(3)所用稀硫酸溶液的溶质质量分数_____。
九年级化学计算题中等难度题查看答案及解析
黄铜是铜和锌的合金。为了测定某黄铜中铜的质量分数,称取10.0g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时共用去98.0g稀硫酸,将反应后的剩余物过滤、干燥,称得剩余固体3.5g。试计算:
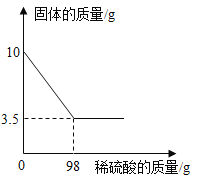
求:(1)铜样品中锌的质量是______(直接填结果);
(2)所用稀硫酸溶液的溶质质量分数是_____?(写过程)
九年级化学计算题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
黄铜是铜锌合金。可塑性好,耐腐蚀,许多金色饰品就是用它来制作的。现称取20.0 g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至没有气泡产生为止。请结合下列图示计算。

(1)该20.0 g黄铜样品中含锌的质量为________。
(2)完全反应时生成气体的质量为________g。
(3)计算所得溶液中溶质的质量分数为__________(结果精确到0.1%)。
九年级化学简答题中等难度题查看答案及解析
黄铜是铜锌合金。可塑性好,耐腐蚀,许多金色饰品就是用它来制作的。现称取20.0 g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至没有气泡产生为止。请结合下列图示计算。

(1)该20.0 g黄铜样品中含锌的质量为________。
(2)完全反应时生成气体的质量为________g。
(3)计算所得溶液中溶质的质量分数为__________(结果精确到0.1%)。
九年级化学计算题中等难度题查看答案及解析
某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10g样品放入烧杯中,再取60g稀硫酸分六次加入烧杯中,充分反应,实验数据如下:
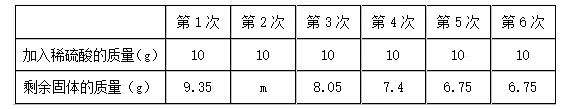
(1)m的值为 。
(2)黄铜样品中锌的质量分数为 。(写出计算步骤,下同)
(3)所用稀硫酸的溶质质量分数为多少?
九年级化学计算题中等难度题查看答案及解析
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入稀硫酸的质量(g) | 6 | 6 | 6 | 6 | 6 |
| 剩余固体的质量(g) | 9.22 | 8.44 | 7.66 | 6.88 | 6.88 |
九年级化学解答题中等难度题查看答案及解析
| 加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
| 第1次 | 10 | 8.7 |
| 第2次 | 10 | 7.4 |
| 第3次 | 10 | 6.1 |
| 第4次 | 10 | 5.6 |
| 第5次 | 10 | 5.6 |
九年级化学解答题中等难度题查看答案及解析
Cu与Zn的合金称为黄铜。为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
| 1 | 2 | 3 | 4 | 5 | |
| 加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 充分反应后剩余固体的质量(g) | 17.4 | 14.8 | 12.2 | 12.0 | m |
试回答下列问题:
(1)上述表格中m的值为 ;
(2)黄铜样品中锌的质量分数为 ;
(3)所用稀硫酸中硫酸的质量分数是多少?
九年级化学计算题中等难度题查看答案及解析
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
九年级化学解答题中等难度题查看答案及解析