-
硫酸在工业上有着重要的用途。
I.以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及工艺流程可简示如下:FeS2 SO2
SO2 H2SO4
H2SO4
(原理)
(工艺流程)
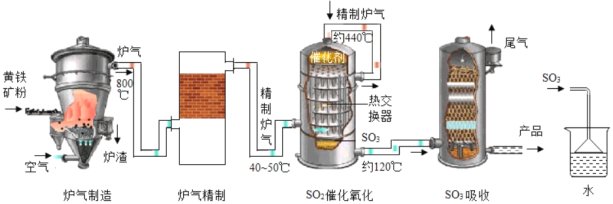
(1)黄铁矿是_____(填“纯净物”或“混合物”)工业生产过程中将矿石粉碎的目的是_____。
(2)在吸收装置中,液体由上而下形成喷雾状的目的是_____。
(3)在实验室模拟制硫酸时用如图装置吸收三氧化硫,除了达到与工业上相同的目的外,还可能考虑的因素是_____。
(4)工业上常用石灰乳来吸收尾气中的二氧化硫,请写出反应的化学方程式_____。(提示:生成物有一种是CaSO3)
II.黄铁矿锻烧后的另一种产物是铁的一种氧化物,其中铁氧质量比为7:3,则其化学式为_____。该物质可用来生产氯化铁晶体。氯化铁也是常用的净水剂之一,相比于明矾,其作为净水剂的优点是_____。
III.实验室中常用浓硫酸来配制稀硫酸。实验室用密度为1.84g/cm3、溶质质量分数为98%的浓硫酸来配制500g 20%,需要水_____g.溶解时,应_____,并用玻璃棒不断搅拌。该实验中还需用到的玻璃仪器有烧杯、量筒、_____。请写出稀硫酸的一种用途_____。
IV.某化工厂以黄铁矿为原料产生硫酸。如果该厂生产98%的浓硫酸100t,不考虑其他各生产阶段的物料损失,需要含FeS260%的矿石质量为多少吨?(写出计算过程)________________
-
硫酸在工业上有着重要的用途。
Ⅰ.以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及工艺流程可简示如下:
(原理)FeS2 SO2
SO2 SO3
SO3 H2SO4
H2SO4
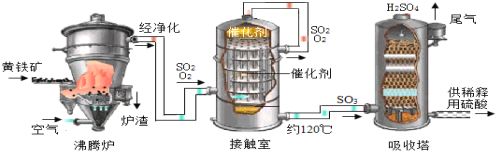
(工艺流程)
(1)黄铁矿是_____(填“纯净物”或“混合物”)。
(2)在吸收塔中,含水吸收液呈雾状由上向下喷酒,这样做的优点是_____
(3)工业上常用石灰乳来吸收尾气中的二氧化硫,反应的化学方程式是_____;
(4)下列有关说法中,不正确的是_____(填序号)。
A 将黄铁矿粉碎的目的是增大反应物之间的接触面积;
B 在原料质量一定的条件下,使用催化剂能提高SO3的产量;
C 生产过程中向空气里排放的大量SO2、SO3可能会引发酸雨;
D 排出的矿渣可用做工业炼铁的原料
Ⅱ.某化工厂以黄铁矿为原料生产硫酸。如果该厂生产98%的浓硫酸100t,不考虑其他各生产阶段的物料损失,理论上需要含FeS260%的矿石的质量为_____。
-
硫酸在工业上有着重要的用途。以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及工艺流程可简示如下:FeS2 SO2
SO2
 H2SO4
H2SO4
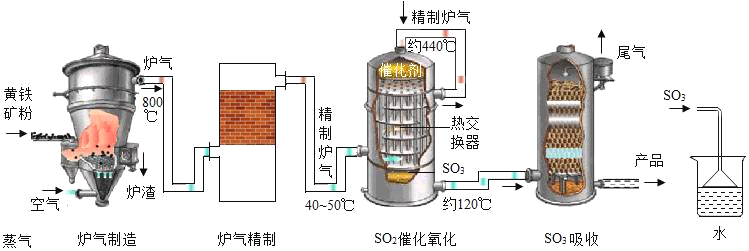
(1)工业生产过程中将矿石粉碎以及在吸收装置中液体由上而下形成喷雾状的目的是_____。
(2)在实验室模拟制硫酸时用如图装置吸收三氧化硫,除了达到与工业上相同的目的外,还可能考虑的因素是_____。
(3)工业上常用熟石灰来吸收尾气中的二氧化硫,请写出反应的化学方程式_____。(提示:生成物有一种是CaSO3)
(4)实验室中常用浓硫酸来配制稀硫酸。稀释时,正确操作是,_____,并用玻璃棒不断搅拌。
-
硫酸在工业上有着重要的用途。以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及工艺流程可简示如下:FeS2 SO2
SO2
 H2SO4
H2SO4
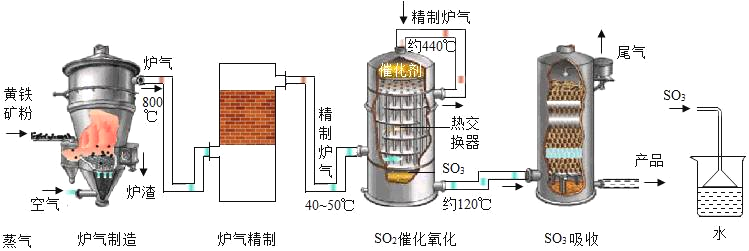
(1)工业生产过程中将矿石粉碎以及在吸收装置中液体由上而下形成喷雾状的目的是_____。
(2)在实验室模拟制硫酸时用如图装置吸收三氧化硫,除了达到与工业上相同的目的外,还可能考虑的因素是_____。
(3)工业上常用熟石灰来吸收尾气中的二氧化硫,请写出反应的化学方程式_____。(提示:生成物有一种是CaSO3)
(4)实验室中常用浓硫酸来配制稀硫酸。稀释时,正确操作是,_____,并用玻璃棒不断搅拌。
-
硫酸(H2SO4)是一种用途广泛的化工原料,工业上常用煅烧黄铁矿(主要成分是FeS2)的方法来生产硫酸,简要的工艺流程图如下:
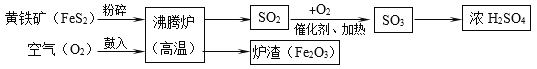
(1)黄铁矿投入沸腾炉前粉碎的目的是________。
(2)在沸腾炉中发生的反应为:(______)FeS2+(______)O2  (______)Fe2O3+(______)SO2(请在化学式前面配上适当的化学计量数),得到的炉渣(Fe2O3)可用来炼铁。
(______)Fe2O3+(______)SO2(请在化学式前面配上适当的化学计量数),得到的炉渣(Fe2O3)可用来炼铁。
(3)请写出流程中SO2转化为SO3的化学方程式_________。
(炉渣的综合利用)
为了实现炉渣(Fe2O3)的综合利用,工业上把炉渣和焦炭、石灰石一起投入高炉,主要反应过程如图:

(4)步骤②发生反应的化学方程式为______。
(5)下列有关高炉炼铁的说法正确的是_______(填序号)。
A.上述流程中涉及的三个反应均为吸热反应
B.上述步骤①反应中,还原剂是焦炭
C.焦炭的作用之一是为炼铁炉提供高温条件
D.焦炭的另一个作用是除去铁矿石中的杂质
(6)分析高炉所得的生铁中单质铁的含量:
小瑾同学为测定生铁中铁的质量分数,先后进行了四次实验,实验数据记录如下表。根据她的实验数据,试计算生铁中铁的质量分数是_________?
| 第一次 | 第二次 | 第三次 | 第四次 |
| 所取生铁的质量∕g | 10 | 10 | 10 | 10 |
| 所加稀硫酸的质量∕g | 25 | 50 | 75 | 100 |
| 生成氢气的质量∕g | 0.10 | 0.20 | 0.30 | 0.35 |
(反思质疑)
小宇同学在梳理工业炼铁的相关知识时,提出了以下质疑:
(质疑一)焦炭也具有还原性而且成本低,工业炼铁为什么不直接用焦炭作为还原剂冶炼铁矿石?
(7)他设计了下图所示的一组对比实验:称取两份相同质量的氧化铁粉末,一份与足量的焦炭粉末混合均匀放入装置A的试管中,另一份放入装置B的玻璃管中。
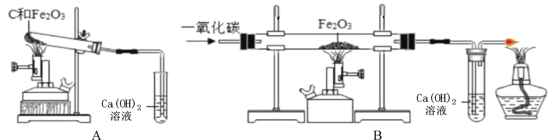
①装置B的玻璃管中发生反应的化学方程式为________。
②当他观察到装置B的玻璃管中固体_________、澄清石灰水变浑浊时,装置A的试管中尚无明显现象。
③通过上述实验对比,小宇同学认为工业上不直接用焦炭作为还原剂炼铁的主要原因有:反应不充分、反应速度慢、_______等。
(质疑二)装置B中反应后的黑色固体一定就是单质铁吗?
(查阅资料)
a.铁常见的氧化物有氧化铁(Fe2O3)、四氧化三铁(Fe3O4)和氧化亚铁(FeO)。
b.四氧化三铁是具有磁性的黑色晶体,氧化亚铁是不溶于水的黑色粉末,无磁性,也不能被磁铁吸引。
④小宇同学设计了如下实验方案:用磁铁吸引装置B进行实验后的黑色固体,发现黑色固体可以部分被吸引,由此得出结论:黑色固体的成分是___________。
-
(2011•海门市二模)工业制硫酸主要分造气、氧化反应和吸收三个阶段.硫酸的生产流程如下(其中黄铁矿的主要成分为FeS2):
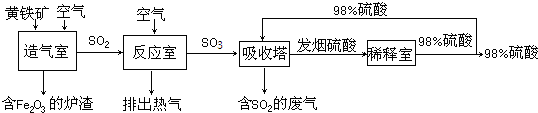
请结合硫酸的生产流程回答:
(1)流程中含Fe2O3炉渣的用途是:______;在反应室中要不断排出热气,才能维持反应室的温度恒定.说明反应室中的化学反应是______(填“放热”或“吸热”)反应.含有SO2的废气造成空气的危害是:______.
(2)实验室通过稀释98%的浓硫酸配制20%稀硫酸98g,则需要加水的质量为______.
(3)用含硫元素32%的黄铁矿在反应流程中有2%的硫受到损失而混入炉渣和废气中(假设在SO2、吸收中没有损失).则这种黄铁矿石10t可以制得98%的硫酸多少t?
-
工业制硫酸主要分造气、氧化反应和吸收三个阶段.硫酸的生产流程如下(其中黄铁矿的主要成分为FeS2):
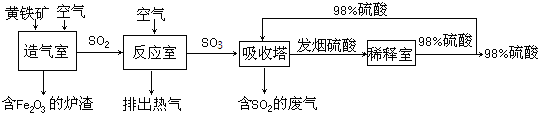
请结合硫酸的生产流程回答:
(1)流程中含Fe2O3炉渣的用途是:______;在反应室中要不断排出热气,才能维持反应室的温度恒定.说明反应室中的化学反应是______(填“放热”或“吸热”)反应.含有SO2的废气造成空气的危害是:______.
(2)实验室通过稀释98%的浓硫酸配制20%稀硫酸98g,则需要加水的质量为______.
(3)用含硫元素32%的黄铁矿在反应流程中有2%的硫受到损失而混入炉渣和废气中(假设在SO2、吸收中没有损失).则这种黄铁矿石10t可以制得98%的硫酸多少t?
-
工业制硫酸主要分造气、氧化反应和吸收三个阶段.硫酸的生产流程如下(其中黄铁矿的主要成分为FeS2):
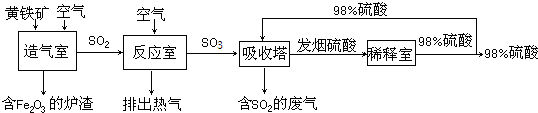
请结合硫酸的生产流程回答:
(1)流程中含Fe2O3炉渣的用途是:______;在反应室中要不断排出热气,才能维持反应室的温度恒定.说明反应室中的化学反应是______(填“放热”或“吸热”)反应.含有SO2的废气造成空气的危害是:______.
(2)实验室通过稀释98%的浓硫酸配制20%稀硫酸98g,则需要加水的质量为______.
(3)用含硫元素32%的黄铁矿在反应流程中有2%的硫受到损失而混入炉渣和废气中(假设在SO2、吸收中没有损失).则这种黄铁矿石10t可以制得98%的硫酸多少t?
-
硫铁矿[主要成分是二硫化亚铁(FeS2)],其他成分不含铁,硫元素是一种重要的化工原料,常用来制备硫酸和氯化铁,工业生产流程如图所示。
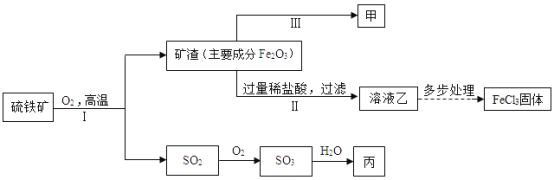
(1)过滤中玻璃棒的作用 _____。
(2)步骤二中主要反应的化学方程式为 _____。
(3)溶液乙中一定有的阳离子_____。
(4)上述流程中所涉及的含硫的物质中,硫元素的化合价共有_____种。
-
工业上以黄铁矿(主要成分是FeS2)为原料,生产硫酸的简要流程图如下:
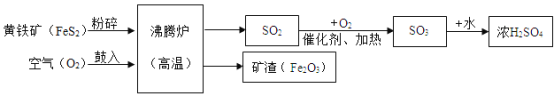
(1)写出流程图中一种氧化物的名称_____。
(2)将黄铁矿粉碎,目的是_____。
(3)请写出黄铁矿在沸腾炉里发生的化学反应方程式____。该反应中的____(填元素符号)从反应前到反应后化合价升高。
(4)该生产流程的炉渣可以做工业炼铁的原料,请写出工业炼铁反应化学方程式______。此外古代记载的湿法冶金技术有“曾青得铁则化为铜”,写出有关化学方程式________。
SO2
SO3
H2SO4











