一种制备氢氧化镁的生产流程如图所示,MgCl2和NaOH按恰好完全反应的比例加料。
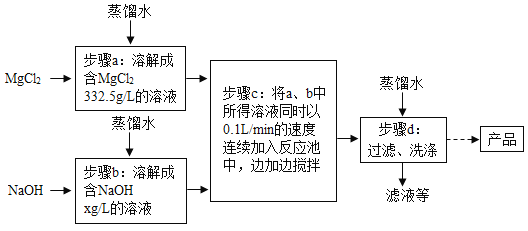
(1)写出步骤c中发生反应的化学方程式:_____。
(2)x=_____。
(3)过滤得到的粗产品还要经过洗涤,洗涤时主要除去的杂质是_____。
(4)如图流程中若用下列物质代替氢氧化钠,也能制得氢氧化镁的是_____。
①盐酸 ②氯化钙 ③氨水 ④硫酸镁
九年级化学填空题中等难度题
一种制备氢氧化镁的生产流程如图所示,MgCl2和NaOH按恰好完全反应的比例加料。

(1)写出步骤c中发生反应的化学方程式:_____。
(2)x=_____。
(3)过滤得到的粗产品还要经过洗涤,洗涤时主要除去的杂质是_____。
(4)如图流程中若用下列物质代替氢氧化钠,也能制得氢氧化镁的是_____。
①盐酸 ②氯化钙 ③氨水 ④硫酸镁
九年级化学填空题中等难度题
一种制备氢氧化镁的生产流程如图所示,MgCl2和NaOH按恰好完全反应的比例加料。

(1)写出步骤c中发生反应的化学方程式:_____。
(2)x=_____。
(3)过滤得到的粗产品还要经过洗涤,洗涤时主要除去的杂质是_____。
(4)如图流程中若用下列物质代替氢氧化钠,也能制得氢氧化镁的是_____。
①盐酸 ②氯化钙 ③氨水 ④硫酸镁
九年级化学填空题中等难度题查看答案及解析
粗盐中含有MgCl2、CaCl2等杂质,必须进行分离和提纯后才能用于工业生产和人们的日常生活。粗盐提纯的部分流程如图:请回答:
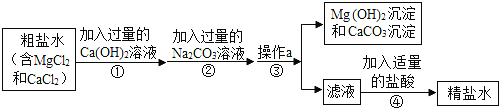
(1)写出步骤①中所发生的化学反应___________。
(2)步骤②加入过量的碳酸钠溶液的目的是什么_________________?
(3)步骤④获得精盐水后,通过什么操作得到食盐晶体________________?
九年级化学流程题中等难度题查看答案及解析
氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图:
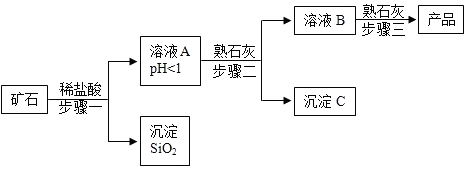
(1)请写出步骤一中发生反应的化学方程式: (任写一个)
(2)溶液A中所含的阳离子有 (填离子符号)
(3)已知:部分金属阳离子以氢氧化物形成沉淀时溶液的pH见表
| 沉淀物 | Fe(OH)2 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀 | 1.9 | 4.2 | 9.1 |
| 完全沉淀 | 3.2 | 6.7 | 11.1 |
步骤二中加入熟石灰,调节溶液的pH范围为
(4)3个步骤中均用到的操作是
(5)步骤三中生成产品的化学方程式为 .
九年级化学填空题中等难度题查看答案及解析
工业上以粗盐(含少量MgCl2、CaCl2杂质)为原料,利用电解饱和食盐水的方法制备NaOH,其简要工艺流程如下:
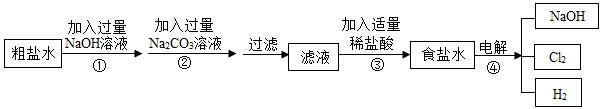
(1)步骤①中发生反应的基本反应类型是_____________反应.
(2)步骤③中加入适量稀盐酸的目的是_____________.
(3)验证步骤②中CaCl2已完全转化为CaCO3的方法是_____________.
(4)写出步骤④中反应的化学方程式_____________.
九年级化学填空题困难题查看答案及解析
利用氢氧化镁制备金属镁的主要流程如图:
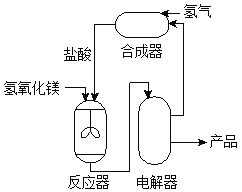
(1)反应器中搅拌的目的是______。
(2)反应器中发生的反应属于基本反应类型中______反应。
(3)电解器中发生反应的化学方程式为:MgCl2Mg + Cl2↑。生产24 kg金属镁,理论上需要氯化镁的质量是______kg。
九年级化学流程题简单题查看答案及解析
(3分)海水的综合利用可以制备金属镁,其流程如下图所示:
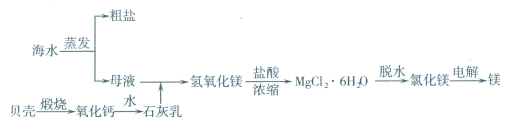
(1)若在空气中加热MgCl2·6H2O,会生成氧化镁,所以要在氯化氢气流中加热MgCl2·6H2O制备氯化镁,分别写出相应反应的化学方程式 、
(2)上述流程中母液加入石灰乳后,过滤,写出实验室里从滤渣得到纯净氢氧化镁的方法。
九年级化学填空题中等难度题查看答案及解析
已知20g氢氧化钠溶液与10g氯化镁溶液恰好完全反应,反应结束后过滤,滤液的质量为27.1g(不考虑实验过程的损失)。(反应的化学方程式:2NaOH + MgCl2 =Mg(OH)2↓ + 2NaCl )计算:
(1)反应生成的Mg(OH)2的质量为多少。
(2)参加反应的氢氧化钠溶液的溶质质量分数?(写出计算过程)
九年级化学计算题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析

九年级化学解答题中等难度题查看答案及解析
用作牙膏摩擦剂的轻质碳酸钙可以用矿石来制备,某化学兴趣小组设计了
种转化流程,如图所示.
(生产流程)
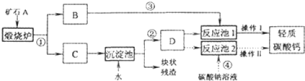
(相关资料)
.二氧化碳持续通入氢氧化钙溶液发生如下反应:
,
;
.碳酸氢钙微溶于水,微热易分【解析】
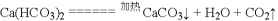 ;
;
.生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆.
(问题讨论)
小王主张用流程①、②、④和操作
的设计.请写出反应①和④的化学方程式:
①________;④________;
操作包括搅拌和________、洗涤、烘干等工序;该流程中,通过反应④可回收副产品_____.
小李认为流程①、②、③和操作
比小王的主张更好,理由是:________;
制轻质碳酸钙时,
为________(选填“悬浊液”或“溶液”),理由是:________.
小李认为得到的产品中可能含有杂质
,所以操作
包括搅拌、________和过滤、烘干等工序,以提高产率.
(产品含量测定)含量的测定:取
产品,研成粉状后,按图进行实验.
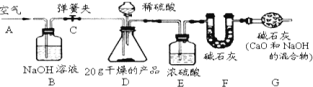
实验步骤:
①连接好装置,检查气密性; ②打开弹簧夹,在
处缓缓通入一段时间空气;
③称量的质量; ④关闭弹簧夹
,慢慢滴加稀硫酸至过量,直至
中无气泡冒出;
⑤打开弹簧夹,再次缓缓通一段时间空气;⑥称量
的质量,得前后两次质量差为
.
问题探究
①产品研成粉的目的________;
②装置的作用是________;
装置的作用是________,
③若没有装置,则测定的
的质量分数会________(填“偏大”、“偏小”、“不变”).
称量的质量,得前后两次质量差为
,可求得产品中
的质量分数为________
.
(总结反思)
某同学设计上述实验方案测定牙膏中钙元素的质量分数:向一定量牙膏中加入过量稀盐酸,测定生成的质量,据此计算牙膏中钙元素的质量分数.小李同学认为即使排除实验仪器和操作的影响,上述测定的结果仍不一定准确,理由是________.
九年级化学综合题困难题查看答案及解析