氯化钴(CoCl2)晶体因含结晶水数目不同而呈现不同的颜色,故可作硅胶干燥剂的指示剂和隐形墨水。通过下列几种方法制备氯化钴:①②
③
下列判断错误的是
A.②、③均为复分解反应
B.钻的金属活动性比铜强
C.氢氧化钴是一种碱
D.无水氯化钴可吸收空气中的水蒸气
九年级化学单选题简单题
氯化钴(CoCl2)晶体因含结晶水数目不同而呈现不同的颜色,故可作硅胶干燥剂的指示剂和隐形墨水。通过下列几种方法制备氯化钴:①②
③
下列判断错误的是
A.②、③均为复分解反应
B.钻的金属活动性比铜强
C.氢氧化钴是一种碱
D.无水氯化钴可吸收空气中的水蒸气
九年级化学单选题简单题
氯化钴(CoCl2)晶体因含结晶水数目不同而呈现不同的颜色,故可作硅胶干燥剂的指示剂和隐形墨水。通过下列几种方法制备氯化钴:①②
③
下列判断错误的是
A.②、③均为复分解反应
B.钻的金属活动性比铜强
C.氢氧化钴是一种碱
D.无水氯化钴可吸收空气中的水蒸气
九年级化学单选题简单题查看答案及解析
氧化钴(CoO)溶于盐酸可得到粉红色的氯化钴(CoCl2)溶液。CoCl2含结晶水数目不同而呈现不同颜色。利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的六水氯化钴晶体(CoCl2•6H2O)受热分解时,剩余固体质量随温度变化的曲线。
已知:①CoCl2•6H2O的相对分子质量为CoCl2和6个结晶水的相对分子质量之和。
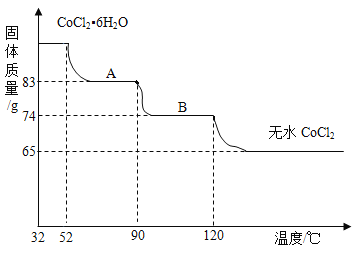
②CoCl2•6H2O受热分解完全脱水的化学方程式为:
CoCl2•6H2OCoCl2+6H2O。
请回答:
(1)CoCl2的钴元素的化合价为_____价。
(2)求物质A(CoCl2•xH2O)中的x值。
九年级化学计算题简单题查看答案及解析
(4分)氢氧化钴[Co(OH)2] 可作涂料和清漆的干燥剂,其制备方法是:把金属钴与稀盐酸反应制得氯化钴(CoCl2),再将氯化钴溶液与氢氧化钠溶液反应制得氢氧化钴。
查阅资料:氯化钴溶液是粉红色,氢氧化钴是难溶于水的粉红色固体。请回答:
(1)金属钴与稀盐酸反应的化学方程式为 。
(2)氯化钴溶液与氢氧化钠溶液反应的现象是 ,化学方程式为 。
(3)下列说法正确的是 。
A.钴的金属活动性比铜的强
B.氢氧化钴可以干燥氯化氢气体
C.氯化钴溶液也能和石灰水反应
九年级化学推断题困难题查看答案及解析
(6分)氢氧化钴[Co(OH)2] 可作涂料和油漆的干燥剂,其制备方法是:把金属钴与稀盐酸反应制得氯化钴(CoCl2),再将氯化钴溶液与氢氧化钠溶液反应制得氢氧化钴。
查阅资料:氯化钴溶液是粉红色,氢氧化钴是难溶于水的粉红色固体。请回答:
(1)预测金属钴与稀盐酸反应的现象 。
(2)氯化钴溶液与氢氧化钠溶液反应的化学方程式是 。
(3)下列说法正确的是 。
A.钴的金属活动性比铜的强
B.氢氧化钴不能与盐酸反应
C.氯化钴溶液也能和石灰水反应
九年级化学填空题中等难度题查看答案及解析
九年级化学选择题中等难度题查看答案及解析
许多植物花瓣的浸出液遇到酸性或碱性溶液都会呈现出不同的颜色,在化学实验室中,常用作酸碱指示剂.现提取几中植物花瓣的浸出液分别滴入三种溶液中,实验记录如下表:
| 植物浸出液 | 稀盐酸溶液 | 氯化钠溶液 | 稀氢氧化钠溶液 |
| 万寿菊 | 黄色 | 黄色 | 黄色 |
| 牵牛花 | 红色 | 紫色 | 蓝色 |
| 玫瑰花 | 浅红色 | 浅红色 | 绿色 |
请分析并回答下列问题:
(1)上述花瓣浸出液中,不能作酸碱指示剂的是 .
(2)若将牵牛花浸出液加入到食醋中,溶液会变 色,若将玫瑰花浸出液加入某无色溶液中,溶液变绿色,则该溶液是pH 7(填“>”、“<”或“=”)
九年级化学填空题中等难度题查看答案及解析
下列方法能达到除去杂质目的的是
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | 铜粉 | 木炭粉 | 在空气中灼烧 |
| B | 二氧化碳 | 水蒸气 | 通过足量的氢氧化钠固体,干燥 |
| C | 氯化钾 | 碳酸钾 | 加适量的稀盐酸,蒸发结晶 |
| D | 硫酸亚铁溶液 | 硫酸铜溶液 | 加入少量铁粉过滤 |
A.A B.B C.C D.D
九年级化学单选题困难题查看答案及解析
除去下列物质中所含的少量杂质,下表中除杂方法正确的是 ( )
选项 物 质 所含杂质 除杂质的方法
A 氧化铜 氯化钠 加水溶解、过滤、蒸发结晶
B 二氧化硫 水蒸气 通过盛有烧碱的干燥管
C 硫酸钠溶液 稀硫酸 加入适量碳酸钠溶液
D 二氧化碳 一氧化碳 点燃
九年级化学选择题困难题查看答案及解析
除去下列物质中所含的少量杂质,下表中除杂方法正确的是
| 选项 | 物 质 | 所含杂质 | 除杂质的方法 |
| A | 氧化铜 | 氯化钠 | 加水溶解、过滤、蒸发结晶 |
| B | 二氧化硫 | 水蒸气 | 通过盛有烧碱的干燥管 |
| C | 硫酸钠溶液 | 稀硫酸 | 加入适量碳酸钠溶液 |
| D | 二氧化碳 | 一氧化碳 | 点燃 |
九年级化学选择题中等难度题查看答案及解析
学习结晶时,同学们对硝酸钾的制备产生浓厚兴趣.
(一)通过查阅资料发现硝酸钾在农业市场用途十分广泛.工业上常采用硝酸钠与氯化钾在一定条件下反应制得硝酸钾和氯化钠.然后再利用硝酸钾和氯化钠在不同温度下的溶解度不同可将其分离,具体流程可以表示为:
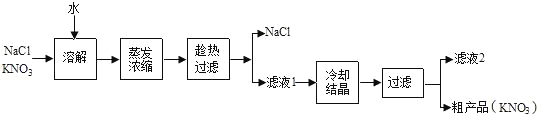
(1)溶解时需要不断搅拌,其目的是_____.
(2)化学实验室蒸发操作所需的玻璃仪器除玻璃棒外还有_____.
(3)分离氯化钠晶体和滤液1时需要趁热过滤的目的是_____.
(4)滤液1一定是_____的饱和溶液.
(5)冷却结晶后获得的硝酸钾晶体中还混有少量的NaCl,为获得更纯净的KNO3,还应进行的操作是洗涤、干燥,洗涤最佳的洗涤剂为_____.
A 常温下的蒸馏水 B 饱和的NaCl溶液 C 饱和的KNO3溶液
(6)洗涤后的液体应该_____.
A 不经处理直接排放到下水道
B 不经处理直接排放到农田
C 倒入原混合溶液中,节约资源并提高产率
(二)为测定洗涤前的粗产品中硝酸钾的质量分数,设计如下实验:取5g粗产品配成50g溶液,然后加入过量的硝酸银溶液(已知NaCl+AgNO3═AgCl↓+NaNO3,硝酸钾和硝酸银不反应),根据沉淀质量先求出NaCl质量,再确定硝酸钾的质量分数.
(7)硝酸银溶液需要过量的原因是_____,证明硝酸银已过量的方法是:静置后,在上层清液中加入硝酸银溶液,如果观察到_____(填有或无)沉淀生成,则已过量.
(8)在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中的硝酸钾的质量分数_____(填偏大、偏小或无影响),对所测定的粗产品中硝酸钾的质量分数_____.(填偏大、偏小或无影响)
(9)经精确测定AgCl沉淀的质量为1.435g,则5g粗产品配成的50g溶液中NaCl的质量分数为_____;该粗产品中硝酸钾的质量分数_____.(写出计算过程,相关物质的相对分子质量:NaCl 58.5,AgCl 143.5).
九年级化学流程题困难题查看答案及解析