-
Mg(OH)2 具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂、过滤,得到只含 MgSO4 和 H2SO4 的混合溶液,为确定混合溶液中镁的含量,取 4 份混合溶液各 100g 向每份混合溶液中加入一定质量的 4%NaOH 溶液,得到实验数据如下表所示:
实验编号
①
②
③
④
NaOH 溶液质量/g
10.0
20.0
30.0
40.0
Mg(OH)2质量/g
0.232
0.522
0.580
0.580
求:100g 混合溶液中含 MgSO4 的质量为多少 g?(要求写出完整计算过程)
九年级化学计算题中等难度题查看答案及解析
-
Mg(OH)2具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂、过滤,得到只含 MgSO4和 H2SO4的混合溶液,为确定混合溶液中镁的含量,取 4 份混合溶液各 100g,向每份混合溶液中加入一定质量的 4% NaOH溶液,得到实验数据如下表所示:
实验编号
①
②
③
④
NaOH 溶液质量/g
10.0
20.0
30.0
40.0
Mg(OH)2质量/g
0.232
0.522
0.580
0.580
(1)实验 (填实验编号)中硫酸镁完全反应。
(2)计算 100g 混合溶液中含 MgSO4的质量(写出计算过程)
九年级化学计算题中等难度题查看答案及解析
-
Mg(OH)2具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂、过滤,得到只含 MgSO4和 H2SO4的混合溶液,为确定混合溶液中镁的含量,取 4 份混合溶液各 100g,向每份混合溶液中加入一定质量的 4% NaOH溶液,得到实验数据如下表所示:
实验编号
①
②
③
④
NaOH 溶液质量/g
10.0
20.0
30.0
40.0
Mg(OH)2质量/g
0.232
0.522
0.580
0.580
(1)实验 (填实验编号)中硫酸镁完全反应。
(2)计算 100g 混合溶液中含 MgSO4的质量(写出计算过程)
九年级化学计算题中等难度题查看答案及解析
-
氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于酸)为原料制备高纯氧化镁的实验流程如下:
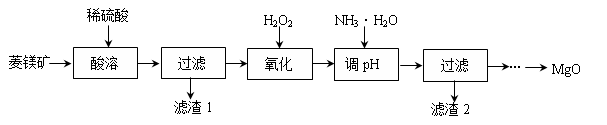
(1)酸溶之前要将矿石粉碎的目的是 。稀硫酸需要过量的目的是 。酸溶步骤中碳酸镁溶解的反应方程式为 。
(2)已知Mg2+、Fe2+和Fe3+在溶液中遇到氨水均可以转化成难溶性碱沉淀,开始沉淀和沉淀完全的pH如下表:
Mg2+
Fe2+
Fe3+
开始沉淀
9.4
7.9
2.7
沉淀完全
12.4
9.6
3.7
流程“氧化”一步中H2O2的作用是将溶液中的Fe2+转化成Fe3+,不能直接沉淀Fe2+的原因是 。
(3)加氨水调节溶液的PH范围为 。
(4)滤渣2的化学式是 。
九年级化学填空题中等难度题查看答案及解析
-
(7分)氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
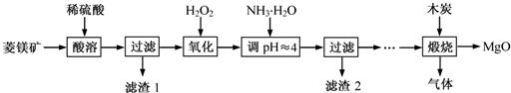
(1)MgCO3与稀硫酸反应的化学方程式为 ;
(2)加入H2O2 氧化时,发生反应的化学方程式为(已经配平,X属于常见的化合物):
,则X的化学式为 ;
(3)NH3·H2O是氨水的主要成分,溶液显 性,加入氨水时,溶液的PH值 (填“增大”、“减少”或“不变”),当PH≈4时,会产生红褐色沉淀,则滤渣2 的成分是 (填化学式)。
(4)通常用PH试纸测定溶液的PH值,其操作方法是 。
(5)煅烧过程存在以下反应:木炭和硫酸镁在高温下除得到氧化镁外,还得两种气体,一种会造成酸雨,另一种大量排放则会引起温室效应。请写出该反应的化学方程式: 。
九年级化学填空题困难题查看答案及解析
-
氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:
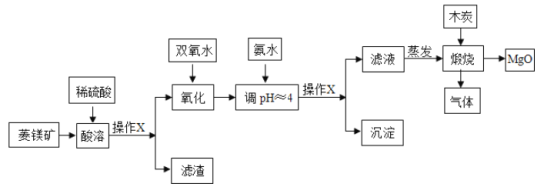
(1)操作X的名称是_____,该操作需要用到的玻璃仪器主要有:烧杯、_____、玻璃棒.
(2)蒸发过程中,要用玻璃棒不断地搅拌,其目的是_____.
(3)碳酸镁与稀硫酸反应的化学方程式为_____;该反应属于_____反应.
(4)加入双氧水氧化时,发生反应的化学方程式为:2FeSO4+H2O2+H2SO4═Fe2(SO4)3+2X.则X的化学式为_____.
(5)煅烧过程存在以下反应:2MgSO4+C
2MgO+2SO2↑+CO2↑;MgSO4+C
MgO+SO2↑+CO↑;MgSO4+3C
MgO+S↑+3CO↑.利用下图装置对煅烧产生的气体进行分步吸收或收集.
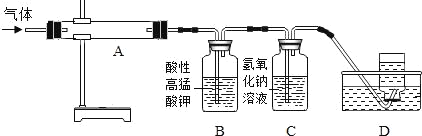
资料:酸性高锰酸钾能吸收二氧化硫;硫蒸气在A装置冷凝成固体.
①上述反应产生的气态氧化物中_____(填化学式)不会对空气造成污染.
②D中收集到的气体具有_____(填一种化学性质).
③C中发生反应的化学方程式为_____.
(6)若直接煅烧100t含碳酸镁84%的菱镁矿,理论上可制得氧化镁多少_____?
九年级化学综合题中等难度题查看答案及解析
-
金属﹣工业的脊梁。金属及合金广泛应用于生活、生产和航天军工。
资料:水圈和岩石圈中含有丰富的镁元素。工业生产中,可用菱镁矿做原科制备金属镁,流程如图所示:
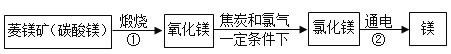
请回答下列问题:
(1)已知①和②属于分解反应,写出②的化学方程式_____。
(2)通过化学反应,以岩石圈的矿石为原料还可以制备很多其他金属,请举一例说明_____(用化学方程式表示其制备原理)。
(3)如图
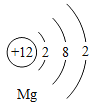 是镁原子结构示意图,镁化学性质活泼,原因是
是镁原子结构示意图,镁化学性质活泼,原因是九年级化学流程题中等难度题查看答案及解析
-
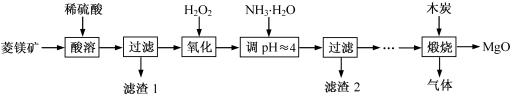
氧化镁在医药、建筑等行业应用广泛,以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶,也不参加反应)为原料制备高纯氧化镁的实验流程如下:
资料:① 不同氢氧化物沉淀的pH范围:
氢氧化物
Fe(OH)3
Mg(OH)2
开始沉淀的pH
1.5
8.6
完全沉淀的pH
3.2
11.1
② 硫在常温下是一种淡黄色固体,硫的熔点约为115.2℃,沸点约为444.7℃;
③ 高锰酸钾溶液只吸收SO2,不吸收CO2;
④ 碱溶液既吸收SO2,又吸收CO2。
试回答下列问题:
(1)MgCO3与稀硫酸反应的化学方程式为 。
(2)加入H2O2目的是在酸性条件下将FeSO4氧化成Fe2(SO4)3,同时生成水,发生反应的化学方程式为 。
(3)加氨水调节溶液的pH约为4的目的是 ,反应的化学方程式为
。
(4)煅烧过程存在以下反应:
2MgSO4+C
2MgO+2SO2↑+CO2↑
MgSO4+C
MgO+SO2↑+CO↑
MgSO4+3C
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。(假设每步反应都完全进行)
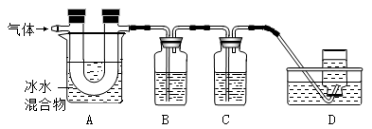
① A中现象是:玻璃管壁出现 色固体;
② B中盛放的溶液可以是 (填字母),实验现象为 ;
a.Ca(OH)2 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③ D中收集的气体是 (填化学式)。
九年级化学填空题困难题查看答案及解析
-
氧化镁在医药等行业应用广泛。实验室以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于水和酸)为原料制备高纯氧化镁的实验流程如下:
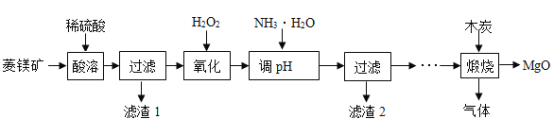
(1)为了提高“酸浸”的效果,可采取的措施有:适当升高温度、____________。MgCO3与稀硫酸反应的化学方程式为_________________。
(2)“氧化”过程中,将FeSO4全部转化为Fe2(SO4) 3,然后加氨水,调节溶液的PH范围为______________。(已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表)
对应离子
Fe3+
Fe2+
Mg2+
开始沉淀时的pH
2.7
7.9
9.4
完全沉淀时的pH
3.7
9.6
11.4
(3)过滤后得到滤渣2和滤液,滤渣2是______(填化学式),此时滤液中的阳离子一定含有____________(填离子符号)。
(4)煅烧过程存在以下反应:
;
;
已知:①硫在常温下是一种淡黄色固体,硫的熔点约为115.2°C,沸点约为444.7°C;②高锰酸钾溶液与SO2反应会褪色,且只吸收SO2,不吸收CO2;③碱溶液既吸收SO2,又吸收CO2。利用下图装置对煅烧产生的气体进行检验并收集。
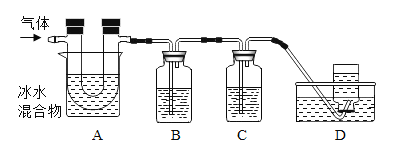
①集气瓶B中盛放的溶液是_______________(填字母),C中盛放的溶液是_____________(填字母)。
a Ca(OH)2溶液
b KMnO4溶液
c NaOH溶液
d BaCl2溶液
②装置D的作用是__________________________。
九年级化学流程题困难题查看答案及解析
-
向一定质量的硫酸钙固体中加入过量的氢氧化钡溶液,充分反应后过滤,得到滤液质量为108.5g,向滤液中加入21.2g碳酸钠粉末,恰好完全反应,过滤后称量滤液质量为100g,则硫酸钙固体的质量为( )
A.6.8g B.13.6g C.20.4g D.27.2g
九年级化学单选题困难题查看答案及解析