-
在研究酸和碱的化学性质时,某同学发现稀H2SO4与NaOH溶液混合后无明显现象产生,于是设计并完成了如下实验方案。
方案一:测定稀H2SO4与NaOH溶液混合前后的pH.
(1)用pH试纸测定NaOH溶液的pH,测得pH___________7 (选填“大于”、“等于”或“小于”);
(2)将定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH, pH=7。
方案二:向盛有NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸,观察到溶液由红色变成无色。
结论:稀H2SO4与NaOH溶液发生了化学反应;
在上述实验中需要用到溶质质量分数为10%的稀硫酸,现用20g溶质质量分数为98%的浓硫酸进行稀释,则需要增加水的质量为________g, 若实验过程中量水时仰视读数,则会造成所得溶液溶质质量分数_____(选填“偏大”、“不变”或“偏小”)
(3)甲酸(HCOOH)是一种具有挥发性的酸, 甲酸在热的浓硫酸中会分解生成两种氧化物;CO和H2O。如图是制取CO,用CO还原氧化铁并检验气体产物,同时收集尾气中的CO的实验装置。
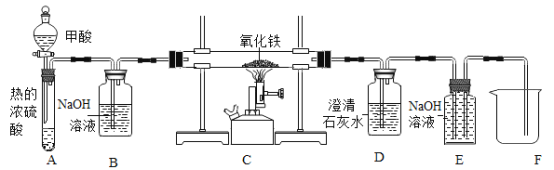
①写出E装置玻璃管内发生反应的化学方程式______。
②若没有B装置,则不能达到检验气体产物的目的,原因是_____。
③E装置可起到收集CO的作用,实验结束时,E中有部分溶液进入到F烧杯中,请设计实验证明该溶液溶质的成分中含有NaOH,写出实验步骤、现象和结论__。
(4)某特种钢村需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验:取20g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。请计算:
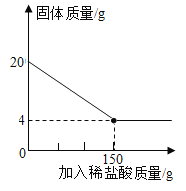
①20g赤铁矿石样品中氧化铁的质量_____。
②计算该样品中铁元素的质量分数,由此判断该赤铁矿石是否属于富铁矿石_____。
③实验中所用稀盐酸溶质的质量分数_____。
-
在研究酸和碱的化学性质时,同学发现稀 H2SO4 与 NaOH溶液混合后无明显现象产生,于是设计并完成了如下实验方案。
方案一:测定稀 H2SO4与 NaOH溶液混合前后的 pH
(1)将 pH试纸伸入某 NaOH溶液中测定 NaOH溶液的 pH,测得 pH_____7(选填“大于”、“等于”或“小于”);
(2)将一定量的稀 H2SO4加入该 NaOH溶液中,混合均匀后测定其 pH,pH=7。
方案二:向盛有 NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸,观察到溶液由红色变成无色。
结论:稀 H2SO4与 NaOH溶液发生了化学反应,反应的化学方程式为:_____;
上述实验操作中错误的是_____。
-
在研究酸和碱的化学性质时,同学发现稀 H2SO4 与 NaOH溶液混合后无明显现象产生,于是设计并完成了如下实验方案。
方案一:测定稀H2SO4与NaOH溶液混合前后的pH。
(1)将pH试纸伸入某 NaOH溶液中测定NaOH溶液的 pH,测得 pH_____7(选填“大于”、“等于”或“小于”);
(2)将一定量的稀 H2SO4加入该 NaOH溶液中,混合均匀后测定其 pH,pH=7。
方案二:向盛有 NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸,观察到溶液由红色变成无色。
结论:稀 H2SO4与 NaOH溶液发生了化学反应,反应的化学方程式为:_____;上述实验操作中错误的是_____。
(3)甲酸(HCOOH)是一种具有挥发性的酸,甲酸在热的浓硫酸中会分解生成两种氧化物:CO和_____(写化学式)。如图是制取CO,用CO还原氧化铁并检验气体产物,同时收集尾气中的CO的实验装置。
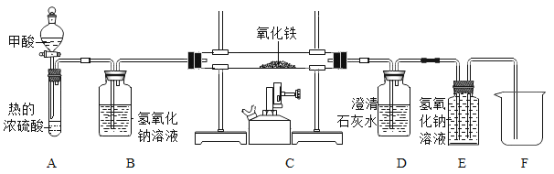
①写出C装置内玻璃管中发生反应的化学方程式:_____
②若没有B装置,则不能达到检验气体产物的目的,原因是什么_____?
③E装置可起到收集 CO的作用,实验结束时,E中有部分溶液进入到F烧杯中,请设计实验证明该溶液溶质的成分中含有NaOH,写出实验步骤、现象和结论_____。
(4)工业上冶炼 150吨含杂质为 2%的生铁,需要含杂质20%的赤铁矿石多少吨___?
-
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案设计、实施和评价.
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH________7(填“大于”、“等于”或“小于”),然后将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后再测定其pH,发现其pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且________过量.
(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应
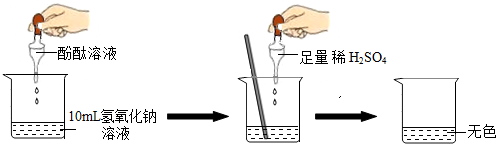
如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为________色.根据上述过程中的颜色变化,确定稀H2SO4与NaOH溶液发生了反应,该反应的化学方程式为________.
②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的BaCl2溶液 | 出现白色沉淀 | 稀H2SO4过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀H2SO4过量 |
| 方案三 | 取样,加入Na2CO3粉末 | 有气体产生 | 稀H2SO4过量 |
方案三中反应的化学方程式为________.上述设计的实验方案中,不正确的是________(填“方案一”、“方案二”或“方案三”).错误的原因是________.请你再设计一个实验方案确定稀H2SO4是否过量,你选用________(填药品或者方法).
-
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案的设计、实施和评价.
①方案一:测定稀H2SO4与NaOH溶液混合前后的pH(20℃).
测定某NaOH溶液的pH,pH______7(选填“大于”、“等于”或“小于”).
将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH,pH 小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且______过量.
②方案二:观察到______.
(根据图示实验步骤,描述实验现象)
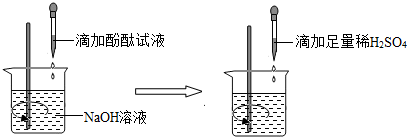
结论:稀H2SO4与NaOH溶液发生了化学反应,反映的化学方程式为______.
③实验室里还可以用稀硫酸与锌粒反应制取氢气,反应的化学方程式是______.
④为了进一步获取稀H2SO4与NaOH溶液确实发生了化学反应的证据,依据中和反应是______(选填“放热”、“吸热”或“无热量变化”)的反应.
-
研究酸和碱的化学性质时,某化学兴趣小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应。请与他们一起完成实验方案的设计、实施和评价。
(实验设计)
方案一:测定稀H2SO4与NaOH溶液混合前后的pH。
①测定某NaOH溶液的pH;
②将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH。若pH<7,则稀H2SO4与NaOH溶液发生了化学反应,并且_______过量。
方案二:向盛有NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸至过量,观察到_______的现象,则证明稀H2SO4与NaOH溶液发生了化学反应。
(交流与反思)上述两个方案在设计思想上的相同点是_______。
(延伸学习)为更好地探究中和反应,我们引入滴定度这个概念,滴定度是指每毫升标准溶液相当于被测定物质的克数,通常用T[M1/M2]表示,如T[H2SO4/NaOH]=0.04g/mL,表示每毫升标准硫酸溶液恰好中和0.04 g NaOH。则若要使标准盐酸对CaO的滴定度T[HCl/CaO]=0.0056g/mL,则盐酸对NaOH的滴定度是__________g/mL。
-
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应。请与他们一起完成实验方案的设计、实施和评价。
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(20℃)
①将pH试纸伸入某NaOH溶液中,测定NaOH溶液的pH,pH_____7(选填“大于”、“等于”或“小于”);实验操作中的错误是_____。
②将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH,pH小于7。
结论:稀H2SO4与NaOH溶液发生了化学反应,并且_____(填写溶质的化学式)过量。
(2)方案二:向盛有NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸至过量,观察到_____的现象。
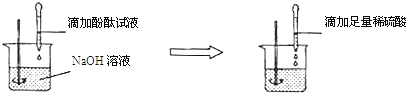
结论:稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为_____。
(3)上述两个方案在设计思想上的相同点是_____。
(4)为了进一步获取稀H2SO4与NaOH溶液确实发生了化学反应的证据,依据中和反应是_____(选填“放热”、“吸热”或“无热量变化”)的反应,采用同温下的稀H2SO4与NaOH溶液进行实验,整个实验中至少需要测定溶液温度_____次。
(5)实验室存放的常见的碱除了氢氧化钠外,还有氢氧化钙,它们存放时都需密封保存,请用化学方程式解释澄清的石灰水必须密封保存的原因_____。
-
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案的设计、实施和评价.
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(20℃)测定某NaOH溶液的pH,pH____7(选填“大于”、“等于”或“小于”).将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH,pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且__过量.
(2)方案二:向盛有NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸至过量,观察到_____的现象.
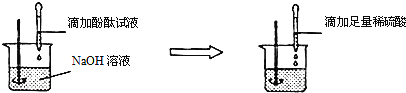
结论:稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为:_______.
(3)上述两个方案在设计思想上的相同点是_______.
(4)为了进一步获取稀H2SO4与NaOH溶液确实发生了化学反应的证据,依据中和反应是_____(选填“放热”、“吸热”或“无热量变化”)的反应,采用同温下的稀H2SO4与NaOH溶液进行实验,整个实验中至少需要测定溶液温度_____次.
(5)实验结束后蒸发稀H2SO4与NaOH溶液完全反应所得溶液15g,得到Na2SO4晶体2.2g,则该溶液是______(填“饱和”与“不饱和”)。(20℃时Na2SO4的溶解度是22g)
-
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应。请与他们一起完成实验方案的设计、实施和评价。
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(20℃)。
测定某NaOH溶液的pH,pH _____7(选填“大于”、“等于”或“小于”)。将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH ,pH 小于7。
结论:稀H2SO4与NaOH溶液发生了化学反应,并且_____过量。
(2)方案二:观察_____。(根据图示实验步骤,概括方案要点)
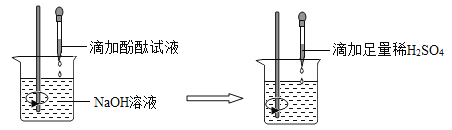
结论:稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为_____。
(3)上述两个方案在设计思想上的相同点是_____。
(4)为了进一步获取稀H2SO4与NaOH溶液确实发生了化学反应的证据,依据中和反应是_____(选填“放热”、“吸热”或“无热量变化”)的反应,采用同温下的稀H2SO4与NaOH溶液进行实验,整个实验中至少需要测定溶液温度_____次。
-
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案的设计、实施和评价.
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(20℃)测定某NaOH溶液的pH,pH______ 7(选填“大于”、“等于”或“小于”).将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH,pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且______过量.
(2)方案二:向盛有NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸至过量,观察到______的现象.
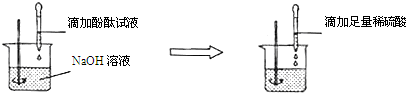
结论:稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为______.
(3)上述两个方案在设计思想上的相同点是______.
(4)为了进一步获取稀H2SO4与NaOH溶液确实发生了化学反应的证据,依据中和反应是______(选填“放热”、“吸热”或“无热量变化”)的反应,采用同温下的稀H2SO4与NaOH溶液进行实验,整个实验中至少需要测定溶液温度______ 次.








