-
根据图中资料信息回答问题:碱石灰敞口放置过程中的现象是_____,完全变质后的物质是_____,碱石灰可以干燥的气体是_____(写出一种化学式即可)。

-
如图所示为实验室中常见的气体制备、干燥、净化和收集实验的部分仪器.试根据题目要求,回答下列问题:(设过程中所有发生的反应都恰好完全进行)

(1)用石灰石和稀盐酸为原料制取并收集干燥、纯净的二氧化碳气体.某同学设计的仪器连接顺序为:A→C→D→F.
①仪器A中发生的化学反应方程式是________.
②上述方案是否合理?请简述理由.________.
(2)欲用纯净的一氧化碳气体,测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应后气体生成物的性质.某同学所选仪器的连接顺序为:一氧化碳→B→E.
①仪器B中看到的实验明显现象是________.
②仪器E中发生反应的化学方程式为________.
③通过测量反应前、后B处大玻璃管的质量变化,来计算氧化铁样品的纯度.若实验结束后大玻璃管中的物质里还有少许红色氧化铁,则计算出样品纯度的结果将________(填“偏大”、“偏小”、“不受影响”其中之一).
④从环境保护的角度考虑,该套实验装置存在的不足是________,请提出你的合理建议________.
-
如图所示为实验室中常见气体的制备、干燥、收集和性质实验的部分仪器.试根据题目要求,回答下列问题:(设过程中所有发生的反应都恰好完全进行).
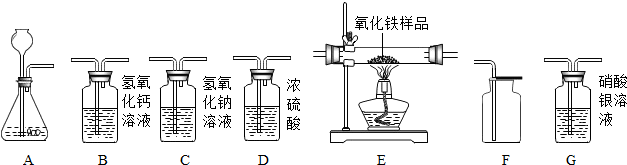
(1)若以石灰石和稀盐酸(盐酸有挥发性)为原料制取二氧化碳气体,现要制备并收集一瓶干燥、纯净的二氧化碳气体.
①所选仪器的连接顺序为________(填写仪器序号字母).
②生成二氧化碳的化学方程式为:________.
③要除去二氧化碳气体中混有的氯化氢气体,请从NaOH溶液、水、AgNO3溶液中选择一种,并简述理由________.
(2)实验室制得的一氧化碳中常混有二氧化碳和水蒸气,欲用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,某同学所选装置的连接顺序为:制得的一氧化碳气体→装置C→装置D→装置E→装置B.(友情提示:3CO+Fe2O3 2Fe+3CO2)
2Fe+3CO2)
①装置C的作用是________;
②装置E中看到的现象是________.
③该实验产生的尾气会造成环境污染,请你写出处理尾气的方法________.
-
(2分)食品保鲜剂可以有效地防止食品的腐败变质。食品保鲜的措施有添加防腐剂、填充保护气体、放置干燥剂和脱氧保鲜剂。请回答:
(1)可作为食品保鲜剂,且被称作“双吸剂”的物质的化学式为 。
(2)用文字解释为什么该物质被称为“双吸剂”? 。
-
碳酸氢铵是一种化肥,常装在丝袋子中.生产厂家有下面使用说明:“本产品宜存贮于干燥阴冷处,防止受潮,避免曝晒或与碱性物质(如熟石灰)混合使用,以免变质,造成肥效损失.”根据上面叙述,回答问题:
(1)碳酸氢铵的性质;
(2)碳酸氢铵受热易分解生成氨气和两种常见的氧化物,请依据信息写出该反应的化学方程式为.
-
在实验室中,某同学发现了一瓶敞口放置的氢氧化钙粉末试剂,并对其产生兴趣,进行了如下实验。
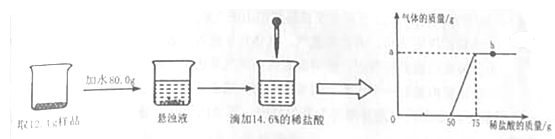
根据实验过程和图象提供的信息,回答下列问题:
(1)完全反应后生成气体的质量是 g。
(2)b点溶液中的溶质为 (填名称)。 _
(3)求恰好完全反应时所得溶液中溶质的质量分数?(利用化学方程式进行计算,书写计算过程,结果精确到0.1%)
-
碱石灰是氧化钙和氢氧化钠的固体混合物,是实验室常用的干燥剂.相关信息如下表所示.同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究.
[小资料]
①碱石灰是氧化钙、氢氧化钙的固体混合物.易吸收空气中的水蒸气和二氧化碳.
②氯化钙溶液显中性. |
[提出问题]实验室中久置的碱石灰样品的成分是什么?
[进行猜想]久置的碱石灰样品中可能含有CaO、NaOH、Na2CO3、Ca(OH)2、CaCO3等成分.用化学方程式表示样品中含有Ca(OH)2或Na2CO3可能含有的原因______(写一个).
[探究过程]

试回答下列问题:
(1)操作①的名称是______,溶液C中一定含______离子.
(2)溶液A中加入CaCl2溶液后产生固体,说明样品中一定含有______,反应的方程式为______.
(3)向溶液A中加入CaCl2溶液后,证明CaCl2溶液过量的方法是______.
[实验结论]
依据上述实验操作过程及现象,综合对滤液和固体成分的探究,下列对样品成分的分析正确的是______(填序号).
①样品中一定含NaOH
②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种
[拓展延伸]
为测定实验室中一瓶变质的烧碱中NaOH的含量,某同学取适量的烧碱样品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g.请分析计算:
(1)反应产生的CO2的质量为______ g.
(2)若所取烧碱样品为50.0g,则样品中NaOH的质量分数是多少?(写出计算过程)______.
(3)用同浓度的硫酸,分别与未变质、部分变质、或全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等.从钠元素质量守恒的角度解释其原因是:______.
-
碱石灰是氧化钙和氢氧化钠的固体混合物,是实验室常用的干燥剂.相关信息如下表所示.同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究.
[小资料]
①碱石灰是氧化钙、氢氧化钙的固体混合物.易吸收空气中的水蒸气和二氧化碳.
②氯化钙溶液显中性. |
[提出问题]实验室中久置的碱石灰样品的成分是什么?
[进行猜想]久置的碱石灰样品中可能含有CaO、NaOH、Na2CO3、Ca(OH)2、CaCO3等成分.用化学方程式表示样品中含有Ca(OH)2或Na2CO3可能含有的原因______(写一个).
[探究过程]

试回答下列问题:
(1)操作①的名称是______,溶液C中一定含______离子.
(2)溶液A中加入CaCl2溶液后产生固体,说明样品中一定含有______,反应的方程式为______.
(3)向溶液A中加入CaCl2溶液后,证明CaCl2溶液过量的方法是______.
[实验结论]
依据上述实验操作过程及现象,综合对滤液和固体成分的探究,下列对样品成分的分析正确的是______(填序号).
①样品中一定含NaOH
②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种
[拓展延伸]
为测定实验室中一瓶变质的烧碱中NaOH的含量,某同学取适量的烧碱样品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g.请分析计算:
(1)反应产生的CO2的质量为______ g.
(2)若所取烧碱样品为50.0g,则样品中NaOH的质量分数是多少?(写出计算过程)______.
(3)用同浓度的硫酸,分别与未变质、部分变质、或全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等.从钠元素质量守恒的角度解释其原因是:______.
-
将干燥的CO2气体通入如图所示的装置中(上下敞口)。图中①④放置浸泡紫色石蕊溶液(适量)的湿润棉球,②③放置用紫色石蕊溶液染成紫色的干燥棉球。回答问题。
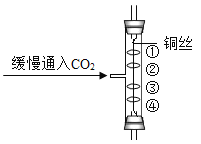
(1)请分别描述能证明下列结论的实验现象①CO2的密度比空气大_____,②CO2不具备使紫色石蕊变色能力:_____。
(2)取出已变红的棉花球,然后用酒精灯微热,能观察到棉球又变成紫色,原因是________。
-
请用化学方程式解释下列实验现象或实验事实.
(1)某些食品常用生石灰做干燥剂.
(2)工业上常用纯碱和熟石灰来制取火碱.
(3)石灰水敞口放置会变质.








