-
碳酸钠在实际生产、生活中有着广泛的用途,如制造玻璃、造纸和纺织等。
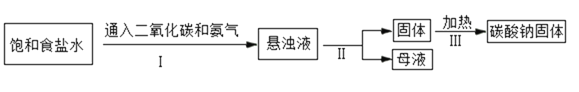
(1)碳酸钠俗称苏打或____。如图为侯氏制碱法的流程图,通过步骤I后得到的悬浊液中有小苏打(在该溶液中难溶)和一种氮肥,请写出步骤I中发生反应的化学方程式:_____;上述过程中得到的氮肥遇碱会生成具有刺激性气味的______(填化学式),该气体能使_____;从流程图中可得出小苏打的一条化学性质是_____。
(2)氢氧化钠在空气中容易变质生成碳酸钠,现有放在空气中一段时间的氢氧化钠溶液,其中溶质的成分可能是:猜想①:NaOH;猜想②:Na2CO3;猜想③:_____。请设计实验证明猜想③正确。(写出相关的步骤和现象)________
(3)某海洋化工集团生产的碳酸钠产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%。为测定该产品中碳酸钠的质量分数,现取11.0g碳酸钠样品放入烧杯中,称得烧杯及所盛碳酸钠样品的总质量为158.0g,然后向烧杯中加入100g稀盐酸,充分反应,实验数据记录如下:
| 反应时间/min | 3 | 6 | 9 | 12 |
| 烧杯及所盛物质的总质量/g | 255.8 | 254.0 | 253.6 | 253.6 |
请你据此分析计算,该产品中碳酸钠的质量分数_____(是、否)符合标准。(写出计算过程,结果精确到0.1%)
(4)小强同学想在社区宣传栏出一期“低碳减排·绿色生活”专刊,内容之一是汽车耗油量与二氧化碳排放量间关系。已知:①汽油密度约为0.7kg/L;②汽油(假定其为纯净物,根据汽油中C、H组成关系,其化学式可简单表示为CH2,其燃烧的化学方程式可表示为:2CH2+3O2 2CO2+2H2O;请计算4升汽油完全燃烧生成二氧化碳的质量______?
2CO2+2H2O;请计算4升汽油完全燃烧生成二氧化碳的质量______?
-
碳酸氢钠在生产、生活中有着广泛的用途。碳酸氢钠的俗称是( )
A. 纯碱 B. 苏打 C. 熟石灰 D. 小苏打
-
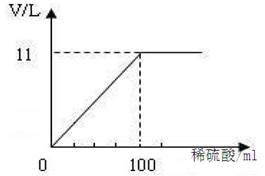
(10分)碳酸钠(Na2CO3)俗称苏打,是一种白色固体,广泛用于玻璃、造纸、纺织和洗涤剂的生产等。它能与稀硫酸等酸反应生成CO2。(Na2CO3与稀硫酸反应的化学方程式为:Na2CO3+H2SO4===Na2SO4+CO2↑+H2O)现将100g Na2CO3固体粉末(含有Na2SO4杂质)加入202g水中,完全溶解,再加入100mL稀硫酸(密度为1.2g/mL),恰好完全反应后使气体全部逸出,固体粉末的质量与产生CO2体积的关系如图(该状况下,CO2的密度为2g/L)。通过计算:
(1)生成CO2的质量是________________g;
(2)求100mL稀硫酸中溶质的质量和反应后所得溶液的溶质质量分数。
-
下列常见的盐在生产、生活中的用途不合理的是( )。
A.用亚硝酸钠腌制食品
B.碳酸钠广泛应用于玻璃、造纸、纺织和洗涤剂的生产
C.用纯碱消耗面粉发酵生成的酸
D.天安门前的华表是用大理石做的,碳酸钙还可用作补钙剂
-
碳酸钠俗称纯碱、苏打,广泛用于玻璃、造纸、防治和洗涤剂的生产等,纯碱工业的发展对于促进国民经济发展发挥了重要的作用。下列有关纯碱碳酸钠的叙述不正确的是( )
A.用纯碱可除去面团发酵时产生的有机酸
B.可用纯碱代替洗涤灵,用于洗涤餐具表面的油污
C.纯碱溶液的pH>7呈碱性,但不属于碱,而是盐类
D.“冬天捞碱”可说明纯碱的溶解度随温度的变化不大
-
在工业上,碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
【资料卡片】
(1)碳酸钠俗称纯碱、____。以纯碱和熟石灰为原料可以制烧碱,化学方程式为________。
(2)1921年,_______(填字母)发明了将制碱与制氨结合起来的联合制碱法,大大提高了原料的利用率。
A.拉瓦锡 B.道尔顿 C.侯德榜 D.张青莲
【定性实验】食盐是联合制碱法的主要原料之一,因此制得的纯碱中含有少量氯化钠。为了检验纯碱样品中存在氯离子,需要用到的药品是__________(填字母)。
A.氯化钡溶液 B.硝酸银溶液 C.稀硝酸 D.稀盐酸
【定量实验】将12.0g纯碱样品溶于水,加入足量氯化钡溶液,充分反应后,过滤、洗涤、低温干燥,得到19.7g沉淀。计算纯碱样品中碳酸钠的质量分数。__________(写出计算过程,结果保留一位小数)
【实验设计与评价】甲同学设计了如图实验装置,通过测量一定质量的纯碱样品与足量稀硫酸反应后产生二氧化碳的体积,进一步计算纯碱样品中碳酸钠的质量分数。
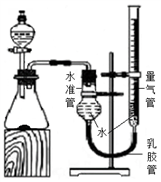
(1)检查装置的气密性时,起始状态量气管和水准管中液面相平,提高量气管,__________,证明该装置的气密性良好。
(2)乙同学认为该装置测得的二氧化碳的体积会偏小(不考虑操作上的失误),他的理由是______________________。
(3)丙同学认为该装置测得的二氧化碳的体积会偏大(不考虑操作上的失误),他的理由是______________________。
-
在工业上,碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
【资料卡片】
(1)碳酸钠俗称纯碱、____。以纯碱和熟石灰为原料可以制烧碱,化学方程式为________。
(2)1921年,_______(填字母)发明了将制碱与制氨结合起来的联合制碱法,大大提高了原料的利用率。
A.拉瓦锡 B.道尔顿 C.侯德榜 D.张青莲
【定性实验】食盐是联合制碱法的主要原料之一,因此制得的纯碱中含有少量氯化钠。为了检验纯碱样品中存在氯离子,需要用到的药品是__________(填字母)。
A.氯化钡溶液 B.硝酸银溶液 C.稀硝酸 D.稀盐酸
【定量实验】将12.0g纯碱样品溶于水,加入足量氯化钡溶液,充分反应后,过滤、洗涤、低温干燥,得到19.7g沉淀。计算纯碱样品中碳酸钠的质量分数。__________(写出计算过程,结果保留一位小数)
【实验设计与评价】甲同学设计了如图实验装置,通过测量一定质量的纯碱样品与足量稀硫酸反应后产生二氧化碳的体积,进一步计算纯碱样品中碳酸钠的质量分数。
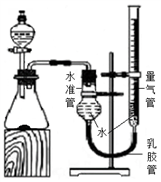
(1)检查装置的气密性时,起始状态量气管和水准管中液面相平,提高量气管,__________,证明该装置的气密性良好。
(2)乙同学认为该装置测得的二氧化碳的体积会偏小(不考虑操作上的失误),他的理由是______________________。
(3)丙同学认为该装置测得的二氧化碳的体积会偏大(不考虑操作上的失误),他的理由是______________________。
-
下列说法不正确的是( )
A. 小苏打是碳酸氢钠的俗称,是发酵粉的主要成分之一,还可以治疗胃酸过多症
B. 纯碱属于碱类,可用于玻璃、造纸、纺织、洗涤剂的生成
C. 大理石、石灰石的主要成分相同,都是重要的建筑材料
D. 胃酸中含有适量的盐酸,帮助消化,增加食欲
-
下列物质的名称、俗称与用途对应正确的是( )
| 物质名称 | 俗称 | 用途 |
| A | 碳酸钠 | 火碱 | 制造玻璃 |
| B | 碳酸氢钠 | 苏打 | 焙制糕点 |
| C | 氢氧化钙 | 消石灰 | 改良酸性土壤 |
| D | 甲醛溶液 | 福尔马林 | 长期保鲜食品 |
A.A B.B C.C D.D
-
碳酸钠广泛用于造纸、纺织、制革等工业,是一种重要的化工原料。我国侯德榜发明了将制碱与制氨结合起来的联合制碱法,为碳酸钠的工业化生产作出了巨大贡献。
(查阅资料)侯氏制碱法中主要反应:
Ⅰ.NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
Ⅱ.2NaHCO3=Na2CO3+H2O+CO2↑
(实验探究)小明以粗盐配制饱和食盐水,并采用如图1所示装置模拟制备碳酸氢钠,进而制得碳酸钠。
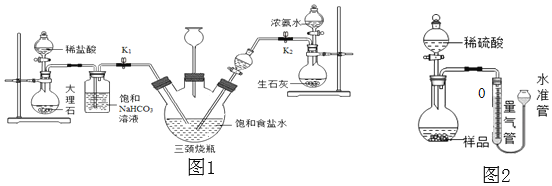
实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。请回答下列问题:
| 加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
| 剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
(1)粗盐中除了含有泥沙等不溶性杂质,还含有少量的MgCl2等。若要除去粗盐中的MgCl2,可加入过量的NaOH溶液,写出对应的化学方程式______,再过滤,然后向滤液中加入适量______,得到氯化钠溶液。
(2)饱和 NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为______。
(3)三颈烧瓶上连接的长颈漏斗的主要作用是______,有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是______;关闭K2停止通NH3后,还要继续通一段时间CO2,其目的是______。
(4)根据实验记录,计算t2时 NaHCO3固体的分解率(已分解的 NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程_____。
(拓展延伸)小华设计如图2的实验装置测定某纯碱样品 (含少量杂质NaCl)中碳酸钠的质量分数:取一定量的样品与足量稀硫酸反应,通过排饱和碳酸氢钠溶液测定生成CO2的体积,计算样品中碳酸钠的质量分数。(已知常温常压下CO2的密度是1.977g/L)
(1)如果样品质量为5.3g,则实验中选用的量气管规格最合适的是______(填字母)。
A.500mL B.1000mL C.1500mL D.2000mL
(2)若实验中测得碳酸钠质量分数偏小,下列可能的原因是______。
a.装置漏气
b.读取数据时量气管的液面低于水准管的液面
c.反应结束后烧瓶中有CO2残留
d.读取数据时仰视读数
e.稀硫酸加入烧瓶占据体积

2CO2+2H2O;请计算4升汽油完全燃烧生成二氧化碳的质量______?



